|
Метрологические
|
Содержание
1.Основные
понятия метрологии химического анализа 2
2.Классификация
погрешностей 3
2.1.Систематические
погрешности 4
2.2.Случайные
погрешности 8
3.Правильность,
воспроизводимость и точность анализа,
среднее значение и стандартное
отклонение 8
4.Нормальное
распределение 16
5.t-Распределение 19
6.Погрешность
суммы и произведения 25
7.Обнаружение
промахов 26
8.Сравнение
двух средних 28
9.Контрольные
вопросы 33
-
Основные понятия метрологии химического анализа
Метрология
(от
греч. metron
–
мера и logos
–
слово, учение) наука об измерениях и
методах достижения их единства и
требуемой точности. Один из основных
разделов метрологии посвящен методам
определения погрешности
измерений
и созданию эталонов.
До
недавнего времени широкое распространение
имел термин «ошибка измерения». По ГОСТ
16263-70 этот термин относится к категории
нерекомендуемых. Теория погрешности
измерений основана на использовании
аппарата теории
вероятности и
математической
статистики.
Метрологическими
характеристиками методик анализа помимо
погрешности являются:
-
правильность;
-
воспроизводимость;
-
интервал
определяемых содержаний; -
чувствительность;
-
предел
обнаружения
или
предел
определения
(при
определении микроконцентраций).
Нельзя
не отметить также, что в результате
исследований на стыке прикладной
математики и экспериментальной химии
возникла новая отрасль науки, получившая
название хемометрика.
Наряду
с рассмотрением погрешностей и других
вопросов метрологии в хемометрике
изучают такие разделы, как планирование
эксперимента и
оптимизация,
распознавание образов и
т.д.
-
Классификация погрешностей
Погрешностью
измерения
называют отклонение результата измерения
от истинного значения измеряемой
величины.
Погрешности
могут быть классифицированы по нескольким
признакам. При классификации по способу
выражения различают абсолютные
и
относительные
nогрешности, по
характеру проявления – систематические
и
случайные,
по
способу обработки результатов параллельных
определений – средние
арифметические и
средние
квадратические и
т.д.
Абсолютную
погрешность
анализа Δхi
определяют из соотношения:
![]() ,
,
где
хi
–
результат анализа; μ
–
истинное содержание анализируемого
компонента в пробе.
Отношение
абсолютной погрешности измерения к
истинному значению измеряемой величины
называют относительной
погрешностью измерения.
Обычно
относительную погрешность выражают в
процентах, хотя могут быть использованы
и доли единицы:

Истинное
содержание анализируемого компонента
в пробе остается неизвестным вследствие
погрешности анализа. В практических
расчетах вместо истинного используют
так называемое действительное
содержание, равное
среднему арифметическому нескольких
параллельных определений.
Погрешность
измерения зависит от многих факторов:
от класса точности применяемых приборов,
методики измерения, индивидуальных
особенностей наблюдателя и т.д.
Погрешность
измерения, которая при повторных
измерениях остается постоянной или
закономерно изменяется, называют
систематической
погрешностью.
Знак
данной систематической погрешности от
опыта к опыту не меняется. Систематическая
погрешность или только занижает, или
только завышает результат анализа.
Погрешность,
которая при повторных измерениях
изменяется случайным образом, называют
случайной
погрешностью
измерения.
Знак
случайной величины в серии измерений
не остается постоянным и от опыта к
опыту меняется.
Грубые
погрешности, существенно превышающие
ожидаемые при данных условиях, называют
промахами.
Они
обычно бывают следствием грубых
оперативных погрешностей аналитика
(потеря раствора с осадком при фильтровании,
потеря осадка при прокаливании или
взвешивании и т.д.).
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #

Погрешности в химическом анализе 1

Если получено большое количество результатов n >20, то это число аналитических измерений называют генеральной совокупностью. Генеральная совокупность — гипотетическая совокупность Погрешности в химическом всех мысленных результатов (от + до — ). анализе Если n < 20, то результаты составляют выборку, которая рассматривается как выборка n результатов из генеральной совокупности. Под истинным значением следует понимать значение, известное с высокой точностью и потому принимаемое в качестве истинного. Обозначается или 2

Среднее, среднее арифметическое и выборочное среднее являются синонимами и представляют собой частное от деления суммы результатов отдельных измерений на число измерений в выборке. 3

Медианой выборки называют результат, относительно которого число результатов с меньшим и большим значением одинаково. Если выборка состоит из нечетного числа измерений, в качестве медианы берут центральную точку, для выборки с четным числом измерений, медианой считают среднее пары центральных измерений. Например: 4

КЛАССИФИКАЦИЯ ПОГРЕШНОСТЕЙ ХИМИЧЕСКОГО АНАЛИЗА По способу вычисления погрешности можно разделить на абсолютные и относительные. v Абсолютная погрешность равна разности между средним из измеренных значений величины ( ) и истинным значение ( истин. ) этой величины: В зависимости от знака абсолютные погрешности могут быть разделены на положительные и отрицательные. (погрешности единичных определений) v. Относительная погрешность может быть выражена в долях или процентах: Относительная погрешность обычно берется по модулю и знака не имеет. 5
Классификация погрешностей по характеру причин, их вызывающих. Систематические • погрешности, вызываемые известными причинами или причины которых можно установить при детальном рассмотрении анализа и устранить. Результаты анализа отклоняются от истинного значения на постоянную величину, т. е. она постоянна во всех измерениях или меняется по постоянно действующему закону. Случайные Промахи 6 • К случайным относят погрешности, хаотически меняющиеся от измерения к измерению, причины которых достоверно неизвестны. Их величины могут быть оценены с применением методов математической статистики. Сопровождают любое измерение. • Это резко искажающая результат анализа и обычно легко обнаруживаемая погрешность, вызванная, как правило, небрежностью или некомпетентностью химика-аналитика.
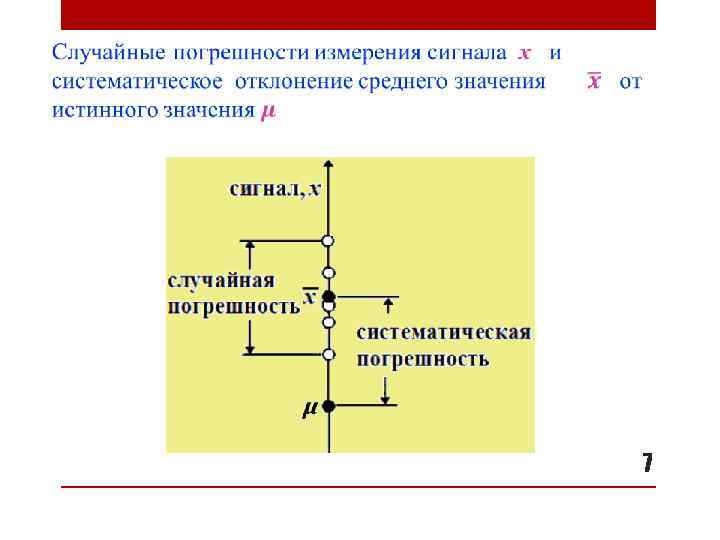
7

Общая погрешность одного единичного результата анализа, ei , складывается из случайной и систематической составляющей: 8

Деление погрешностей на систематические и случайные в известной степени условно. Систематические погрешности одной выборки результатов при рассмотрении большого числа данных могут переходить в случайные. В то же время многие случайные погрешности могут быть уменьшены или исключены методами, подобными методам уменьшения или исключения систематических погрешностей. 9
Систематические погрешности I тип Погрешности известной природы, значения которых могут быть рассчитаны и учтены путем введения соответствующих поправок 10 II тип Инструментальные, методические, реактивные, индивидуальные и т. д. III тип Причины не известны. Наиболее трудно выявить и исключить. Устанавливаются после пересмотра всех этапов анализа

Систематическую погрешность характеризует понятие правильность. Правильность измерений есть близость к нулю систематических погрешностей, т. е. это фактически означает близость полученного значения к значению принятому за действительное и выражается абсолютной и относительной погрешностью. Основные способы проверки правильности: • способ «введено—найдено «; • сравнение результатов анализа с результатом, полученным другим независимым методом; • проведение анализа стандартного образца. 11

Стандартные образцы — это образцы, состав и свойства которых надежно установлены и официально удостоверены государственным учреждением. Обычно стандартные образцы анализируют на один или несколько компонентов многими методами во многих лабораториях, поэтому содержание компонентов в стандартных образцах, указанное в свидетельстве о составе образца, можно принимать за истинное значение. Непременным условием применения стандартного образца в химическом анализе является совпадение состава и свойств стандартного образца и анализируемой пробы. При использовании стандартного образца для оценки правильности метода или методики проводят многократный химический анализ стандартного образца и сравнивают найденное количество с истинным, паспортным содержанием определяемого компонента. После того как систематическая погрешность выявлена одним из описанных выше основных способов, она должна быть оценена и устранена. Численно оценить величину систематической погрешности можно лишь с точностью, лимитируемой случайными погрешностями анализа. 12

Воспроизводимость определяется согласованием нескольких результатов между собой и обычно выражается отклонением экспериментальных данных от среднеарифметического значения, т. е. воспроизводимость характеризует возможность повторного получения аналогичных результатов. При этом измерения могут выполняться в разных условиях (в разное время, разными методами и т. д. ). Сходимость измерений есть близость друг к другу результатов измерений, выполненных в одинаковых условиях. Для оценки воспроизводимости проводят сравнение результатов с другими результатами , полученными тем же путем. 13

Воспроизводимость — это лишь одна из составляющих точности результатов анализа. Может так случиться, что достаточно хорошо воспроизводящиеся результаты тем не менее не соответствуют действительности: найденная концентрация компонента значительно отличается от его истинного содержания в образце. Подобное систематическое отличие измеренной величины от истинной характеризуется понятием правильность. 14
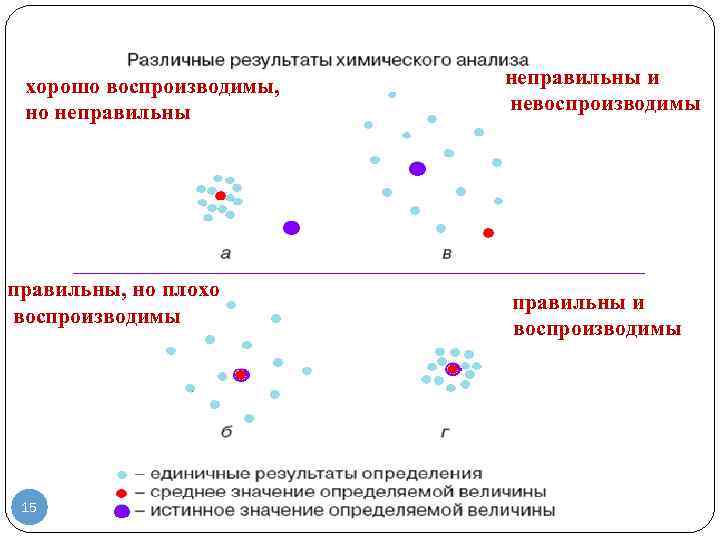
хорошо воспроизводимы, но неправильны, но плохо воспроизводимы 15 неправильны и невоспроизводимы правильны и воспроизводимы
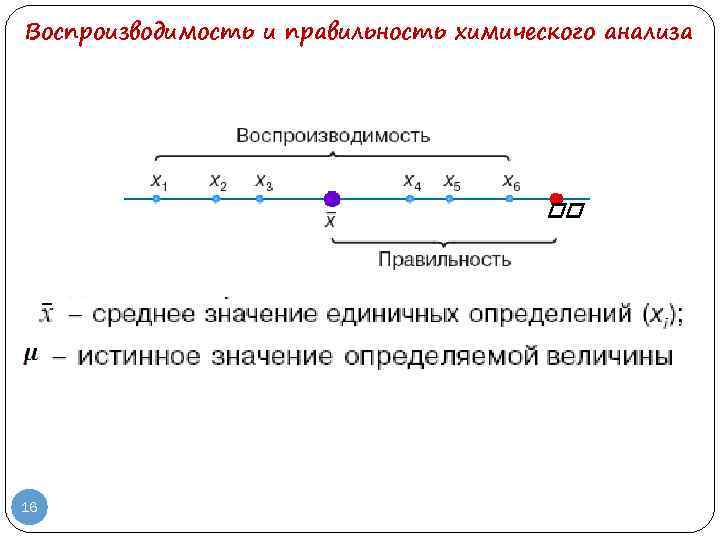
Воспроизводимость и правильность химического анализа 16

Обработка результатов химического анализа методами математической статистики Предварительно систематические погрешности должны быть выявлены и устранены или переведены в разряд случайных. Данные анализа при этом являются случайными величинами с определенным распределением вероятности. Объективная возможность появления той или иной случайной величины задается ее вероятностью. случайная величина считается заданной, если известна ее функция распределения, вероятность ее попадания в тот или иной интервал. Одной из основных задач аналитика при оценке случайных погрешностей химического анализа является нахождение функции распределения, которой описываются экспериментальные данные. 17

Если n > 20 Дисперсия (σ2) характеризует рассеяние случайной величины относительно своего математического ожидания и определяется как математическое ожидание квадратов отклонений х от . Положительное значение корня квадратного от дисперсии (σ) называют стандартным отклонением и также используют для характеристики рассеяния случайной величины х относительно генерального среднего . 18
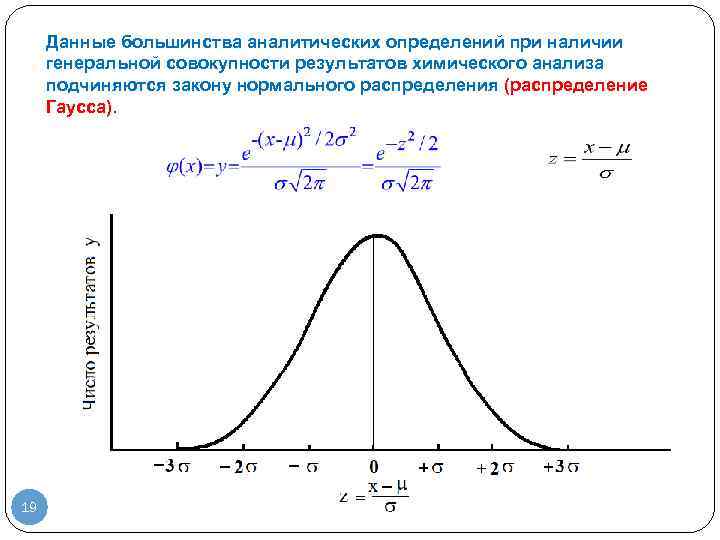
Данные большинства аналитических определений при наличии генеральной совокупности результатов химического анализа подчиняются закону нормального распределения (распределение Гаусса). 19

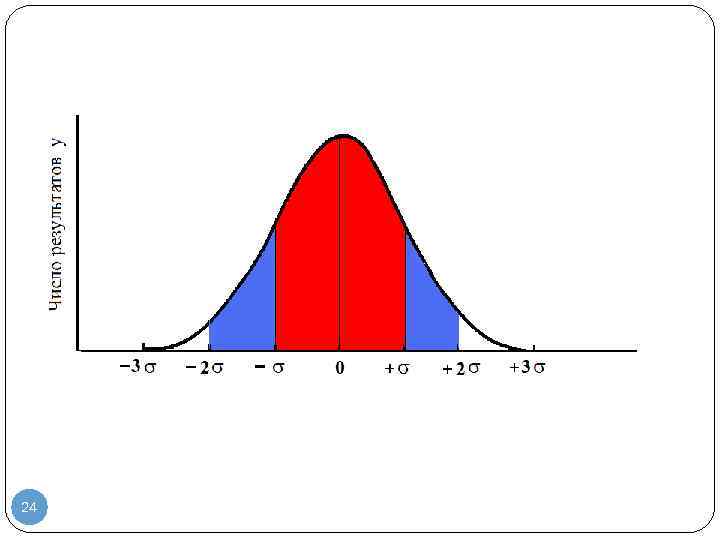
Анализ кривой показывает: Каждой положительной погрешности соответствует отрицательная; Относительная вероятность измерений, содержащих небольшую погрешность очень велика. 68. 26% результатов попадает в интервал 95. 44% — 99. 73% — и только 0. 26% результатов не попадает в этот интервал 20

Свойства нормального распределения Гаусса. 1. Максимум кривой распределения приходится на x= (в этом легко убедиться, продифференцировав и приравняв нулю производную (х)) Изменение параметра не изменяет формы кривой, а приводит к ее смещению по оси х. 2. График дифференциального закона распределения представляет собой колообразную кривую, симметричную относительно максимума. 3. Значение функции плотности вероятности в максимуме определяется только параметром . 4. Кривая (х) имеет две расположенные симметрично точки перегиба на расстоянии от линии симметрии х= , равном . 21
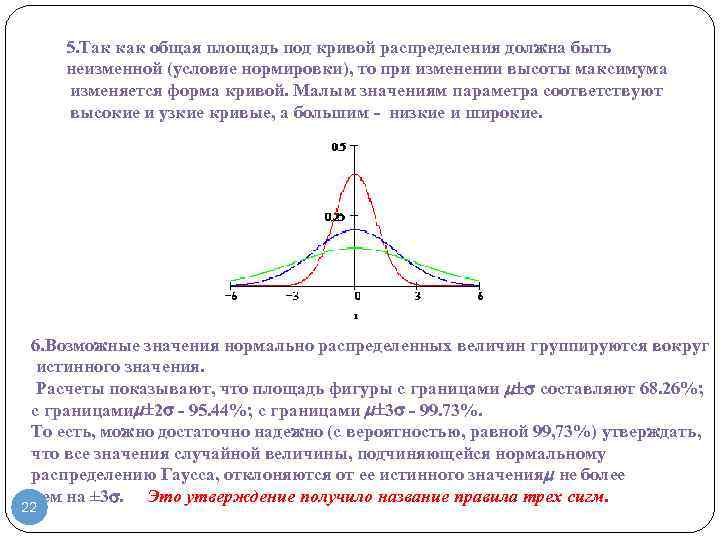
5. Так как общая площадь под кривой распределения должна быть неизменной (условие нормировки), то при изменении высоты максимума изменяется форма кривой. Малым значениям параметра соответствуют высокие и узкие кривые, а большим — низкие и широкие. 6. Возможные значения нормально распределенных величин группируются вокруг истинного значения. Расчеты показывают, что площадь фигуры с границами составляют 68. 26%; с границами 2 — 95. 44%; с границами 3 — 99. 73%. То есть, можно достаточно надежно (с вероятностью, равной 99, 73%) утверждать, что все значения случайной величины, подчиняющейся нормальному распределению Гаусса, отклоняются от ее истинного значения не более чем на ± 3. Это утверждение получило название правила трех сигм. 22

23
24
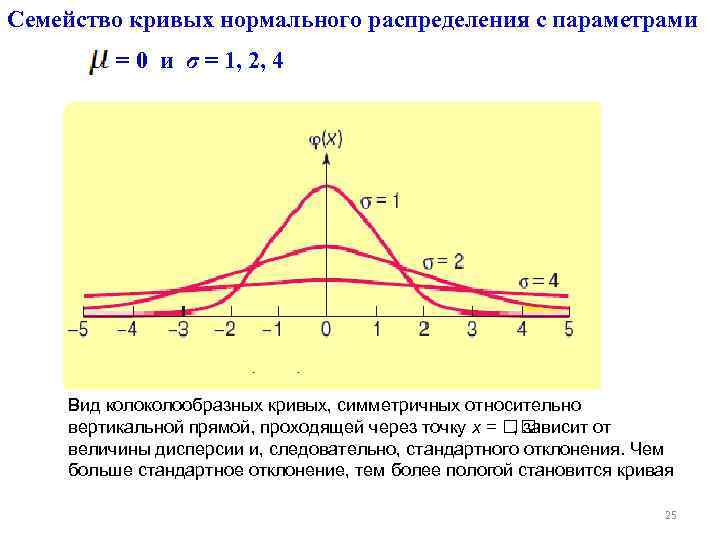
Семейство кривых нормального распределения с параметрами = 0 и σ = 1, 2, 4 Вид колообразных кривых, симметричных относительно вертикальной прямой, проходящей через точку х = , зависит от величины дисперсии и, следовательно, стандартного отклонения. Чем больше стандартное отклонение, тем более пологой становится кривая 25
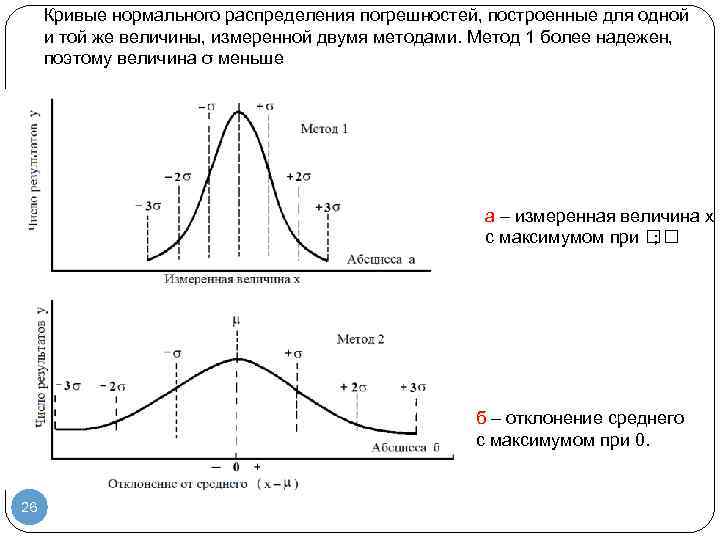
Кривые нормального распределения погрешностей, построенные для одной и той же величины, измеренной двумя методами. Метод 1 более надежен, поэтому величина σ меньше а – измеренная величина x c максимумом при ; б – отклонение среднего с максимумом при 0. 26

Если n<20 Дисперсия случайных величин На практике при проведении анализа одного и того же объекта имеем 3— 7 результатов (выборочная совокупность(n < 20)). Для оценки дисперсии 2 случайной величины используется выборочная дисперсия s 2 Для расчета выборочной дисперсии (дисперсии случайных величин), характеризующей разброс (рассеяние) полученных значений относительно среднего используют выражение: является лишь случайным приближением к σ и может довольно значительно от нее отличаться. есть центр выборки, но не обязательно является центром генеральной совокупности; n-1= f представляет собой число степеней свободы или число независимых отклонений, которые возможны внутри выборки, после того как рассчитано (одна связь была наложена на результаты при подсчете среднего) 27

Стандартное отклонение — характеризует рассеяние результатов внутри выборочной совокупности, имеет размерность измеряемой величины и рассчитывается по формуле: Стандартное отклонение является мерой разброса и характеризует случайную погрешность метода анализа. Относительное стандартное отклонение Дисперсия, стандартное отклонение и относительное стандартное отклонение характеризуют воспроизводимость результатов химического анализа. 28

Стандартное отклонение среднего 29

Нормальный закон распределения неприменим для обработки малого числа измерения выборочной совокупности (n = 3— 7) даже если генеральная совокупность в целом распределена нормально. Для малых выборок вместо нормального распределения используют распределение Стьюдента (t-распределение), которое связывает между собой три основные характеристики выборочной совокупности: ширину доверительного интервала, соответствующую ему вероятность и объем выборочной совокупности. коэффициент Стьюдента 30

Как и нормированное нормальное распределение Гаусса, t-распределение симметрично и имеет максимум при том же значении абсциссы, как и при нормальном распределении. Однако такие характеристики как высота и ширина кривой зависят от числа степеней свободы: чем меньше число степеней свободы, тем медленнее кривая сближается с осью абсцисс, тем меньше ее крутизна. При f t-распределение переходит в нормальное распределение. Практически эта разница становится мало заметной уже при f 20. . 31

В общем случае можно записать: или, что то же самое где — математическое ожидание (генеральное среднее – теоретическое значение среднего при бесконечном числе параллельных измерений; при отсутствии систематической погрешности оно равно истинному значению), экспериментальное (выборочное) среднее, полученное из конечной серии измерений, — — его стандартное отклонение, а t. P, f –так называемый коэффициент Стьюдента, зависящий как от заданной доверительной вероятности Р, так и от числа степеней свободы f величины. 32

Госсет указал, что возможно при малом числе измерений определить доверительную вероятность или доверительный интервал, когда известна S. Он вывел распределение погрешностей средних значений при малом числе измерений. По формулам Госсета составлены таблицы распределения Стьюдента, где представлены значения t, которые указываются с определенной вероятностью Р и для определенного значения f. Р- вероятность появления случайной погрешности (0. 90; 0. 95; 0. 99). 33
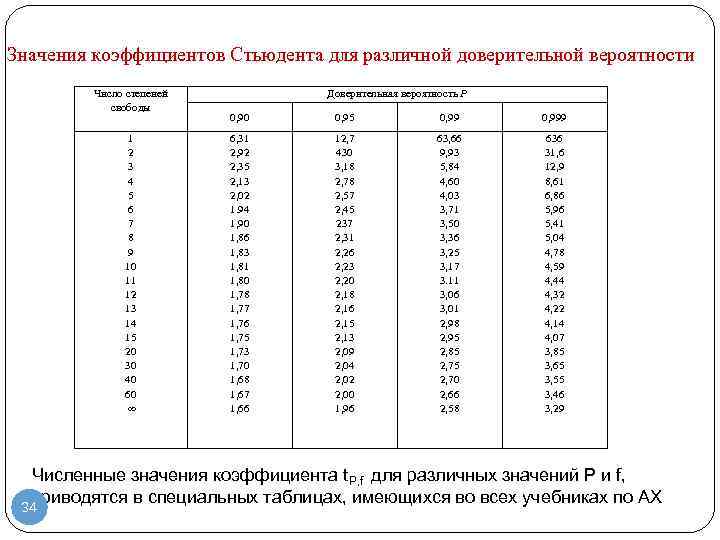
Значения коэффициентов Стьюдента для различной доверительной вероятности Число степеней свободы 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 20 30 40 60 Доверительная вероятность Р 0, 90 0, 95 0, 999 6, 31 2, 92 2, 35 2, 13 2, 02 1. 94 1, 90 1, 86 1, 83 1, 81 1, 80 1, 78 1, 77 1, 76 1, 75 1, 73 1, 70 1, 68 1, 67 1, 66 12, 7 430 3, 18 2, 78 2, 57 2, 45 237 2, 31 2, 26 2, 23 2, 20 2, 18 2, 16 2, 15 2, 13 2, 09 2, 04 2, 02 2, 00 1, 96 63, 66 9, 93 5, 84 4, 60 4, 03 3, 71 3, 50 3, 36 3, 25 3, 17 3. 11 3, 06 3, 01 2, 98 2, 95 2, 85 2, 70 2, 66 2, 58 636 31, 6 12, 9 8, 61 6, 86 5, 96 5, 41 5, 04 4, 78 4, 59 4, 44 4, 32 4, 22 4, 14 4, 07 3, 85 3, 65 3, 55 3, 46 3, 29 Численные значения коэффициента t. P, f для различных значений Р и f, приводятся в специальных таблицах, имеющихся во всех учебниках по АХ 34

, Доверительный интервал рассчитывают из стандартного отклонения S и числа параллельных определений n при помощи специального статистического коэффициента: —коэффициента Стьюдента t для выбранной доверительной вероятности P и числа степеней свободы f: Результат 35

Генеральное пределах от среднее, , до находится в , которые называются доверительными границами. чем больше число определений n, чем меньше доверительный интервал при заданной доверительной вероятности, тем выше точность анализа. Наиболее сильное влияние на величину доверительного интервала оказывает увеличение числа определений лишь до 4 -5 параллельных измерений. Дальнейшее увеличение числа параллельных проб оказывает значительно меньшее влияние. 36

Грубая погрешность или промах – это случайная погрешность результата отдельного измерения, входящего в ряд измерений, которая для данных условий резко отличается от остальных результатов этого ряда. Измерение, где допущен промах, исключается и во внимание не принимается 37

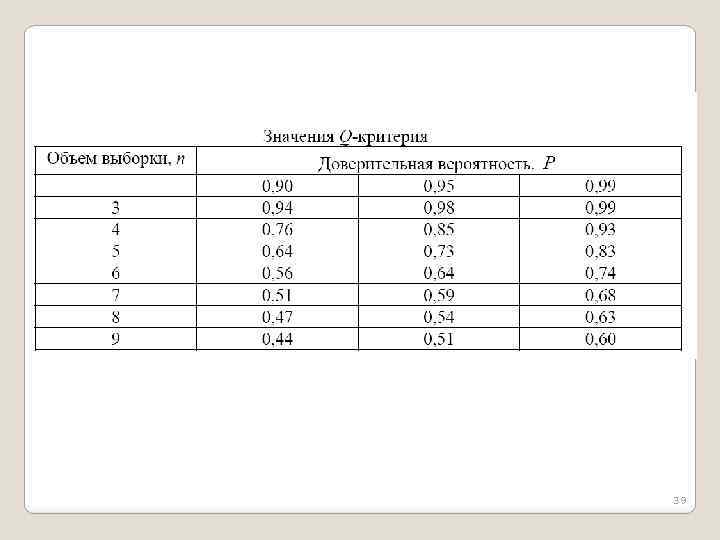
Исключение промахов Cначала расположить все результаты серии измерений по ранжиру. Сомнительное значение может находиться либо в начале ряда (х1), либо в конце (хn). Рассчитывают коэффициент Q Большее из полученных значений Q сравнивают со значением Qтабл, зависящим от выбранных доверительной вероятности Р и объема выборки n и взятом из специальной таблицы (cправочник). Доверительную вероятность для проверки промахов по Q – критерию обычно полагают равной 90 %. Если Qтабл > Qэксп, то сомнительный результат следует сохранить. 38
39

Суммирование погрешностей. Закон распространения погрешностей Для оценки общей погрешности служит закон распространения погрешностей. При наличии нескольких суммирующихся независимых друг от друга источников погрешностей для оценки общей погрешности следует сложить квадраты стандартных отклонений — дисперсии — отдельных составляющих. Для оценки погрешности произведения или частного следует сложить квадраты относительных случайных погрешностей. Пусть общая погрешность результатов анализа s 2, состоит из погрешности пробоотбора S 2 p и погрешности измерения s 2 M. При этом было отобрано т проб и каждая была проанализирована n раз. В этом случае 40

При химическом анализе воспроизводимость результатов измерений аналитического сигнала (S) не совпадает с воспроизводимостью методикианализа в целом (Sм). В общем случае Sм > S, так как значение Sм складывается из совокупности погрешностей отбора пробы (Sо. п. ), погрешностей подготовительных операций пробы перед измерениями (Sп. о. ) и погрешности измерения аналитического сигнала: 41

42

Суммирование погрешностей 43

Случайные погрешности гравиметрического метода Массовую долю определяемого компонента рассчитывают по формуле: где М и М 0 — массы тигля с осадком и без него (г); P и P 0 — массы лодочки для взвешивания с навеской и без нее (г). Если пренебречь погрешностью гравиметрического фактора, то выборочные дисперсии случайных погрешностей sm 2=sр2=2 sе 2 Дисперсию массовой доли определяемого компонента можно представить как сумму дисперсий некоррелированных переменных m и р: Очевидно, что абсолютная погрешность гравиметрического определения (sa) зависит от значения гравиметрического фактора: чем больше F, тем выше абсолютная погрешность. 44

Однако, на величину относительной погрешность определения гравиметрический фактор влияет только косвенно, так как в выражение для расчета относительной погрешности не входит: 45

F-критерий. Сравнение дисперсий двух выборок В аналитической практике нередко возникает необходимость сравнения двух средних значений. Так бывает, когда одну и ту же пробу анализируют разными методами. В таких случаях также важно установить является ли разница результатов статистически значимой. Проверку нуль-гипотезы о незначимом различии двух дисперсий проводят с помощью F- критерия. Для этого вычисляют отношение где s 12 — большая по значению дисперсия, s 22 — меньшая. Поэтому значение F всегда больше единицы. Если рассчитанное значение F не превышает табличное значение Fтабл для заданной вероятности P=95 % и числе степеней свободы – между дисперсиями не существует значимой разницы. 46
Наиболее надежно ошибку титрования можно определить экспериментально, проводя большое число анализов стандартного образца. Это особенно необходимо при разработке нового метода анализа. Однако такая работа очень трудоемка, поэтому ошибку титрования рассчитывают из условий равновесия для каждой системы. К рассчитанным минимальным ошибкам прибавляют затем другие систематические ошибки капельную, ошибку градуировки, температурную и др. Так как этот расчет основан на применении закона действующих масс к водным растворам, в следующем разделе будут приведены некоторые конкретные примеры. [c.215]
Ошибки методические. Эти ошибки зависят от особенностей применяемого метода анализа, например от не вполне количественного протекания реакции, на которой основано определение, от частичной растворимости осадка, от соосаждения вместе с ним различных посторонних примесей, от частичного разложения или улетучивания осадка при прокаливании, от гигроскопичности прокаленного осадка, от течения наряду с основной реакцией каких-либо побочных реакций, искажающих результаты титриметрических определений, от свойств примененного при титровании индикатора и т. д. Методические ошибки составляют наиболее серьезную причину искажения результатов количественных определений, устранить их трудно. [c.48]
Определение элементного состава нефтей проводится общепринятыми методами анализа органических соединений, в частности углерод и водород — сожжением, по Либиху, или в калориметрической бомбе, азот, — по Дюма, сера, — по Кариусу, а кислород, — по разности, причем на процент его содержания ложатся все ошибки опыта. [c.76]
Погрешность в результатах анализа зависит также от метода последующего определения. При использовании колориметрических методов относительная ошибка обычно составляет 1—5%, Спектрофотометрический метод дает примерно 5%, а флуорометрический —3—8% и в отдельных случаях до 15%. [c.153]
Так как Г > Р Р Ь /2), между 51 и 32 можно предположить различие, которым нельзя пренебречь. Концентрации шести проб имеют больший разброс, чем если бы, как предполагалось, действовала только ошибка метода анализа. Ошибку пробоотбора з» находят в виде компоненты дисперсии из уравнения (8.1) [c.141]
Модификации газового хроматографа краны, устройства для ввода проб, делители потока, ловушки, регуляторы потока, оборудование для переноса веществ в другие приборы, например в масс-спектрометр полное описание материалов или оборудования, специально изготовленных в лаборатории метод получения представленных образцов результаты, полученные другими методами анализа ошибки, которых следует избегать описание способа содержания системы в рабочем состоянии. [c.11]
Распределение ошибок. Суммарная случайная ошибка метода анализа складывается из дисперсий частных ошибок. Желая улучшить точность метода анализа, следует обратить [c.33]
МОСТИ не учесть тех или иных параметров, которые существенно влияют на процесс, то это может привести к серьезным ошибкам при получении конечного расчетного уравнения, что является недостатком метода анализа размерностей. При отсутствии надежных исходных данных, вытекающих из физической сущности процесса, в случае применения данного метода для их выяснения нередко приходится использовать инженерную интуицию. [c.78]
Необходимо отметить, что при большом содержании определяемого элемента весовой или объемный методы анализа дают более точные результаты. Это объясняется отчасти несовершенством оптической аппаратуры (по сравнению с весами), а также недостаточным знанием химических условий реакций образования окрашенных соединений. Однако при малом содержании того или другого компонента колориметрический метод дает более точные результаты. При взвешивании на аналитических весах количеств вещества порядка 1 10 г вероятная ошибка определения составляет 10%, а взвешивание меньших количеств практически невозможно колориметрическое же определение таких количеств (как это было показано на примере марганца) вполне возможно. [c.215]
Для химика очень важно знать, каковы степень и характер этого приближения. Это необходимо знать не только для правильной оценки работы лаборатории. Точность анализа и ошибка определения необходимы для оценки метода анализа, для определения возможности применения нового, еще недостаточно изученного метода или применения известного метода к новым материалам. Наконец, точность необходимо знать нередко и в более простых случаях, а именно — для выбора технических приемов выполнения отдельных аналитических операций. [c.478]
Ошибки метода могут быть учтены или предотвращены при хорошем понимании химических и физико-химических характеристик данного метода анализа. [c.480]
В этом случае абсолютная ошибка почти не превышает чувствительности аналитических весов и хи.мика нельзя обвинять в том, что он плохо взвешивал и поэтому получил относительную ошибку 8%. Тем не менее следует считать, что химик неправильно выбрал метод анализа для определения таких малых количеств железа не следовало применять обычный весовой метод анализа. [c.480]
Примесей. Для решения такой трудной задачи необходимо объединение методов аналитической химии следовых количеств и прецизионной аналитической химии. Результаты анализов одной и той же пробы на содержание следовых количеств веществ, выполненных в разных лабораториях, часто существенно различаются (иногда даже на порядок). Например, в семи лабораториях проводили определение содержания углерода в образце молибдена и получили следующие тщательно проверенные средние значения 5 11 10 16 21 10 и 9 млн . Идеальным условием определения следовых количеств элементов в пробе является их равномерное распределение в ней, как, например, в гомогенной жидкой или газообразной фазе в этом случае ошибка анализа определяется только правильностью и воспроизводимостью метода. Анализ твердых веществ усложняется неравномерностью распределения в них следовых количеств элементов. В этом случае проба может быть неоднородной по чистоте, и, следовательно, не представительной. В целом вероятность неравномерного распределения следовых количеств элементов возрастает с уменьшением их содержания. [c.412]
Абсолютная ошибка наглядно отражает надежность аналитического метода относительная ошибка (поскольку отнесена к измеряемой единице) —эффективность метода анализа. [c.437]
Чувствительность Ь инструментальных методов анализа определяется фактором пересчета показаний прибора (обычно в единицах шкалы) на содержание вещества в гравиметрии — это обратная величина стехиометрического гравиметрического фактора (Ь=1//). Чем меньше /, тем больше чувствительность метода и тем меньше абсолютная ошибка гравиметрического определения количества вещества х. В объемных методах анализа фактору f соответствует эквивалентная концентрация с применяемого титранта. Чтобы ошибка определения была невелика, а чувствительность метода высока, эта величина должна быть как можно меньшей, что способствует получению интенсивного сигнала у. Однако при этом начинает сказываться эффект разбавления, что приводит к систематическим ошибкам определения, поэтому следует выбирать оптимальную величину Сз. [c.457]
Случайные ошибки градуировки и самого анализа входят в общую ошибку метода анализа [c.458]
Преимущества потенциометрического метода титрования. Потенциометрическое титрование при прочих равных условиях имеет ряд преимуществ по сравнению с визуальными титриметрическими методами анализа. Метод потенциометрического титрования более чувствителен, при использовании его исключается субъективная ошибка, возникающая при визуальном нахождении момента завершения химической реакции, т. е. конечной точки титрования. Этот метод дает возможность определять вещества в мутных и сильно окрашенных растворах, дифференцированно (раздельно) титровать компоненты смесн веществ в одной и той же порции раствора и, наконец, автоматизировать процесс титрования, так как измеряемой величиной является электрический параметр. [c.37]
Области применения фотометрии. Фотометрический анализ характеризуется высокой избирательностью и малыми затратами времени на его осуществление. Величина средней квадратичной ошибки фотометрических методов анализа составляет 2—5% (отн.). Благодаря этим преимуществам фотометрические методы очень широко используют. Некоторыми типичными примерами применения этого метода являются количественный анализ смесей (например, изомеров [63]), определение примесей в сплавах или минералах и породах [73] или же решение задач клинического анализа. Далее, фотометрические методы применяются при изучении кинетики реакций или для непрерывного аналитического контроля технологических процессов. Ввиду значительно больших молярных коэффициентов поглощения методы фотометрии в ультрафиолетовой области в общем обладают большей чувствительностью, чем методы инфракрасной спектроскопии [уравнение (2.3.7)]. Поэтому фотометрию в ультрафиолетовой и видимой областях предпочитают использовать при определении следовых количеств веществ [74], при контроле степени чистоты веществ, сочетая при необходимости фотометрические методы с подходящими способами выделения и концентрирования. [c.248]
Метод анализа можно представить в виде цепи передачи информации (см. рис. 1.1, б). В каждом случае источником информации является анализируемый образец — проба в начальном состоянии. Путем предварительных преобразований (растворение, подходящая обработка, включение операций разделения при неудовлетворительной избирательности) упрощают структуру информационного множества, после чего получают сигнал, используемый для аналитических целей. По каналу связи сигнал поступает в приемник (регистрирующее устройство), где он преобразуется в измеряемую величину, например электрическое напряжение. На выходе цепи передачи информации (рис. 1.1,6) получают характеристические сигналы г,, или сигналы / , интенсивность которых зависит от количества вещества. В большинстве инструментальных методов сигналы обоих видов можно получить одновременно. Полученный сигнал 2 незначительно отклоняется от первичного сигнала . Однако сигнал у, являющийся функцией количества вещества, подвержен более сильному воздействию помех.. Во-первых, его изменяет подчиненная некоторому статистическому распределению величина случайной ошибки сгц (шумы). Шумы ограничивают достоверность определяемой интенсивности сигнала одновременно они определяют наименьшее значение интенсивности г/и, которое еще можно обнаружить и измерить. Далее, сигнал у, исходящий из пробы, уширяется (например, интервал перехода индикатора), и его интенсивность уменьшается. В этом случае может измениться даже первоначальная закономерная связь интенсивности с концентрацией определяемого вещества. Наконец, при неудовлетворительной избирательности метода анализа возможно изменение интенсивности вследствие наложения соседних сигналов. [c.12]
При выполнении калибровки относительная ошибка метода анализа увеличивается. Условием для описанного выше типа калибровки является постоянство чувствительности Ь для всех исследуемых проб. В некоторых случаях, например в рентгеновской спектрометрии, это условие не выполняется. Тогда в каждую исследуемую пробу вводят эталонную (стандартную) добавку. Из переведенной в раствор пробы отбирают две равные аликвотные части и к одной из них добавляют известное количество определяемого элемента х , х. Учитывая, что у = Ьх, получим систему уравнений [c.19]
Оценка средней квадратичной ошибки. Для характеристики случайной ошибки метода анализа используют величину средней квадратичной ошибки в. Обычный прием аналитической химии заключается в исследовании серии проб с различным содержанием определяемого вещества при некотором ограниченном числе параллельных определений. При наличии т проб и некоторого числа Лд параллельных определений для средней квадратичной ошибки получаем следующую формулу [c.23]
В общем случае оптимальная область применения метода анализа характеризуется наименьшими абсолютной и относительной средними квадратичными ошибками (разд. 2.2). [c.25]
При выполнении этого метода проверки особенно четко вырисовывается малая убедительность средней квадратичной ошибки с небольшим числом степеней свободы. Расхождение двух средних квадратичных ошибок с числом степеней свободы Д = /2 = 3 учитывают (0,95 < Р< 0,99) только в том случае, если одна средняя квадратичная ошибка в три раза больше другой. Даже при числе степеней свободы /1 = /2 = 12 для аналитических выводов требуется, чтобы соотношение s /s2 1/3. Таким образом, о случайных ошибках методов анализа с достаточной строгостью можно судить, только располагая достаточным числом результатов. Доказуемость расхождения особенно определяется величиной Д. Поэтому для меньшей из обеих средних квадратичных ошибок нужно предусматривать возможно большее число степеней свободы. [c.31]
Разброс среднего значения x определяется случайными ошибками обеих стадий метода анализа. По этой причине частную ошибку операции разделения можно найти как разность. Имеем [c.34]
Навески е = 2 2 = 2е , требующиеся для такого способа обнаружения ошибок, проще всего заменить отбором аликвотных частей раствора. Выполняя большее число определений, можно обнаружить ошибки обоих видов в разных пробах. Это позволяет избежать лишней работы. Описанные способы особенно удобны для использования в методах анализа, построенных на принципе навеска — растворение — измерение, отличающихся небольшой случайной ошибкой. [c.37]
Это манометрический метод анализа [46]. Давление определяют манометром. Ошибка этого метода меньше, чем в объемном газовом анализе. [c.85]
Методы анализа, основанные на отражении Р-частиц, в общем менее точны, чем методы, основанные на их поглощении. Однако принцип отражения Р-частиц веществом положен в основу измерения толщины металлических покрытий. При этом можно, например, определить толщину слоя цинка, нанесенного на железо, хрома, нанесенного на алюминий, и т. д. Методы, основанные на отражении Р-частиц, применяют в металлургии для анализа бинарных систем. Ошибка анализа при этом тем меньше, чем больше различаются заряды ядер компонентов смеси. Метод применим для непрерывного контроля содержания ниобия в хроме или вольфрама в железе. Средняя квадратичная ошибка определения содержания (3% и более) ниобия в хроме составляет 2%. На рис. 6.8 приведена схема установки для проведения определений по методу отражения Р Частиц. [c.320]
При определении следовых количеств примесей особое значение приобретают вопросы надежности анализа. Как известно, в кинетических методах анализа ошибки определений, как правило, бывают выше, чем в методах, основанных на реакциях определяемого иона с реактивом в стехиометрическом соотношении благодаря сильному влиянию температуры, ионной силы, состояния поверхности сосудов и других факторов на скорость реакции. Поэтому аналитик, использующий кинетические методы, должен обращать особое внимание на статистическую обработку результатов анализа [17, 18]. Статистические методы могут характеризовать лишь йоспроизводи-мость анализа и не дают ответа на вопрос о правильности анализа. Правильность анализа может быть установлена на основе четкого знания химизма всех процессов анализа и с учетом данных независимого метода анализа [19]. С помощью статистических методов можно оценить чувствительность реакции. В основу такой оценки может быть положена величина среднеквадратичной ошибки измерения [20]. [c.32]
Все методы анализа ароматических углеводородов можно разделить по суш,еству на физические и химические, а принципиально— на прямые и косвенные, т. е. можпо определять количество бензина н по разности — исследуемый углеводород (косвенный метод) и количество самого углеводорода (прямой метод). В обоих случаях все ошибки анализа ложатся на определяемое вещество поэтому рациональнее прямой метод, так как тогда уменьшается ошибка. I соясалению, все методы достаточно грубы и не дают, за редкими исключениями, хоть сколько-нибудь точных цифр. Эти методы раз-б1фаются далее, после обзора физических и химических свойств отдельных ароматических углеводородов легкого масла. [c.404]
В углях с выходом летучих веществ ниже 35% наблюдается хорошее соответствие (см. рис. 2) степени метаморфизма, определенной этим способом, степени метаморфизма, установленной на основании других методов анализов, например по содержанию углерода, водорода, выходу летучих веществ и др. Для образцов углей с выходом летучих веществ более 30% замеры, не представляющие собой средние из многих данных, могут привести к существенной ошибке в определении степени их метаморфизма. Так, например, у обнаруженных в южном полушарии каменных углей с выходом летучих веществ 28—30% индекс вспучивания близок к нулю, что необычно и наводит на мысль о предварительной окисленности исследуемых образцов. В действительности же это оказались такие угли, витринит которых подобен по своей отражательной способности пламенным, жирным лотарингским углям с выходом летучих веществ около 35%, обладающим слабой спекаемостью. Общая величина выхода летучих веществ 28—30% в углях получается в результате примешивания к вит-риниту (выход летучих веществ 35%) значительного количества инер-тинита (выход летучих веществ приблизительно 20%). Ухудшение спекаемости таких углей наступает из-за высокого содержания в них инертинита, который вообще не превращается в пластическое состояние, и очень малого при этом содержания спекающегося экзинита. [c.18]
Реакционная способность прокаленных коксов определялась в атмосфере воздуха по модернизированной методике Красюкова А.Ф. Определение проводилось на коксах с размером частиц 0,5-1,0 мм. Метод анализа в определенной степени моделирует условия окисления анодов при их работе. Важным достоинством метода является интегральность оценки, ошибки определений не превышали 5 %. [c.84]
Здесь уместно отметить, что утверждение Квптковского и Петрова [124] о полной непригодности методов структурно-группового анализа для исследования нефтяных высокомолекулярных углеводородов, содержащих ароматические структуры, слишком категорично и недостаточно мотивировано. Их расчеты проведены на примерах сравнительно простых двойных и тройных смесей из синтетических углеродов, не вполне моделирующих сложные многокомпонентные -системы, какими являются даже узкие фракции высокомолекулярных углеводородов нефти. Известно, что чем сильнее отклоняется явление по своим характеристикам от средних значений, тем реже оно повторяется. Во всяком случае, пока нет более точных методов определения строения сложных гибридных структур высокомолекулярных углеводородов нефти, структурно-групповыми методами анализа следует пользоваться, даже если ошибки определений будут составлять 15—20%. Правда, такие отклонения уже легко будет обнаружить по данным элементарного анализа и константам ( , п и др.). Методы структурно-группового анализа дают полуколичественную характеристику, в общем правильно отражающую сочетание структурных элементов в усредненной молекуле многокомпонентных смесей. На примерах индивидуальных синтетических соединений и их смесей надо вести дальнейшие исследования по выяснению закономерностей, связывающих свойства со строением молекулы. [c.252]
Тел1пература размягчения- Другим эмпирическим методом анализа битумных материалов, широко используемым при их производстве, является определение температуры размягчения по кольцу и шару (КиШ). По этому методу определяют температуру, при которой битум приобретает такую консистенцию, что он может течь определенное расстояние при заданной скорости нагрева. По данным [481, консистенция ряда каменноугольных пеков при температуре размягчения по КиШ колеблется в пределах 8,9-10 —27,4-10 П. Как указывалось выше, битумы при температуре размягчения имеют более высокую вязкость. Необходимо учесть, что допустимая ошибка в определении температуры размягчения 0,5 °С может привести к отклонению значений вязкости на 14%. Скорость сдвига в ходе определения также различна, особенно вначале, когда битум имеет аномальные реологические свойства. [c.134]
Наряду с различными случайными ошибками в работе нередки систематические ошибки. Систематические ошибки могут происходить по различным причинам их можно разделить на три группы 1) ошибки метода, 2) ошибки приборов и реактивов, 3) оишбки исполнителя анализа. [c.479]
Для установления правильности выполнения данного метода анализа можно определить в одном или нескольких контрольных обря.зцах содержание свинца весовым методом, осаждая сернокислый свинец. Если результаты удовлетворительно совпадают, можно считать с достаточной надежностью, что анализ хроматным методом выполняется хорошо. Крайне мало вероятно, чтобы дна совершенно разных метода дали результаты с совершенно одинаковой ошибкой. [c.483]
Факторы OTi и /П2 в уравнении (20) имеют довольно значительную величину, так что ошибки взвешивания OTi и тг возрастают до больших значений и возникает относительно большая ошибка определения тквг- Поэтому косвенные методы анализа отличаются значительно меньшей точностью, чем прямые, и по возможности их следует избегать. [c.108]
В некоторых методах анализа относительная ошибка Оу1у постоянна во всем интервале измерений. Поэтому эти методы особенно эффективны для исследования небольших количеств пробы, например в анализе следовых количеств вешеств. [c.452]
Как было показано в разд. 44.3, при измерении какого-либо параметра различными аналитическими методами происходит небольшой,, но неизбежный случайный разброс результатов. При оценке результатов измерений, например, методами, приведенными в разд. 44.7, этот разброс тем или иным образом сказывается на результатах анализа. Из данных по случайному разбросу результатов анализа эталонной пробы можно определить случайный разброс, или точность, метода анализа, а из отклонения среднего значения от известного теоретического найти лравильность, или систематическую ошибку, метода. Если аналогично оценить операции отбора пробы и подготовки ее к анализу, то можно сделать соответствующие выводы о методе анализа в целом. Эти выводы имеют особенно важное значение для аналитической практики, но на их получение тратится много времени, поскольку необходимо осуществить весь ход анализа. Часто соответствующие рекомендации касаются только принципа проведения анализа или в лучшем случае собственно метода [c.461]
По точности многие физико-химические методы анализа уступают классическим, и особенно весовому методу. Нередко, когда весовым н объемным методами достигается точность, определяемая сотыми и десятыми долями процента, при выполнении анализа физико-химичес1шми методами ошибки определении составляют 5—10%, а иногда и значительно больше. [c.21]
В некоторых методах анализа, например в спектрографии и других, относительная ошибка Оу1у постоянна во всем интервале измерений от у до уа. Обычно интенсивность сигнала у определяют по линейной шкале. Тогда нижний предел интервала измерений определтся ошибкой отсчета показаний по шкале Оу и i/u = Зоу. [c.18]
Ценные указания о возможности использования метода анализа иногда дает зависимость средней квадратичной ошибки 0у от измеряемой величины у. Наибольшей эффективностью методы анализа обладают в том случае, если абсолютная и относительная средние квадратичные ошибки малы.Поэтому методы, отличающ,иеся постоянной абсолютной ошибкой Оу = onst, предпочитают использовать при определении больших содержаний искомых веществ, а методы с постоянной относительной ошибкой Oyly = onst — при определении малых количеств. Подобно тому как Оу является мерилом случайной ошибки, t/u играет важную роль как критерий возможности обнаружения сигнала, В общем случае, если относительную ошибку предела обнаружения принять равной Оу/у = 0,33, то, выполняя Пд параллельных определений, минимально обнаруживаемую интенсивность сигнала можно уменьшить в раз. С учетом уравнения (2.2.3) получим [c.18]
Общая ошибка метода анализа определяется случайными ошибками калиб-бровки (Ао У/Ие) и анализа (Лсу/лд), Кроме того, на нее оказывает влияние как чувствительность метода Ь, так и относительная величина ее сред1 й квадратичной ошибки (а ,/ЬУ. Далее, вследствие наличия члена (г/д — у) величина становится зависимой от концентрации. Точный результат возможен, если величина Оу мала, а величина Ь велика. Кроме того, измеряемая величина уд должна находиться в середине интервала измерений. Если выполняется условие 1/тн < 1/лд, то ошибка еще более уменьшается. К этому легко можно приблизиться, располагая десятью ( ) эталонными пробами, т. е. при т = Ю. При условии 1/ше С 1/пд относительная ошибка определяется следующим выражением [c.19]
Нередко средняя квадратичная ошибка зависит от величины результата определения и от состава пробы. Поэтому величину найденной в конкретном случае средней квадратичной ошибки нельзя безоговорочно обобщать. Особенно это справедливо в тех случаях, когда метод анализа прошел испы- [c.24]
МИ методами. В отсутствие подходящего изотопа-осадителя, анализ проводят косвенным методом. Ишибаши и Киши предложили метод определения Са и Ы, основанный на осаждении их в виде фосфатов действием фосфорной кислоты с последующим растворением осадка и определением выделившейся кислоты при помощи радиоактивного изотопа свинца. (В то время еще не был известен радиоактивный изотоп Аналогичные определения можно проводить, используя принцип соосаждения радиоактивного изотопа с определенным веществом. При этом должны быть известны коэффициенты распределения веществ все процессы осаждения следует проводить в одинаковых условиях. Эренберг применил указанный метод для определения щавелевой кислоты, осаждая ее действием раствора СаС12, содержащего ТЬВ [171. Метод радиоактивных изотопов позволяет с высокой точностью проводить определение высокомолекулярных веществ (сахар, крахмал) и продуктов полимеризации по их концевым группам другие методы анализа указанных соединений дают довольно большую ошибку. При проведении анализа методом осаждения с применением радиоактивных индикаторов массу осадка можно определить, даже если реакция осаждения протекает нестехиометрически или в результате реакции образуется довольно растворимое соединение, так как распределение радиоактивного изотопа между двумя фазами постоянно. [c.316]

