Контрольное правило вестгарда, позволяющее выявить случайную ошибку, наблюдается, когда
1) десять последовательных результатов находятся на одной стороне от средней
2) два последовательных контрольных результата с любой стороны от средней превышают контрольные пределы хср±2σ
3) один контрольный результат превышает контрольные пределы xср+3σ (+)
4) четыре последовательных контрольных результата находятся на одной стороне от средней и превышают контрольные пределы хср+1σ
Поделитесь с коллегами ссылкой на наш сайт
Правила Вестгарда
редактировать
Правила Вестгарда представляют собой набор статистических шаблонов, появление каждого из которых маловероятно из-за случайной изменчивости, что вызывает подозрение в неправильной точности или прецизионности измерительной системы. Они используются для лабораторного контроля качества в «сериях», состоящих из измерений нескольких образцов. Они представляют собой набор модифицированных правил Western Electric, разработанных и представленных в его книгах и семинарах по контролю качества. Правила следующие:
| Правило | Критерии | Подозреваемые | Пример |
|---|---|---|---|
| 12s | Одно измерение превышает 2 стандартных отклонения либо выше, либо ниже среднего. эталонного диапазона. | Погрешность и / или неточность | 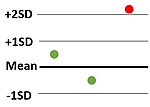 |
| 13s | Одно измерение превышает 3 стандартных отклонения либо выше, либо ниже среднего значения эталонного диапазона. | Неточность и / или неточность | 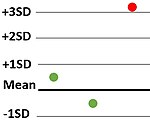 |
| 22s | 2 последовательных измерения превышают 2 стандартных отклонения от эталонного диапазона и находятся на той же стороне от среднего. | Неточность. |  |
| R4s | Два измерения в одном прогоне имеют разницу в 4 стандартных отклонения (например, одно превышает 2 стандартных отклонения выше среднего, а другое превышает 2 стандартных отклонения ниже среднего). | Неточность. | 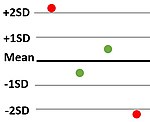 |
| 41s | 4 последовательных измерения превышают 1 стандартное отклонение на той же стороне от среднего. | Неточность. | 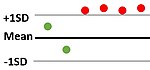 |
| 10x | 10 последовательных измерений находятся по одну сторону от среднего. | Неточность. | 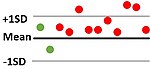 |
Рекомендуемые последствия при возникновении любого из вышеперечисленных шаблонов — отказ от выполнения, за исключением правила 1 2s (вверху в таблице), которое служит предупреждением и рекомендацией к тщательной проверке данные.
См. также
Ссылки
Внешние ссылки
Последняя правка сделана 2021-06-20 12:54:13
Содержание доступно по лицензии CC BY-SA 3.0 (если не указано иное).
From Wikipedia, the free encyclopedia
The Westgard rules are a set of statistical patterns, each being unlikely to occur by random variability, thereby raising a suspicion of faulty accuracy or precision of the measurement system. They are used for laboratory quality control, in «runs» consisting of measurements of multiple samples. They are a set of modified Western Electric rules, developed by James Westgard and provided in his books and seminars on quality control.[1] They are plotted on Levey–Jennings charts, wherein the X-axis shows each individual sample, and the Y-axis shows how much each one differs from the mean in terms of standard deviation (SD). The rules are:[2]
| Rule | Criteria | Suspected | Example |
|---|---|---|---|
| 12s | One measurement exceeds 2 standard deviations either above or below the mean of the reference range. | Inaccuracy and/or imprecision | 
|
| 13s | One measurement exceeds 3 standard deviations either above or below the mean of the reference range. | Inaccuracy and/or imprecision | 
|
| 22s | 2 consecutive measurements exceed 2 standard deviations of the reference range, and on the same side of the mean. | Inaccuracy and/or imprecision | 
|
| R4s | Two measurements in the same run have a 4 standard deviation difference (such as one exceeding 2 standard deviations above the mean, and another exceeding 2 standard deviations below the mean). | Imprecision. | 
|
| 41s | 4 consecutive measurements exceed 1 standard deviation on the same side of the mean. | Inaccuracy. | 
|
| 10x | 10 consecutive measurements are on the same side of the mean. | Inaccuracy. | 
|
The recommended consequences when any of the above patterns occur is to reject the run, except for the rule of 12s (top in table), which serves as a warning and a recommendation of careful inspection of the data.[2]
See also[edit]
- Western Electric rules
- Nelson rules
References[edit]
- ^ Ofer Harel; Enrique F. Schisterman; Albert Vexler & Marcus D. Ruopp (July 2008). «Monitoring Quality Control: Can We Get Better Data?». Epidemiology. 19 (4): 621. doi:10.1097/ede.0b013e318176bfb2. PMC 2625303. PMID 18496467.
- ^ a b Heidi Hanes. «Westgard Rules — Guidelines». SMILE, Johns Hopkins University. Review date: 1 April 2020
External links[edit]
- Official website
Подборка по базе: Методические материалы по повышению качества управле�….pdf, МУ ЛР Экспертиза качества риса_2 _2022.docx, практическая работа №3 оценка качества образования.docx, МДК01.01 Подготовка рабочего места, лабораторных условий, средст, Шалабаев Алибек МП-21 Волевые качества и пути их развития.pptx, + Тема 2.4. Практическая работа 8 Оценка качества (1).docx, Комплектование,подготовка к работе пахотного агрегара.контроль к, Современные способы контроля качества термической обработки.doc, Методические улахания по выполнению лабораторных работ Механика., ВЫПУСКНАЯ-Лаборатория-МЕНЕДЖМЕНТ КАЧЕСТВА.pdf

Билет 2
 К
К онтроль качества клинических лабораторных исследований. Внутрилабораторный контроль качества клинических лабораторных исследований. Построение контрольных карт. Критерии оценки контрольной карты. Правила Вестгарда.
онтроль качества клинических лабораторных исследований. Внутрилабораторный контроль качества клинических лабораторных исследований. Построение контрольных карт. Критерии оценки контрольной карты. Правила Вестгарда.



Контроль качества в медицинской лаборатории – это статистический процесс, используемый для наблюдения и оценки аналитического процесса производства результатов исследования проб пациентов.
Построение контрольных карт
Контрольные карты строятся для каждого лабораторного показателя и каждого контрольного материала
Из 20 результатов, полученных в установочной серии, рассчитывают среднее значение (Xср.) и S (стандартное отклонение) и устанавливают контрольные пределы: Xср. ± 1S, Xср. ± 2S и Xср. ± 3S
Если в ряду результатов есть значение, выходящее за пределы 3S, то это значение отбрасывается и проводится еще одна аналитическая серия.
Контрольные правила Вестгарда
Задачи: минимизировать ложную выбраковку данных и обнаружить максимум ошибок Правила:
1(2s) Это предупредительное правило, которое считается нарушенным, если результат одного контрольного измерения вышел за пределы ±2S.
1(3s) Это правило позволяет обнаружить недопустимую случайную ошибку или начало большой систематической ошибки (сдвиг). Это правило нарушает любой контрольный результат, вышедший за пределы ±3S.
2(2s) Это правило выявляет только систематическую ошибку. Оно считается нарушенным, когда два последовательных контрольных результата оказываются по одну сторону от среднего арифметического значения за пределом 2S.
R(4s) Это правило позволяет выявить только случайную ошибку и применяется только в пределах одной аналитической серии. Если расстояние между результатами измерения контрольного материала в данной аналитической серии составляет более 4S, правило считается нарушенным из-за наличия случайной ошибки.
4(1s) Правило считается нарушенным, когда четыре последовательных результата контрольных измерений находятся по одну сторону от среднего значения за пределом 1S.
10(x) Это правило считается нарушенными, 10 точек лежат по одну сторону от среднего арифметического значения независимо от контрольных пределов, в которых они находятся.
Если присутствует хотя бы один из вышеперечисленных контрольных признаков, аналитическая серия бракуется. – найти источник ошибки, – устранить причину, – переделывать всю серию – и контрольные материалы и пробы пациентов. Если ни один из признаков Вестгарда не определяется, серия принимается, и результаты пациентов сообщаются лечащим врачам.
Аналитическая серия — серия измерений, выполняемых в один день, без изменения настроек и калибровки аналитической системы.
Погрешность результата измерения (систематическая, случайная) — отклонение результата измерения от истинного значения измеряемой величины.
Точность результата измерения — отражает близость к нулю погрешности результата измерения.
Правильность измерения — отражает близость к нулю систематической погрешности.
Воспроизводимость — близость результатов измерения одной и той же величины, полученных в разных местах, разными средствами, разными операторами, в разное время, но приведенных к одним и тем же условиям.
Сходимость — близость результатов измерения одной и той же величины измерений в одинаковых условиях в пределах одной аналитической серии.
2.Биохимия витаминов. Общее понятие о витаминах. Классификация витаминов. Метаболизм витаминов. Витамины и провитамины. Нарушения обмена витаминов. Эффекты витаминов на обмен веществ, симптомы дефицита.
Витамины — низкомолекулярные органические соединения различной химической природы и различного строения, синтезируемые главным образом растениями, частично — микроорганизмами. Для человека витамины — незаменимые пищевые факторы.
Недостаток поступления витаминов с пищей, нарушение их всасывания или нарушение их использования организмом приводит к развитию патологических состояний, называемых гиповитаминозами.
Основные причины гиповитаминозов
• Недостаток витаминов в пище;
• Нарушение всасывания в ЖКТ;
• Врождённые дефекты ферментов, участвующих в превращениях витаминов;
• Действие структурных аналогов витаминов (антивитамины).
Потребность человека в витаминах зависит от пола, возраста, физиологического состояния и интенсивности труда. Существенное влияние на потребность человека в витаминах оказывают характер пищи (преобладание углеводов или белков в диете, количество и качество жиров), а также климатические условия.
Классификация витаминов
По химическому строению и физико-химическим свойствам (в частности, по растворимости) витамины делят на 2 группы.
А. Водорастворимые
Витамин В1 (тиамин); Витамин В2 (рибофлавин); Витамин РР (никотиновая кислота, никотинамид, витамин В3); Пантотеновая кислота (витамин В5); Витамин В6 (пиридоксин); Биотин (витамин Н); Фолиевая кислота (витамин Вс, В9); Витамин В12 (кобаламин); Витамин С (аскорбиновая кислота); Витамин Р (биофлавоноиды).
Б. Жирорастворимые
Витамин А (ретинол); Витамин D (холекальциферол); Витамин Е (токоферол); Витамин К (филлохинон).
Водорастворимые витамины при их избыточном поступлении в организм, будучи хорошо растворимыми в воде, быстро выводятся из организма.
Жирорастворимые витамины хорошо растворимы в жирах и легко накапливаются в организме при их избыточном поступлении с пищей. Их накопление в организме может вызвать расстройство обмена веществ, называемое гипервитаминозом, и даже гибель организма.
А. Водорастворимые витамины
1. Витамин В1 (тиамин). Структура витамина включает пиримидиновое и тиазоловое кольца, соединённые метановым мостиком.
Источники. Витамин В1 — первый витамин, выделенный в кристаллическом виде К. Функом в 1912 г. Он широко распространён в продуктах растительного происхождения (оболочка семян хлебных злаков и риса, горох, фасоль, соя и др.). В организмах животных витамин В, содержится преимущественно в виде дифосфорного эфира тиамина (ТДФ); он образуется в печени, почках, мозге, сердечной мышце путём фосфорилирования тиамина при участии тиаминкиназы и АТФ.
Суточная потребность взрослого человека в среднем составляет 2-3 мг витамина В1. Но потребность в нём в очень большой степени зависит от состава и общей калорийности пищи, интенсивности обмена веществ и интенсивности работы. Преобладание углеводов в пище повышает потребность организма в витамине; жиры, наоборот, резко уменьшают эту потребность.
Биологическая роль витамина В1 определяется тем, что в виде ТДФ он входит в состав как минимум трёх ферментов и ферментных комплексов: в составе пируват- и α- кетоглутаратдегидрогеназных комплексов он участвует в окислительном декарбокси- лировании пирувата и α-кетоглутарата; в составе транскетолазы ТДФ участвует в пентозофосфатном пути превращения углеводов.
Основной, наиболее характерный и специфический признак недостаточности витамина В1 — полиневрит, в основе которого лежат дегенеративные изменения нервов. Вначале развивается болезненность вдоль нервных стволов, затем — потеря кожной чувствительности и наступает паралич (бери-бери). Второй важнейший признак заболевания — нарушение сердечной деятельности, что выражается в нарушении сердечного ритма, увеличении размеров сердца и в появлении болей в области сердца. К характерным признакам заболевания, связанного с недостаточностью витамина В1, относят также нарушения секреторной и моторной функций ЖКТ; наблюдают снижение кислотности желудочного сока, потерю аппетита, атонию кишечника.
2. Витамин В2 (рибофлавин). В основе структуры витамина В2 лежит структура изоаллоксазина, соединённого со спиртом рибитолом.
Рибофлавин представляет собой кристаллы жёлтого цвета (от лат. flavos — жёлтый), слабо растворимые в воде.
Главные источники витамина В2 — печень, почки, яйца, молоко, дрожжи. Витамин содержится также в шпинате, пшенице, ржи. Частично человек получает витамин В2 как продукт жизнедеятельности кишечной микрофлоры.
Суточная потребность в витамине В2 взрослого человека составляет 1,8 — 2,6 мг.
Биологические функции. В слизистой оболочке кишечника после всасывания витамина происходит образование коферментов FMN и FAD по схеме:
Коферменты FAD и FMN входят в состав флавиновых ферментов, принимающих участие в окислительно-восстановительных реакциях (см. разделы 2, 6, 9, 10).
Клинические проявления недостаточности рибофлавина выражаются в остановке роста у молодых организмов. Часто развиваются воспалительные процессы на слизистой оболочке ротовой полости, появляются длительно незаживающие трещины в углах рта, дерматит носогубной складки. Типично воспаление глаз: конъюнктивиты, васкуляризация роговицы, катаракта. Кроме того, при авитаминозе В2 развиваются общая мышечная слабость и слабость сердечной мышцы.
3. Витамин РР (никотиновая кислота, никотинамид, витамин B3)
Источники. Витамин РР широко распространён в растительных продуктах, высоко его содержание в рисовых и пшеничных отрубях, дрожжах, много витамина в печени и почках крупного рогатого скота и свиней. Витамин РР может образовываться из триптофана (из 60 молекул триптофана может образоваться 1 молекула никотинамида), что снижает потребность в витамине РР при увеличении количества триптофана в пище.
Суточная потребность в этом витамине составляет для взрослых 15 — 25 мг, для детей — 15 мг.
Биологические функции. Никотиновая кислота в организме входит в состав NAD и NADP, выполняющих функции коферментов различных дегидрогеназ (см. раздел 2). Синтез NAD в организме протекает в 2 этапа:
NADP образуется из NAD путём фосфорилирования под действием цитоплазматической NAD-киназы.
NAD+ + АТФ —> NADP+ + АДФ
Недостаточность витамина РР приводит к заболеванию «пеллагра», для которого характерны 3 основных признака: дерматит, диарея, деменция («три Д»). Пеллагра проявляется в виде симметричного дерматита на участках кожи, доступных действию солнечных лучей, расстройств ЖКТ (диарея) и воспалительных поражений слизистых оболочек рта и языка. В далеко зашедших случаях пеллагры наблюдают расстройства ЦНС (деменция): потеря памяти, галлюцинации и бред.
4. Пантотеновая кислота (витамин В5)
Пантотеновая кислота состоит из остатков D- 2,4-дигидрокси-3,3-диметилмасляной кислоты и β-аланина, соединённых между собой амидной связью:
Пантотеновая кислота — белый мелкокристаллический порошок, хорошо растворимый в воде. Она синтезируется растениями и микроорганизмами, содержится во многих продуктах животного и растительного происхождения (яйцо, печень, мясо, рыба, молоко, дрожжи, картофель, морковь, пшеница, яблоки). В кишечнике человека пантотеновая кислота в небольших количествах продуцируется кишечной палочкой. Пантотеновая кислота — универсальный витамин, в ней или её производных нуждаются человек, животные, растения и микроорганизмы.
Суточная потребность человека в пантотеновой кислоте составляет 10 — 12 мг.
Биологические функции. Пантотеновая кислота используется в клетках для синтеза коферментов: 4-фосфопантотеина и КоА (рис. 3-1). 4-фосфопантотеин — кофермент пальмитоилсинтазы. КоА участвует в переносе ацильных радикалов в реакциях общего пути катаболизма (см. раздел 6), активации жирных кислот, синтеза холестерина и кетоновых тел (см. раздел 8), синтеза ацетилглюкозаминов (см. раздел 15), обезвреживания чужеродных веществ в печени (см. раздел 12).
Клинические проявления недостаточности витамина. У человека и животных развиваются дерматиты, дистрофические изменения желёз внутренней секреции (например, надпочечников), нарушение деятельности нервной системы (невриты, параличи), дистрофические изменения в сердце, почках, депигментация и выпадение волос и шерсти у животных, потеря аппетита, истощение. Низкий уровень пантотената в крови у людей часто сочетается с другими гиповитаминозами (В1, В2) и проявляется как комбинированная форма гиповитаминоза.
5. Витамин В6 (пиридоксин, пиридоксаль, пиридоксамин)
В основе структуры витамина В6 лежит пиридиновое кольцо. Известны 3 формы витамина В6, отличающиеся строением замещающей группы у атома углерода в п-положении к атому азота. Все они характеризуются одинаковой биологической активностью.
Все 3 формы витамина — бесцветные кристаллы, хорошо растворимые в воде.
Источники витамина В6 для человека — такие продукты питания, как яйца, печень, молоко, зёленый перец, морковь, пшеница, дрожжи. Некоторое количество витамина синтезируется кишечной флорой.
Суточная потребность составляет 2-3 мг.
Биологические функции. Все формы витамина В6 используются в организме для синтеза коферментов: пиридоксальфосфата и пиридоксамин- фосфата. Коферменты образуются путём фосфорилирования по гидроксиметильной группе в пятом положении пиримидинового кольца при участии фермента пиридоксалькиназы и АТФ как источника фосфата.
Пиридоксалевые ферменты играют ключевую роль в обмене аминокислот: катализируют реакции трансаминирования и декарбоксилирования аминокислот, участвуют в специфических реакциях метаболизма отдельных аминокислот: серина, треонина, триптофана, серосодержащих аминокислот, а также в синтезе гема (см. разделы 9, 12).
Клинические проявления недостаточности витамина. Авитаминоз В6 у детей проявляется повышенной возбудимостью ЦНС, периодическими судорогами, что связано, возможно, с недостаточным образованием тормозного медиатора ГАМК (см. раздел 9), специфическими дерматитами. У взрослых признаки гиповитаминоза В6 наблюдают при длительном лечении туберкулёза изониазидом (антагонист витамина В6). При этом возникают поражения нервной системы (полиневриты), дерматиты.
6. Биотин (витамин Н)
В основе строения биотина лежит тиофеновое кольцо, к которому присоединена молекула мочевины, а боковая цепь представлена валерьяновой кислотой.
Источники. Биотин содержится почти во всех продуктах животного и растительного происхождения. Наиболее богаты этим витамином печень, почки, молоко, желток яйца. В обычных условиях человек получает достаточное количество биотина в результате бактериального синтеза в кишечнике.
Суточная потребность биотина у человека не превышает 10 мкг.
Биологическая роль. Биотин выполняет коферментную функцию в составе карбоксилаз: он участвует в образовании активной формы СO2.
В организме биотин используется в образовании малонил-КоА из ацетил-КоА (см. раздел 8), в синтезе пуринового кольца (см. раздел 10), а также в реакции карбоксилирования пирувата с образованием оксалоацетата (см. раздел 6).
Клинические проявления недостаточности биотина у человека изучены мало, поскольку бактерии кишечника обладают способностью синтезировать этот витамин в необходимых количествах. Поэтому картина авитаминоза проявляется при дисбактериозах кишечника, например, после приёма больших количеств антибиотиков или сульфамидных препаратов, вызывающих гибель микрофлоры кишечника, либо после введения в рацион большого количества сырого яичного белка. В яичном белке содержится гликопротеин авидин, который соединяется с биотином и препятствует всасыванию последнего из кишечника. Авидин (молекулярная масса 70 000 кД) состоит из четырёх идентичных субъединиц, содержащих по 128 аминокислот; каждая субъединица связывает по одной молекуле биотина.
При недостаточности биотина у человека развиваются явления специфического дерматита, характеризующегося покраснением и шелушением кожи, а также обильной секрецией сальных желёз (себорея). При авитаминозе витамина Н наблюдают также выпадение волос и шерсти у животных, поражение ногтей, часто отмечают боли в мышцах, усталость, сонливость и депрессию.
7. Фолиевая кислота (витамин Вс, витамин B9)
Фолиевая кислота состоит из трёх структурных единиц: остатка птеридина (I), парааминобензойной (II) и глутаминовой (III) кислот.
Витамин, полученный из разных источников, может содержать 3 — 6 остатков глутаминовой кислоты. Фолиевая кислота была выделена в 1941 г. из зелёных листьев растений, в связи с чем и получила своё название (от лат. folium — лист).
Источники. Значительное количество этого витамина содержится в дрожжах, а также в печени, почках, мясе и других продуктах животного происхождения.
Суточная потребность в фолиевой кислоте колеблется от 50 до 200 мкг; однако вследствие плохой всасываемости этого витамина рекомендуемая суточная доза — 400 мкг.
Биологическая роль фолиевой кислоты определяется тем, что она служит субстратом для синтеза коферментов, участвующих в реакциях переноса одноуглеродных радикалов различной степени окисленности: метильных, оксиметильных, формильных и других. Эти коферменты участвуют в синтезе различных веществ: пуриновых нуклеотидов, превращении dУМФ в dTМФ, в обмене глицина и серина (см. разделы 9, 10).
Наиболее характерные признаки авитаминоза фолиевой кислоты — нарушение кроветворения и связанные с этим различные формы малокровия (макроцитарная анемия), лейкопения и задержка роста. При гиповитаминозе фолиевой кислоты наблюдают нарушения регенерации эпителия, особенно в ЖКТ, обусловленные недостатком пуринов и пиримидинов для синтеза ДНК в постоянно делящихся клетках слизистой оболочки.
Авитаминоз фолиевой кислоты редко проявляется у человека и животных, так как этот витамин в достаточной степени синтезируется кишечной микрофлорой. Однако использование сульфаниламидных препаратов для лечения ряда заболеваний может вызвать развитие авитаминозов. Эти препараты — структурные аналоги парааминобензойной кислоты, ингибирующие синтез фолиевой кислоты у микроорганизмов (см. раздел 2). Некоторые производные птеридина (аминоптерин и метотрексат) тормозят рост почти всех организмов, нуждающихся в фолиевой кислоте. Эти препараты находят применение в лечебной практике для подавления опухолевого роста у онкологических больных.
8. Витамин В12 (кобаламин)
Витамин В12 был выделен из печени в кристаллическом виде в 1948 г. В 1955 г. Дороти Ходжкен с помощью рентгеноструктурного анализа расшифровала структуру этого витамина. За эту работу в 1964 г. ей была присуждена Нобелевская премия. Витамин В12 — единственный витамин, содержащий в своём составе металл кобальт (рис. 3-2).
Источники. Ни животные, ни растения не способны синтезировать витамин В12. Это единственный витамин, синтезируемый почти исключительно микроорганизмами: бактериями, актиномицетами и сине-зелёными водорослями. Из животных тканей наиболее богаты витамином В12 печень и почки. Недостаточность витамина в тканях животных связана с нарушением всасывания кобаламина из-за нарушения синтеза внутреннего фактора Касла, в соединении с которым он и всасывается. Фактор Касла синтезируется обкладочными клетками желудка. Это — гликопротеин с молекулярной массой 93 000 Д. Он соединяется с витамином В12 при участии ионов кальция. Гипоавитаминоз В12обычно сочетается с понижением кислотности желудочного сока, что может быть результатом повреждения слизистой оболочки желудка. Гипоавитаминоз В12 может развиться также после тотального удаления желудка при хирургических операциях.
Суточная потребность в витамине В12 крайне мала и составляет всего 1 — 2 мкг.
Витамин В12 служит источником образования двух коферментов: метилкобаламина в цитоплазме и дезоксиаденозилкобаламина в митохондриях (рис. 3-2).
• Метил-В12 — кофермент, участвующий в образовании метионина из гомоцистеина. Кроме того, метил-В12 принимает участие в превращениях производных фолиевой кислоты, необходимых для синтеза нуклеотидов — предшественников ДНК и РНК.
• Дезоксиаденозилкобаламин в качестве кофермента участвует в метаболизме жирных кислот с нечётным числом углеродных атомов и аминокислот с разветвлённой углеводородной цепью (см. разделы 8, 9).
Основной признак авитаминоза В12 — макроцитарная (мегалобластная) анемия. Для этого заболевания характерны увеличение размеров эритроцитов, снижение количества эритроцитов в кровотоке, снижение концентрации гемоглобина в крови. Нарушение кроветворения связано в первую очередь с нарушением обмена нуклеиновых кислот, в частности синтеза ДНК в быстроделящихся клетках кроветворной системы. Помимо нарушения кроветворной функции, для авитаминоза В12 специфично также расстройство деятельности нервной системы, объясняемое токсичностью метилмалоновой кислоты, накапливающейся в организме при распаде жирных кислот с нечётным числом углеродных атомов, а также некоторых аминокислот с разветвлённой цепью.
9. Витамин С (аскорбиновая кислота)
Аскорбиновая кислота — лактон кислоты, близкой по структуре к глюкозе. Существует в двух формах: восстановленной (АК) и окисленной (дегидроаскорбиновой кислотой, ДАК).
Обе эти формы аскорбиновой кислоты быстро и обратимо переходят друг в друга и в качестве коферментов участвуют в окислительновосстановительных реакциях. Аскорбиновая кислота может окисляться кислородом воздуха, пероксидом и другими окислителями. ДАК легко восстанавливается цистеином, глутатионом, сероводородом. В слабощелочной среде происходят разрушение лактонового кольца и потеря биологической активности. При кулинарной обработке пищи в присутствии окислителей часть витамина С разрушается.
Источники витамина С — свежие фрукты, овощи, зелень (табл. 3-1).
Суточная потребность человека в витамине С составляет 50 — 75 мг.
Биологические функции. Главное свойство аскорбиновой кислоты — способность легко окисляться и восстанавливаться. Вместе с ДАК она образует в клетках окислительновосстановительную пару с редокс-потенциалом +0,139 В. Благодаря этой способности аскорбиновая кислота участвует во многих реакциях гидроксилирования: остатков Про и Лиз при синтезе коллагена (основного белка соединительной ткани), при гидроксилировании дофамина, синтезе стероидных гормонов в коре надпочечников (см. разделы 9, 11).
В кишечнике аскорбиновая кислота восстанавливает Fе3+ в Fе2+, способствуя его всасыванию, ускоряет освобождение железа из ферритина (см. раздел 13), способствует превращению фолата в коферментные формы. Аскорбиновую кислоту относят к природным антиоксидантам (см. раздел 8). Большое значение этой роли витамина С придавал известный американский учёный Л. Полинг, дважды лауреат Нобелевской премии. Он рекомендовал использовать для профилактики и лечения ряда заболеваний (например, простудных) большие дозы аскорбиновой кислоты (2 — 3 г).
Клинические проявления недостаточности витамина С. Недостаточность аскорбиновой кислоты приводит к заболеванию, называемому цингой (скорбут). Цинга, возникающая у человека при недостаточном содержании в пищевом рационе свежих фруктов и овощей, описана более 300 лет назад, со времени проведения длительных морских плаваний и северных экспедиций. Это заболевание связано с недостатком в пище витамина С. Болеют цингой только человек, приматы и морские свинки. Главные проявления авитаминоза обусловлены в основном нарушением образования коллагена в соединительной ткани. Вследствие этого наблюдают разрыхление дёсен, расшатывание зубов, нарушение целостности капилляров (сопровождающееся подкожными кровоизлияниями). Возникают отёки, боль в суставах, анемия. Анемия при цинге может быть связана с нарушением способности использовать запасы железа, а также с нарушениями метаболизма фолиевой кислоты.
10. Витамин Р (биофлавоноиды)
В настоящее время известно, что понятие «витамин Р» объединяет семейство биофлавоноидов (катехины, флавононы, флавоны). Это очень разнообразная группа растительных полифенольных соединений, влияющих на проницаемость сосудов сходным образом с витамином С.
Наиболее богаты витамином Р лимоны, гречиха, черноплодная рябина, чёрная смородина, листья чая, плоды шиповника.
Суточная потребность для человека точно не установлена.
Биологическая роль флавоноидов заключается в стабилизации межклеточного матрикса соединительной ткани и уменьшении проницаемости капилляров. Многие представители группы витамина Р обладают гипотензивным действием.
Клиническое проявление гипоавитаминоза витамина Р характеризуется повышенной кровоточивостью дёсен и точечными подкожными кровоизлияниями, общей слабостью, быстрой утомляемостью и болями в конечностях.
Б. Жирорастворимые витамины
1. Витамин А (ретинол) — циклический, ненасыщенный, одноатомный спирт.
Источники. Витамин А содержится только в животных продуктах: печени крупного рогатого скота и свиней, яичном желтке, молочных продуктах; особенно богат этим витамином рыбий жир. В растительных продуктах (морковь, томаты, перец, салат и др.) содержатся каротиноиды, являющиеся провитаминами А. В слизистой оболочке кишечника и клетках печени содержится специфический фермент каротиндиоксигеназа, превращающий каротиноиды в активную форму витамина А.
Суточная потребность витамина А взрослого человека составляет от 1 до 2,5 мг витамина или от 2 до 5 мг (3-каротинов. Обычно активность витамина А в пищевых продуктах выражается в международных единицах; одна международная единица (МЕ) витамина А эквивалентна 0,6 мкг β-каротина и 0,3 мкг витамина А.
Биологические функции витамина А. В организме ретинол превращается в ретиналь и ретиноевую кислоту, участвующие в регуляции ряда функций (в росте и дифференцировке клеток); они также составляют фотохимическую основу акта зрения.
Наиболее детально изучено участие витамина А в зрительном акте (рис. 3-3). Светочувствительный аппарат глаза — сетчатка. Падающий на сетчатку свет адсорбируется и трансформируется пигментами сетчатки в другую форму энергии. У человека сетчатка содержит 2 типа рецепторных клеток: палочки и колбочки. Первые реагируют на слабое (сумеречное) освещение, а колбочки — на хорошее освещение (дневное зрение). Палочки содержат зрительный пигмент родопсин, а колбочки — йодопсин. Оба пигмента — сложные белки, отличающиеся своей белковой частью. В качестве кофермента оба белка содержат 11-цис-ретиналь, альдегидное производное витамина А.
Ретиноевая кислота, подобно стероидным гормонам, взаимодействует с рецепторами в ядре клеток-мишеней. Образовавшийся комплекс связывается с определёнными участками ДНК и стимулирует транскрипцию генов (см. раздел 4). Белки, образующиеся в результате стимуляции генов под влиянием ретиноевой кислоты, влияют на рост, дифференцировку, репродукцию и эмбриональное развитие (рис. 3-4).
Основные клинические проявления гиповитаминоза А. Наиболее ранний и характерный признак недостаточности витамина А у людей и экспериментальных животных — нарушение сумеречного зрения (гемералопия, или «куриная» слепота). Специфично для авитаминоза А поражение глазного яблока — ксерофтальмия, т. е. развитие сухости роговой оболочки глаза как следствие закупорки слёзного канала в связи с ороговением эпителия. Это, в свою очередь, приводит к развитию конъюнктивита, отёку, изъязвлению и размягчению роговой оболочки, т. е. к кератомаляции. Ксерофтальмия и кератомаляция при отсутствии соответствующего лечения могут привести к полной потере зрения.
У детей и молодых животных при авитаминозе А наблюдают остановку роста костей, кератоз эпителиальных клеток всех органов и, как следствие этого, избыточное ороговение кожи, поражение эпителия ЖКТ, мочеполовой системы и дыхательного аппарата. Прекращение роста костей черепа приводит к повреждению тканей ЦНС, а также к повышению давления спинномозговой жидкости. 2. Витамины группы D (кальциферолы) Кальциферолы — группа химически родственных соединений, относящихся к производным стеринов. Наиболее биологически активные витамины — D2 и D3. Витамин D2 (эргокальциферол), производное эргостерина — растительного стероида, встречающегося в некоторых грибах, дрожжах и растительных маслах. При облучении пищевых продуктов УФО из эргостерина получается витамин D2, используемый в лечебных целях. Витамин D3, имеющийся у человека и животных, — холекальциферол, образующийся в коже человека из 7-дегидрохолестерина под действием УФ-лучей (рис. 3-5).
Витамины D2 и D3— белые кристаллы, жирные на ощупь, нерастворимые в воде, но хорошо растворимые в жирах и органических растворителях.
Источники. Наибольшее количество витамина D3 содержится в продуктах животного происхождения: сливочном масле, желтке яиц, рыбьем жире.
Суточная потребность для детей 12 — 25 мкг (500 — 1000 МЕ), для взрослого человека потребность значительно меньше.
Биологическая роль. В организме человека витамин D3 гидроксилируется в положениях 25 и 1 и превращается в биологически активное соединение 1,25-дигидроксихоле- кальциферол (кальцитриол). Кальцитриол выполняет гормональную функцию, участвуя в регуляции обмена Са2+ и фосфатов, стимулируя всасывание Са2+ в кишечнике и кальцификацию костной ткани, реабсорбцию Са2+и фосфатов в почках. При низкой концентрации Са2+ или высокой концентрации D3 он стимулирует мобилизацию Са2+ из костей (см. раздел 11).
Недостаточность. При недостатке витамина D у детей развивается заболевание «рахит», характеризуемое нарушением кальцификации растущих костей. При этом наблюдают деформацию скелета с характерными изменениями костей (X- или о-образная форма ног, «чётки» на рёбрах, деформация костей черепа, задержка прорезывания зубов).
Избыток. Поступление в организм избыточного количества витамина D3 может вызвать гипервитаминоз D. Это состояние характеризуется избыточным отложением солей кальция в тканях лёгких, почек, сердца, стенках сосудов, а также остеопорозом с частыми переломами костей.
3. Витамины группы Е (токоферолы)
Витамин Е был выделен из масла зародышей пшеничных зёрен в 1936 г. и получил название токоферол. В настоящее время известно семейство токоферолов и токотриенолов, найденных в природных источниках. Все они — метальные производные исходного соединения токола, по строению очень близки и обозначаются буквами греческого алфавита. Наибольшую биологическую активность проявляет α-токоферол.
Токоферолы представляют собой маслянистую жидкость, хорошо растворимую в органических растворителях.
Источники витамина Е для человека — растительные масла, салат, капуста, семена злаков, сливочное масло, яичный желток.
Суточная потребность взрослого человека в витамине примерно 5 мг.
Биологическая роль. По механизму действия токоферол является биологическим антиоксидантом. Он ингибирует свободнорадикальные реакции в клетках и таким образом препятствует развитию цепных реакций перекисного окисления ненасыщенных жирных кислот в липидах биологических мембран и других молекул, например, ДНК (см. раздел 8). Токоферол повышает биологическую активность витамина А, защищая от окисления ненасыщенную боковую цепь.
Клинические проявления недостаточности витамина Е у человека до конца не изучены. Известно положительное влияние витамина Е при лечении нарушения процесса оплодотворения, при повторяющихся непроизвольных абортах, некоторых форм мышечной слабости и дистрофии. Показано применение витамина Е для недоношенных детей и детей, находящихся на искусственном вскармливании, так как в коровьем молоке в 10 раз меньше витамина Е, чем в женском. Дефицит витамина Е проявляется развитием гемолитической анемии, возможно из-за разрушения мембран эритроцитов в результате ПОЛ.
4. Витамины К (нафтохиноны)
Витамин К существует в нескольких формах в растениях как филлохинон (К1), в клетках кишечной флоры как менахинон (К2).
Источники витамина К — растительные (капуста, шпинат, корнеплоды и фрукты) и животные (печень) продукты. Кроме того, он синтезируется микрофлорой кишечника. Обычно авитаминоз К развивается вследствие нарушения всасывания витамина К в кишечнике, а не в результате его отсутствия в пище.
Суточная потребность в витамине взрослого человека составляет 1-2 мг.
Биологическая функция витамина К связана с его участием в процессе свёртывания крови (рис. 3-6). Он участвует в активации факторов свёртывания крови: протромбина (фактор II), проконвертина (фактор VII), фактора Кристмаса (фактор IX) и фактора Стюарта (фактор X). Эти белковые факторы синтезируются как неактивные предшественники. Один из этапов активации — их карбоксилирование по остаткам глутаминовой кислоты с образованием y-карбоксиглутаминовой кислоты, необходимой для связывания ионов кальция (см. раздел 13). Витамин К участвует в реакциях карбоксилирования в качестве кофермента.
Для лечения и предупреждения гиповитаминоза К используют синтетические производные нафтохинона: менадион, викасол, синкавит.
Основное проявление авитаминоза К — сильное кровотечение, часто приводящее к шоку и гибели организма.
3. Ситуационная задача. Пациентка 67 лет поступила в гастроэнтерологическое отделение в связи с обострением хронического атрофического гастрита. Анализ периферической крови: WBC – 4,3 × 109/л, RBC – 2,56 × 1012/л, Hb – 100 г/л, Ht – 29,8%, MCV – 116,5 фл, MCH – 39,2 пг, MCHC – 337 г/л, RDW – 20,8%, PLT – 160 × 109/л. Ретикулоциты –2%.
Вопрос: Предположительный диагноз по данному случаю:
Предполагаемый ответ:
А. железодефицитная анемия;
Б. мегалобластная анемия;
В. гемолитическая анемия вследствие механического разрушения эритроцитов;
Г. анемия хронических заболеваний;
Д. талассемия.
Контрольное правило вестгарда, позволяющее выявить случайную ошибку, наблюдается, когда
1) два последовательных контрольных результата с любой стороны от средней превышают контрольные пределы хср±2σ
2) десять последовательных результатов находятся на одной стороне от средней
3) четыре последовательных контрольных результата находятся на одной стороне от средней и превышают контрольные пределы хср+1σ
4) один контрольный результат превышает контрольные пределы xср+3σ (+)
Последовательность блоков: атомизатор → дифракционная решетка → детектор → регистратор является принципиальной схемой
1) атомно-абсорбционного спектрометра
2) рентгенофлуоресцентного спектрометра
3) масс-спектрометра
4) атомно-эмиссионного спектрометра (+)
К функциям, которые выполняет атомизатор в составе атомно-эмиссионного спектрометра, относят
1) атомизацию пробы и возбуждение атомов (+)
2) атомизацию пробы и ионизацию атомов элементов
3) атомизацию пробы и образование нестабильных изотопов элементов
4) только атомизацию
Ацетилирование относится к реакциям
1) I фазы метаболизма
2) несинтетическим
3) гидролитического расщепления
4) II фазы метаболизма (+)
Основным метаболитом морфина является
1) морфин-3-глюкуронид (+)
2) диацетилморфин
3) норморфин
4) кодеин
К алколоидам, производным индола, относится
1) лизергиновая кислота (+)
2) кокаин
3) атропин
4) кодеин
Если растворимость вещества в октаноле составляет 1:10, а в воде 1:1000, коэффициент распределения (октанол/вода) равен
1) 1,0
2) — 2,0
3) 2,0 (+)
4) 0,0
В процессе кумуляции наблюдается
1) синергизм веществ
2) видоизменение яда в более токсичное вещество
3) накопление яда в неизмененном виде (+)
4) потенцирование действия нескольких веществ
Непрямым способом изучения активности биотрансформации лекарственного средства является
1) фенотипирование
2) drug-мониторинг
3) генотипирование (+)
4) назначение ингибиторов ферментов
Степень острой интоксикации оксидом углерода определяется
1) процентным содержанием карбоксигемоглобина в крови, сохранностью сознания (+)
2) выраженностью изменений окраски кожных покровов, уровнем артериального давления
3) количеством телец Гейнца в эритроцитах, уровнем гемоглобина
4) частотой пульса, процентным содержанием метгемоглобина в крови
К преимуществам атомно-абсорбционной спектрометрии относят
1) высокую чувствительность, возможность сочетать качественный и количественный анализ, простоту исполнения (+)
2) низкую чувствительность, моноэлементный анализ, простоту метода
3) низкую стоимость, простоту исполнения
4) многоэлементный анализ, возможность анализа элементов и молекул, невозможность сочетания качественного и количественного анализа
Чем больше среднеквадратичное отклонение, тем больше величина _________ ошибки
1) биологической
2) систематической
3) вероятностной
4) случайной (+)
К функциям атомизатора в атомно-абсорбционном спектрометре относят
1) бомбардировку атомов исследуемого элемента пучком быстрых электронов
2) подготовку и подачу пробы в источник излучения
3) возбуждение атомов пробы
4) подготовку атомов пробы к поглощению световой энергии, разделение соединений в составе пробы на отдельные атомы (+)
В биологических и медицинских исследованиях принимают уровень значимости различий не выше
1) 0,01
2) 0,05 (+)
3) 0,005
4) 0,5
Аналитическая чувствительность теста характеризуется
1) минимальной достоверно выявляемой в процессе анализа концентрацией измеряемого вещества (+)
2) способностью теста в процессе анализа не реагировать на «посторонние» соединения в пробе
3) способностью теста достоверно выявлять анализируемое вещество
4) вероятностью правильного определения концентрации анализируемого вещества в образце
Межлабораторный контроль качества дает возможность
1) сравнить квалификацию персонала
2) сравнить качество работы нескольких лабораторий (+)
3) выявить нарушения санитарно-эпидемиологических правил
4) выявить нарушения соблюдения нормативных документов
Под нештатной ситуацией, при которой создается реальная или потенциальная возможность выделения патогенного агента в окружающую среду или заражения персонала, понимают
1) производственную микротравму
2) чрезвычайную ситуацию
3) производственную травму
4) аварию (+)
При возникновении контаминации в помещениях пцр-лаборатории следует
1) немедленно остановить работу и провести мероприятия по ликвидации контаминации (+)
2) продолжать работу
3) обработать рабочие поверхности 95%-м спиртом и продолжить работу
4) сменить перчатки, обработать рабочую поверхность дезинфицирующим раствором и продолжить работу
Выводы эксперта в заключении представляются в ______ форме
1) положительной или отрицательной
2) обоснованной или необоснованной
3) определенной или неопределенной
4) категорической или вероятностной (+)
Опасность заражения медицинских работников существует при
1) только при попадании ПБА на кожу или слизистые оболочки
2) любой медицинской манипуляции (+)
3) только при загрязнении одежды биологическими жидкостями
4) только в случае укола или пореза
1) МЕТОД СУПРАВИТАЛЬНОЙ ОКРАСКИ БРИЛЛИАНТОВЫМ КРЕЗИЛОВЫМ СИНИМ ПРИМЕНЯЕТСЯ ДЛЯ ОБНАРУЖЕНИЯ
1. ретикулоцитов
2. моноцитов
3. нейтрофилов
4. эритроцитов
2) ОКРАСКА МАЗКА КРОВИ ДЛЯ ПОДСЧЕТА ЛЕЙКОЦИТАРНОЙ ФОРМУЛЫ ПРОВОДИТСЯ ПО МЕТОДУ
1. Романовского-Гимза
2. Грама
3. Папаниколау
4. Циля-Нильсена
3) ПОДСЧЕТ МЕГАКАРИОЦИТОВ КОСТНОГО МОЗГА ПРОВОДЯТ В
1. камере Фукс-Розенталя
2. камере Горяева
3. мазке крови
4. счетчике клеток
4) МЕТОДОМ ОПРЕДЕЛЕНИЯ ОНКОМАРКЕРОВ В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ ЯВЛЯЕТСЯ
1. иммуноферментный анализ
2. иммуноэлектрофорез
3. полимеразная цепная реакция
4. реакция агглютинации
5) ОПРЕДЕЛЕНИЕ ГРУППЫ КРОВИ ОСНОВАНО НА РЕАКЦИИ
1. агглютинации
2. иммунодиффузии
3. иммуноэлектрофореза
4. преципитации
6) ИММУНОГИСТОХИМИЧЕСКИЕ МЕТОДЫ ОСНОВАНЫ НА ВЗАИМОДЕЙСТВИИ
1. антигена и меченого антитела
2. антигена, антитела и комплемента
3. растворимого антигена и антитела
4. фиксированного антигена и антитела
7) ПОЛИМЕРАЗНО-ЦЕПНАЯ РЕАКЦИЯ ОСНОВАНА НА
1. амплификации специфических участков ДНК
2. взаимодействии антигена и антитела
3. образовании иммунных комплексов
4. полимеризации молекул
ТЕСТОМ, ПОЗВОЛЯЮЩИМ ВЕРИФИЦИРОВАТЬ ГЕПАТИТ В, СЛУЖИТ ОПРЕДЕЛЕНИЕ
1. HBs-антигена с помощью иммуноферментного анализа
2. активности АЛТ и АСТ
3. увеличения билирубина
4. щелочной фосфатазы
9) СРЕДНИЙ ОБЪЁМ ЭРИТРОЦИТОВ (MCV) 80-100FL ХАРАКТЕРЕН ДЛЯ
1. нормоцитов
2. макроцитов
3. мегалоцитов
4. микроцитов
10) СРЕДНИЙ ОБЪЁМ ЭРИТРОЦИТОВ >100FL ХАРАКТЕРЕН ДЛЯ _________ АНЕМИИ
1. мегалобластной
2. апластической
3. гемолитической
4. железодефицитной
11) МИКРОЦИТОЗ ХАРАКТЕРЕН ДЛЯ АНЕМИИ
1. железодефицитной
2. В-12 дефицитной
3. беременных
4. при всех злокачественных заболеваниях
12) СОДЕРЖАНИЕ РЕТИКУЛОЦИТОВ В КРОВИ БОЛЕЕ 10% ПРИ ОТСУТСТВИИ ТЕРАПИИ ПРЕПАРАТАМИ ЖЕЛЕЗА СВИДЕТЕЛЬСТВУЕТ ОБ АНЕМИИ
1. гемолитической
2. В-12 дефицитной
3. гипопластической
4. железодефицитной
13) ГИПЕРСЕГМЕНТАЦИЯ НЕЙТРОФИЛОВ (>5 ФРАГМЕНТОВ) ХАРАКТЕРНА ДЛЯ
1. дефицита витамина В-12 и фолиевой кислоты
2. воспаления
3. гемолитической анемии
4. железодефицитной анемии
14) ОБНАРУЖЕНИЕ КОЛЕЦ КЕБОТА В ЭРИТРОЦИТАХ СВИДЕТЕЛЬСТВУЕТ О
1. свинцовой интоксикации
2. анемии беременных
3. гемолитической анемии
4. железодефицитной анемии
15) ТЕЛЬЦА ЖОЛЛИ В ЭРИТРОЦИТАХ НАБЛЮДАЮТСЯ ПРИ _______ АНЕМИИ
1. мегалобластной
2. гемолитической
3. железодефицитной
4. серповидноклеточной
16) В МОЧЕ В НОРМЕ ПРИСУТСТВУЕТ НЕБОЛЬШОЕ КОЛИЧЕСТВО _________ ЦИЛИНДРОВ
1. гиалиновых
2. восковидных
3. зернистых
4. эритроцитарных
17) К ЭЛЕМЕНТАМ ОРГАНИЗОВАННОГО ОСАДКА МОЧИ ОТНОСЯТ
1. цилиндры
2. аморфные соли
3. бактерии
4. кристаллы
18) ПРИ БАКТЕРИУРИИ ОСАДОК МОЧИ ОКРАШИВАЮТ ПО
1. Граму
2. Нейссеру
3. Папаниколау
4. Цилю — Нильсену
19) ВОСПРОИЗВОДИМОСТЬ РЕЗУЛЬТАТОВ ИЗМЕРЕНИЯ ХАРАКТЕРИЗУЕТСЯ
1. близостью результатов измерений одной и той же величины, полученных в разных местах разными операторами
2. близостью друг к другу результатов измерений одной и той же величины, выполненных в одной аналитической серии
3. разницей между предполагаемым результатом измерения и истинным значением измеряемой величины (или АЗ — аттестованным значением)
4. степенью близости среднего значения и истинной величины измеряемого параметра
20) СХОДИМОСТЬ РЕЗУЛЬТАТОВ ИЗМЕРЕНИЯ ХАРАКТЕРИЗУЕТСЯ
1. близостью друг к другу результатов измерений одной и той же величины, выполненных в одной аналитической серии
2. близостью результатов измерений одной и той же величины, полученных в разных местах разными операторами
3. разницей между предполагаемым результатом измерения и истинным значением измеряемой величины (или АЗ — аттестованным значением)
4. степенью близости среднего значения и истинной величины измеряемого параметра
21) ПРАВИЛЬНОСТЬ ИЗМЕРЕНИЯ ОПРЕДЕЛЯЕТ
1. степень близости среднего значения и истинной величины измеряемого параметра
2. близость друг к другу результатов измерений одной и той же величины, выполненных в одной аналитической серии
3. близость результатов измерений одной и той же величины, полученных в разных местах разными операторами
4. разницу между предполагаемым результатом измерения и истинным значением измеряемой величины (или АЗ — аттестованным значением)
22) СМЕЩЕНИЕ РЕЗУЛЬТАТОВ ИЗМЕРЕНИЯ ХАРАКТЕРИЗУЕТСЯ
1. разницей между предполагаемым результатом измерения и истинным значением измеряемой величины (или АЗ — аттестованным значением)
2. близостью друг к другу результатов измерений одной и той же величины, выполненных в одной аналитической серии
3. близостью результатов измерений одной и той же величины, полученных в разных местах разными операторами
4. степенью близости среднего значения и истинной величины измеряемого параметра
23) КОНТРОЛЬНОЕ ПРАВИЛО ВЕСТГАРДА, УКАЗЫВАЮЩЕЕ НА СЛУЧАЙНУЮ ОШИБКУ, НАБЛЮДАЕТСЯ, ЕСЛИ
1. разница между максимальным и минимальным контрольными результатами превышает хср+4σ
2. два последовательных контрольных результата с любой стороны от средней превышают контрольные пределы хср±2σ
3. десять последовательных результатов находятся на одной стороне от средней
4. четыре последовательных контрольных результата находятся на одной стороне от средней и превышают контрольные пределы хср+1σ
24) КОНТРОЛЬНОЕ ПРАВИЛО ВЕСТГАРДА, КОТОРОЕ ПОЗВОЛЯЕТ ВЫЯВИТЬ СИСТЕМАТИЧЕСКУЮ ОШИБКУ, ИМЕЕТ МЕСТО, КОГДА
1. десять последовательных результатов находятся на одной стороне от средней
2. один контрольный результат превышает контрольные пределы xср+2σ
3. один контрольный результат превышает контрольные пределы xср+3σ
4. разница между максимальным и минимальным контрольными результатами превышает хср+4σ
25) КОНТРОЛЬНОЕ ПРАВИЛО ВЕСТГАРДА, ПОЗВОЛЯЮЩЕЕ ВЫЯВИТЬ СИСТЕМАТИЧЕСКУЮ ОШИБКУ, НАБЛЮДАЕТСЯ, КОГДА
1. два последовательных контрольных результата с любой стороны от средней превышают контрольные пределы хср±2σ
2. один контрольный результат превышает контрольные пределы xср+2σ
3. один контрольный результат превышает контрольные пределы xср+3σ
4. разница между максимальным и минимальным контрольными результатами превышает хср+4σ
26) КОНТРОЛЬНОЕ ПРАВИЛО ВЕСТГАРДА, ПОЗВОЛЯЮЩЕЕ ВЫЯВИТЬ СЛУЧАЙНУЮ ОШИБКУ, НАБЛЮДАЕТСЯ, КОГДА
1. один контрольный результат превышает контрольные пределы xср+3σ
2. два последовательных контрольных результата с любой стороны от средней превышают контрольные пределы хср±2σ
3. десять последовательных результатов находятся на одной стороне от средней
4. четыре последовательных контрольных результата находятся на одной стороне от средней и превышают контрольные пределы хср+1σ
27) ПОКАЗАТЕЛИ КОНТРОЛЬНЫХ КАРТ СВИДЕТЕЛЬСТВУЮТ О СТАБИЛЬНОСТИ РАБОТЫ АНАЛИЗИРУЕМОЙ ЛАБОРАТОРНОЙ СИСТЕМЫ В ТОМ СЛУЧАЕ, КОГДА
1. анализируемые значения показателей находятся по обе стороны от среднего значения и не выходят за пределы хср±2σ
2. десять последовательных результатов находятся на одной стороне от средней
3. один контрольный результат превышает контрольные пределы xср+3σ
4. разница между максимальным и минимальным контрольными результатами превышает хср+4σ
28) ВНЕШНИЙ КОНТРОЛЬ КАЧЕСТВА ОПРЕДЕЛЯЕТ
1. систему объективной оценки качества лабораторных исследований в разных лабораториях
2. контроль использования лабораторных методов исследования в разных лабораториях
3. оценку качества метрологического контроля в разных лабораториях
4. систему оценки качества методов, используемых в разных лабораториях
29) ПОГРЕШНОСТЬ РЕЗУЛЬТАТА ИЗМЕРЕНИЙ ХАРАКТЕРИЗУЕТСЯ ОТКЛОНЕНИЕМ РЕЗУЛЬТАТОВ ИЗМЕРЕНИЙ
1. истинного (действительного) значения
2. одной и той же пробы при использовании различных методов
3. одной и той же пробы при использовании разных приборов
4. одной и той же пробы разными операторами
30) СЛУЧАЙНАЯ ПОГРЕШНОСТЬ ИЗМЕРЕНИЯ ХАРАКТЕРИЗУЕТ
1. составляющую погрешности, случайным образом изменяющуюся при повторных измерениях
2. абсолютную погрешность, деленную на истинное значение измеряемой величины
3. погрешность между измеряемым и истинным значением измеряемой величины
4. погрешность, превосходящую все предыдущие погрешности измерений
31) СИСТЕМАТИЧЕСКАЯ ПОГРЕШНОСТЬ ИЗМЕРЕНИЯ ХАРАКТЕРИЗУЕТСЯ КАК ПОГРЕШНОСТЬ
1. повторяющаяся в серии измерений
2. зависящая от значения измеряемой величины
3. между измеренным и истинным значением измеряемой величины
4. не зависящая от значения измеряемой величины
32) В ЦИТОПЛАЗМЕ НЕЙТРОФИЛОВ ОБНАРУЖЕНЫ КРУПНЫЕ ВКЛЮЧЕНИЯ ТЕМНО-СИНЕГО ЦВЕТА И ВАКУОЛИЗАЦИЯ, ЧТО ХАРАКТЕРНО ДЛЯ
1. синдрома Чедиака-Хигаси
2. дефекта адгезии лейкоцитов
3. дефицита миелопероксидазы
4. хронического гранулематоза
33) ПОДОБНОЕ ИЗМЕНЕНИЕ ФОРМЫ ЭРИТРОЦИТОВ ХАРАКТЕРНО ДЛЯ АНЕМИИ 
1. серповидно-клеточной
2. беременных
3. гемолитической
4. железодефицитной
34) ПРИ МИКРОСКОПИИ МОКРОТЫ ОБНАРУЖЕНЫ КРУПНЫЕ КЛЕТКИ ОКРУГЛОЙ ФОРМЫ БЛЕДНО-ГОЛУБОГО ЦВЕТА С ЧЕТКИМИ КОНТУРАМИ, КОТОРЫЕ СЛЕДУЕТ ОПРЕДЕЛИТЬ КАК
1. альвеолярные макрофаги
2. липофаги
3. макрофаги с гемосидерином
4. макрофаги с частицами пыли
35) В ЛЮБОМ ОБРАЗЦЕ МОКРОТЫ ПРИ МИКРОСКОПИИ В НОРМЕ МОЖНО ОБНАРУЖИТЬ КЛЕТКИ
1. плоского эпителия
2. базальные
3. промежуточные
4. цилиндрического мерцательного эпителия
36) СТАТИСТИЧЕСКИЙ ПОКАЗАТЕЛЬ, ВЫРАЖЕННЫЙ ФОРМУЛОЙ ОТРАЖАЕТ 
1. стандартное, или среднеквадратическое, отклонение
2. коэффициент аналитической вариации
3. смещение измерений
4. стандартную (среднюю) ошибку
37) СТАТИСТИЧЕСКИЙ ПОКАЗАТЕЛЬ, ВЫРАЖЕННЫЙ ФОРМУЛОЙ ОТРАЖАЕТ 
1. смещение измерений
2. коэффициент аналитической вариации
3. стандартное, или среднеквадратическое, отклонение
4. стандартную (среднюю) ошибку
38) СТАТИСТИЧЕСКИЙ ПОКАЗАТЕЛЬ, ВЫРАЖЕННЫЙ ФОРМУЛОЙ ОТРАЖАЕТ 
1. коэффициент аналитической вариации
2. смещение измерений
3. стандартное, или среднеквадратическое, отклонение
4. стандартную (среднюю) ошибку
39) СТАТИСТИЧЕСКИЙ ПОКАЗАТЕЛЬ, ВЫРАЖЕННЫЙ ФОРМУЛОЙ ОТРАЖАЕТ 
1. стандартную (среднюю) ошибку
2. коэффициент аналитической вариации
3. смещение измерений
4. стандартное, или среднеквадратическое, отклонение
40) КОНТРОЛЬНАЯ КАРТА ШУХАРТА ВЫЯВЛЯЕТ _____________ В РАБОТЕ ЛАБОРАТОРИИ ПРИ ОПРЕДЕЛЕНИИ КОНКРЕТНОГО _________ ЛАБОРАТОРНОГО ПАРАМЕТРА 
1. случайные погрешности; количественного
2. систематические ошибки; качественного
3. систематические ошибки; количественного
4. случайные погрешности; качественного
41) КОЭФФИЦИЕНТ ВАРИАЦИИ ИСПОЛЬЗУЮТ ДЛЯ ОЦЕНКИ
1. воспроизводимости измерений
2. правильности измерений
3. специфичности используемого метода
4. чувствительности используемого метода
42) МУТНОСТЬ МОЧИ, ВЫЗВАННУЮ ПРИСУТСТВИЕМ ФОРМЕННЫХ ЭЛЕМЕНТОВ, МОЖНО УДАЛИТЬ
1. центрифугированием
2. добавлением кислоты
3. добавлением щёлочи
4. нагреванием до 30°С
43) РЕАКЦИЯ ВОДЫ ПРИ ПРИГОТОВЛЕНИИ КРАСКИ ПО РОМАНОВСКОМУ ПРИ ОКРАСКЕ МАЗКОВ И ТОЛСТЫХ КАПЕЛЬ НА МАЛЯРИЮ ДОЛЖНА БЫТЬ
1. 7,0
2. 6,8
3. 7,4
4. 8,2
44) ОПТИМАЛЬНЫМ АНТИКОАГУЛЯНТОМ ПРИ ОПРЕДЕЛЕНИИ ПОКАЗАТЕЛЕЙ КИСЛОТНО-ОСНОВНОГО СОСТОЯНИЯ ЯВЛЯЕТСЯ
1. литиевая соль гепарина
2. гепарин натрия
3. цитрат натрия
4. этилендиаминтетрауксусная кислота
45) РЕФЕРЕНТНЫМ МЕТОДОМ ИССЛЕДОВАНИЯ УРОВНЯ ГЛИКЕМИИ ЯВЛЯЕТСЯ МЕТОД
1. гексокиназный
2. глюкозооксидазный
3. ортотолуидиновый
4. преобразования меди по Бенедикту
46) БЕЛОК БЕНС-ДЖОНСА МОЖНО ОПРЕДЕЛИТЬ С ИСПОЛЬЗОВАНИЕМ
1. электрофореза белков мочи
2. диализа мочи
3. реакции преципитации
4. ультрацентрифугирования белков мочи
47) С ДИАГНОСТИЧЕСКОЙ ЦЕЛЬЮ АКТИВНОСТЬ ФЕРМЕНТОВ ЧАЩЕ ВСЕГО ОПРЕДЕЛЯЮТ В
1. сыворотке
2. ликворе
3. моче
4. слюне
48) ПРИ ДИАГНОСТИКЕ ХРОНИЧЕСКОГО ГЕПАТИТА ЦЕЛЕСООБРАЗНО ИССЛЕДОВАТЬ АКТИВНОСТЬ
1. аланинаминотрансферазы, аспартатаминотрансферазы, γ-глутамилтранспептидазы, щелочной фосфатазы
2. изоферментов щелочной фосфатазы
3. кислой фосфатазы, урокиназы
4. лактатдегидрогеназы, креатинкиназы
49) В ЗАМОРОЖЕННОМ ОБРАЗЦЕ ПЛАЗМЫ НЕВОЗМОЖНО ОПРЕДЕЛИТЬ
1. антигемофильный глобулин А (VIII)
2. антигемофильный глобулин С (ХI)
3. проконвертин (VII)
4. протромбин (II)
50) ОПРЕДЕЛЕНИЕ ПРОТЕИНА С НЕОБХОДИМО ДЛЯ
1. выявления риска тромбоза
2. выявления риска кровотечения
3. оценки фибринолиза
4. подбора дозы непрямых антикоагулянтов
Правила Вестгарда представляют собой набор статистических шаблонов, появление каждого из которых маловероятно из-за случайной изменчивости, что вызывает подозрение в неправильной точности или прецизионности измерительной системы. Они используются для лабораторного контроля качества в «сериях», состоящих из измерений нескольких образцов. Они представляют собой набор модифицированных правил Western Electric, разработанных и представленных в его книгах и семинарах по контролю качества. Правила следующие:
| Правило | Критерии | Подозреваемые | Пример |
|---|---|---|---|
| 12s | Одно измерение превышает 2 стандартных отклонения либо выше, либо ниже среднего. эталонного диапазона. | Погрешность и / или неточность |  |
| 13s | Одно измерение превышает 3 стандартных отклонения либо выше, либо ниже среднего значения эталонного диапазона. | Неточность и / или неточность |  |
| 22s | 2 последовательных измерения превышают 2 стандартных отклонения от эталонного диапазона и находятся на той же стороне от среднего. | Неточность. |  |
| R4s | Два измерения в одном прогоне имеют разницу в 4 стандартных отклонения (например, одно превышает 2 стандартных отклонения выше среднего, а другое превышает 2 стандартных отклонения ниже среднего). | Неточность. |  |
| 41s | 4 последовательных измерения превышают 1 стандартное отклонение на той же стороне от среднего. | Неточность. |  |
| 10x | 10 последовательных измерений находятся по одну сторону от среднего. | Неточность. |  |
Рекомендуемые последствия при возникновении любого из вышеперечисленных шаблонов — отказ от выполнения, за исключением правила 1 2s (вверху в таблице), которое служит предупреждением и рекомендацией к тщательной проверке данные.
См. также
- правила Western Electric
- правила Нельсона
Ссылки
Внешние ссылки
- Официальный сайт
288. [T014594] ФУНКЦИОНАЛЬНУЮ АКТИВНОСТЬ NK-КЛЕТОК ОЦЕНИВАЮТ С ПОМОЩЬЮ
А) цитотоксического теста
Б) НСТ-теста
В) теста кожного окна
Г) иммуноблоттинга
289. [T014595] ФУНКЦИОНАЛЬНАЯ АКТИВНОСТЬ Т-ЛИМФОЦИТОВ ОЦЕНИВАЕТСЯ С ПОМОЩЬЮ
А) теста митоген-индуцированной пролиферации
Б) иммуноблоттинга
В) теста кожного окна
Г) иммуноферментного анализа
290. [T014598] ФЕНОТИПОМ Т-ХЕЛПЕРОВ I ТИПА ЯВЛЯЕТСЯ
А) CD4+/внутриклеточный интерферон-гамма+
Б) CD4+ /внутриклеточный интерлейкин-4+
В) CD8+/внутриклеточный интерлекин-2+
Г) CD8 /внутриклеточный интерферон-альфа+
291. [T014599] МЕТОДОМ ИММУНОДИАГНОСТИКИ НА ОСНОВЕ ИСПОЛЬЗОВАНИЯ МОНОКЛОНАЛЬНЫХ АНТИТЕЛ ЯВЛЯЕТСЯ
А) лазерная проточная цитометрия Б) конА-индуцированная пролиферация лимфоцитов В) тест кожного окна Г) цитотоксический тест
292. [T014600] ИММУНОДИАГНОСТИКА ПРИ ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЯХ НАПРАВЛЕНА НА
А) идентификацию возбудителя
Б) идентификацию дефектов иммунитета
В) определение степени тяжести
Г) определение распространенности процесса
61
293. [T014601] ИММУНОДИАГНОСТИКА В ТРАНСПЛАНТОЛОГИИ И ТРАНСФУЗИОЛОГИИ НАПРАВЛЕНА НА
А) подбор пары донор-реципиент Б) определение показаний для трансплантации/трансфузии
В) оценку эффективности трансплантации/трансфузии Г) исследование уровня аутоантител
294. [T014868] МЕТОД СУПРАВИТАЛЬНОЙ ОКРАСКИ БРИЛЛИАНТОВЫМ КРЕЗИЛОВЫМ СИНИМ ПРИМЕНЯЕТСЯ ДЛЯ ОБНАРУЖЕНИЯ
А) ретикулоцитов
Б) эритроцитов
В) нейтрофилов
Г) моноцитов
295. [T014869] ОКРАСКА МАЗКА КРОВИ ДЛЯ ПОДСЧЕТА ЛЕЙКОЦИТАРНОЙ ФОРМУЛЫ ПРОВОДИТСЯ ПО МЕТОДУ
А) Романовского-Гимза
Б) Грама
В) Циля-Нильсена
Г) Папаниколау
296. [T014870] ПОДСЧЕТ МЕГАКАРИОЦИТОВ КОСТНОГО МОЗГА ПРОВОДЯТ В
А) камере Фукс-Розенталя
Б) камере Горяева
В) счетчике клеток
Г) мазке крови
297. [T014872] ОСНОВНЫМ МЕТОДОМ ОПРЕДЕЛЕНИЯ ОНКОМАРКЕРОВ В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ ЯВЛЯЕТСЯ
А) иммуноферментный анализ
Б) реакция агглютинации
В) иммуноэлектрофорез
Г) полимеразно-цепная реакция
62
298. [T014874] ОПРЕДЕЛЕНИЕ ГРУППЫ КРОВИ ОСНОВАНО НА РЕАКЦИИ
А) агглютинации
Б) преципитации
В) иммунодиффузии
Г) иммуноэлектрофореза
299. [T014876] ИММУНОГИСТОХИМИЧЕСКИЕ МЕТОДЫ ОСНОВАНЫ НА ВЗАИМОДЕЙСТВИИ
А) антигена и меченого антитела Б) антигена, антитела и комплемента
В) растворимого антигена и антитела Г) фиксированного антигена и антитела
300. [T014877] ПОЛИМЕРАЗНО-ЦЕПНАЯ РЕАКЦИЯ ОСНОВАНА НА
А) амплификации специфических участков ДНК
Б) взаимодействии антигена и антитела
В) полимеризации молекул
Г) образовании иммунных комплексов
301. [T014879] ТЕСТОМ, ПОЗВОЛЯЮЩИМ ВЕРИФИЦИРОВАТЬ ГЕПАТИТ «В», СЛУЖИТ ОПРЕДЕЛЕНИЕ
А) HBs-антигена с помощью иммуноферментного анализа
Б) активности АЛТ и АСТ
В) увеличения билирубина
Г) щелочной фосфатазы
302. [T014880] СРЕДНИЙ ОБЪЁМ ЭРИТРОЦИТОВ (MCV) 80-100FL ХАРАКТЕРЕН ДЛЯ
А) нормоцитов
Б) микроцитов
В) макроцитов
Г) мегалоцитов
63
303. [T014881] СРЕДНИЙ ОБЪЁМ ЭРИТРОЦИТОВ >100FL ХАРАКТЕРЕН ДЛЯ
_________ АНЕМИИ
А) мегалобластной
Б) железодефицитной
В) гемолитической
Г) апластической
304. [T014882] МИКРОЦИТОЗ ХАРАКТЕРЕН ДЛЯ АНЕМИИ
А) железодефицитной
Б) В-12 дефицитной
В) беременных
Г) при всех злокачественных заболеваниях
305. [T014883] СОДЕРЖАНИЕ РЕТИКУЛОЦИТОВ КРОВИ БОЛЕЕ 10% СВИДЕТЕЛЬСТВУЕТ О _________ АНЕМИИ
А) гемолитической
Б) железодефицитной
В) В-12 дефицитной
Г) гипопластической
306. [T014884] ГИПЕРСЕГМЕНТАЦИЯ НЕЙТРОФИЛОВ (>5 ФРАГМЕНТОВ) ХАРАКТЕРНА ДЛЯ
А) дефицита витамина В-12 и фолиевой кислоты
Б) железодефицитной анемии
В) воспаления
Г) гемолитической анемии
307. [T014885] ОБНАРУЖЕНИЕ КОЛЕЦ КЕБОТА В ЭРИТРОЦИТАХ СВИДЕТЕЛЬСТВУЕТ О
А) свинцовой интоксикации
Б) железодефицитной анемии
В) гемолитической анемии
Г) анемии беременных
64
308. [T014886] ТЕЛЬЦА ЖОЛЛИ В ЭРИТРОЦИТАХ НАБЛЮДАЮТСЯ ПРИ
_______ АНЕМИИ
А) мегалобластной
Б) серповидноклеточной
В) гемолитической
Г) железодефицитной
309. [T014887] В МОЧЕ В НОРМЕ ПРИСУТСТВУЕТ НЕБОЛЬШОЕ КОЛИЧЕСТВО
_________ ЦИЛИНДРОВ
А) гиалиновых
Б) зернистых
В) эритроцитарных
Г) восковидных
310. [T014890] К ЭЛЕМЕНТАМ ОРГАНИЗОВАННОГО ОСАДКА МОЧИ ОТНОСЯТ
А) цилиндры
Б) кристаллы
В) аморфные соли
Г) бактерии
311. [T014891] ДЛЯ ВЫЯВЛЕНИЯ БАКТЕРИЙ В МОЧЕ ОСАДОК ОКРАШИВАЮТ ПО
А) Граму
Б) Нейссеру
В) Папаниколау
Г) Цилю-Нильсену
65
312. [T014892] ВОСПРОИЗВОДИМОСТЬ РЕЗУЛЬТАТОВ ИЗМЕРЕНИЯ ХАРАКТЕРИЗУЕТСЯ
А) близостью результатов измерений одной и той же величины, полученных в разных местах разными операторами
Б) близостью друг к другу результатов измерений одной и той же величины, выполненных в одной аналитической серии
В) степенью близости среднего значения и истинной величины измеряемого параметра
Г) разницей между предполагаемым результатом измерения и истинным значением измеряемой величины (или АЗ — аттестованным значением)
313. [T014893] СХОДИМОСТЬ РЕЗУЛЬТАТОВ ИЗМЕРЕНИЯ ХАРАКТЕРИЗУЕТСЯ
А) близостью друг к другу результатов измерений одной и той же величины, выполненных в одной аналитической серии
Б) близостью результатов измерений одной и той же величины, полученных в разных местах разными операторами
В) степенью близости среднего значения и истинной величины измеряемого параметра
Г) разницей между предполагаемым результатом измерения и истинным значением измеряемой величины (или АЗ — аттестованным значением)
314. [T014894] ПРАВИЛЬНОСТЬ ИЗМЕРЕНИЯ ОПРЕДЕЛЯЕТ
А) степень близости среднего значения и истинной величины измеряемого параметра
Б) разницу между предполагаемым результатом измерения и истинным значением измеряемой величины (или АЗ — аттестованным значением)
В) близость друг к другу результатов измерений одной и той же величины, выполненных в одной аналитической серии
Г) близость результатов измерений одной и той же величины, полученных в разных местах разными операторами
66
315. [T014895] СМЕЩЕНИЕ РЕЗУЛЬТАТОВ ИЗМЕРЕНИЯ ХАРАКТЕРИЗУЕТСЯ
А) разницей между предполагаемым результатом измерения и истинным значением измеряемой величины (или АЗ — аттестованным значением)
Б) близостью результатов измерений одной и той же величины, полученных в разных местах разными операторами
В) близостью друг к другу результатов измерений одной и той же величины, выполненных в одной аналитической серии
Г) степенью близости среднего значения и истинной величины измеряемого параметра
316. [T014896] КОНТРОЛЬ КАЧЕСТВА БИОХИМИЧЕСКИХ ИССЛЕДОВАНИЙ ПРОВОДИТСЯ С
А) контрольными промышленными сыворотками (жидкими или лиофилизированными)
Б) донорскими сыворотками
В) сыворотками пациентов
Г) растворами, содержащими определяемый субстрат
317. [T014897] КОНТРОЛЬНОЕ ПРАВИЛО ВЕСТГАРДА, УКАЗЫВАЮЩЕЕ НА СЛУЧАЙНУЮ ОШИБКУ, НАБЛЮДАЕТСЯ, ЕСЛИ
А) разница между максимальным и минимальным контрольными результатами превышает хср+4σ
Б) четыре последовательных контрольных результата находятся на одной стороне от средней и превышают контрольные пределы хср+1σ
В) десять последовательных результатов находятся на одной стороне от средней
Г) два последовательных контрольных результата с любой стороны от средней превышают контрольные пределы хср±2σ
318. [T014898] КОНТРОЛЬНОЕ ПРАВИЛО ВЕСТГАРДА, КОТОРОЕ ПОЗВОЛЯЕТ ВЫЯВИТЬ СИСТЕМАТИЧЕСКУЮ ОШИБКУ, ИМЕЕТ МЕСТО, КОГДА
А) десять последовательных результатов находятся на одной стороне от средней
Б) разница между максимальным и минимальным контрольными результатами превышает хср+4σ
В) один контрольный результат превышает контрольные пределы xср+3σ
Г) один контрольный результат превышает контрольные пределы xср+2σ
67
319. [T014899] КОНТРОЛЬНОЕ ПРАВИЛО ВЕСТГАРДА, ПОЗВОЛЯЮЩЕЕ ВЫЯВИТЬ СИСТЕМАТИЧЕСКУЮ ОШИБКУ, НАБЛЮДАЕТСЯ, КОГДА
А) два последовательных контрольных результата с любой стороны от средней превышают контрольные пределы хср±2σ
Б) разница между максимальным и минимальным контрольными результатами превышает хср+4σ
В) один контрольный результат превышает контрольные пределы xср+3σ
Г) один контрольный результат превышает контрольные пределы xср+2σ
320. [T014900] КОНТРОЛЬНОЕ ПРАВИЛО ВЕСТГАРДА, ПОЗВОЛЯЮЩЕЕ ВЫЯВИТЬ СЛУЧАЙНУЮ ОШИБКУ, НАБЛЮДАЕТСЯ, КОГДА
А) один контрольный результат превышает контрольные пределы xср+3σ
Б) четыре последовательных контрольных результата находятся на одной стороне от средней и превышают контрольные пределы хср+1σ
В) десять последовательных результатов находятся на одной стороне от средней
Г) два последовательных контрольных результата с любой стороны от средней превышают контрольные пределы хср±2σ
321. [T014901] ПОКАЗАТЕЛИ КОНТРОЛЬНЫХ КАРТ СВИДЕТЕЛЬСТВУЮТ О СТАБИЛЬНОСТИ РАБОТЫ АНАЛИЗИРУЕМОЙ ЛАБОРАТОРНОЙ СИСТЕМЫ В ТОМ СЛУЧАЕ, КОГДА
А) анализируемые значения показателей находятся по обе стороны от среднего значения и не выходят за пределы хср±2σ
Б) десять последовательных результатов находятся на одной стороне от средней
В) разница между максимальным и минимальным контрольными результатами превышает хср+4σ
Г) один контрольный результат превышает контрольные пределы xср+3σ
322. [T014902] КОНТРОЛЬ КАЧЕСТВА ПРАВИЛЬНОСТИ ИЗМЕРЕНИЙ ПОКАЗАТЕЛЯ ПРОВОДИТСЯ С
А) промышленными сыворотками с известным содержанием вещества Б) сливными сыворотками с известным содержанием вещества
В) промышленными сыворотками с неисследованным содержанием вещества Г) сыворотками пациентов с неисследованным содержанием вещества
68
323. [T014903] ВНЕШНИЙ КОНТРОЛЬ КАЧЕСТВА ОПРЕДЕЛЯЕТ
А) систему объективной оценки качества лабораторных исследований в разных лабораториях
Б) контроль использования лабораторных методов исследования в разных лабораториях
В) систему оценки качества методов, используемых в разных лабораториях Г) оценку качества метрологического контроля в разных лабораториях
324. [T014904] ПОГРЕШНОСТЬ РЕЗУЛЬТАТА ИЗМЕРЕНИЙ ХАРАКТЕРИЗУЕТСЯ ОТКЛОНЕНИЕМ РЕЗУЛЬТАТОВ ИЗМЕРЕНИЙ
А) истинного (действительного) значения Б) одной и той же пробы разными операторами
В) одной и той же пробы при использовании различных методов Г) одной и той же пробы при использовании разных приборов
325. [T014905] СЛУЧАЙНАЯ ПОГРЕШНОСТЬ ИЗМЕРЕНИЯ ХАРАКТЕРИЗУЕТ
А) составляющую погрешности, случайным образом изменяющуюся при повторных измерениях
Б) погрешность между измеряемым и истинным значением измеряемой величины В) абсолютную погрешность, деленную на истинное значение измеряемой величины Г) погрешность, превосходящую все предыдущие погрешности измерений
326. [T014906] СИСТЕМАТИЧЕСКАЯ ПОГРЕШНОСТЬ ИЗМЕРЕНИЯ ХАРАКТЕРИЗУЕТСЯ КАК ПОГРЕШНОСТЬ
А) повторяющаяся в серии измерений Б) между измеренным и истинным значением измеряемой величины
В) зависящая от значения измеряемой величины Г) не зависящая от значения измеряемой величины
69
327. [T014907] В ЦИТОПЛАЗМЕ НЕЙТРОФИЛОВ ОБНАРУЖЕНЫ КРУПНЫЕ ВКЛЮЧЕНИЯ ТЕМНО-СИНЕГО ЦВЕТА И ВАКУОЛИЗАЦИЯ, ЧТО ХАРАКТЕРНО ДЛЯ
А) синдрома Чедиака-Хигаси
Б) хронического гранулематоза
В) дефекта адгезии лейкоцитов
Г) дефицита миелопероксидазы
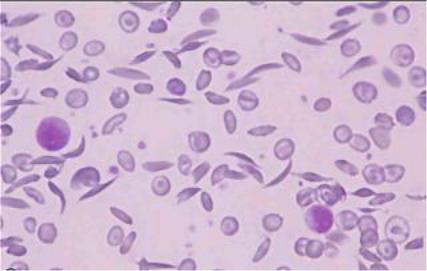
328. [T014908] ПОДОБНОЕ ИЗМЕНЕНИЕ ФОРМЫ ЭРИТРОЦИТОВ
ХАРАКТЕРНО ДЛЯ АНЕМИИ
А) серповидно-клеточной
Б) железодефицитной
В) гемолитической
Г) беременных
329. [T014909] ПРИ МИКРОСКОПИИ МОКРОТЫ ОБНАРУЖЕНЫ КРУПНЫЕ КЛЕТКИ ОКРУГЛОЙ ФОРМЫ БЛЕДНО-ГОЛУБОГО ЦВЕТА С ЧЕТКИМИ КОНТУРАМИ, КОТОРЫЕ СЛЕДУЕТ ОПРЕДЕЛИТЬ КАК
А) альвеолярные макрофаги
Б) липофаги
В) макрофаги с частицами пыли
Г) макрофаги с гемосидерином
70
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
|
Внутрилабораторный контроль качества |
Теоретические основы лабораторного контроля качества
Здравствуйте!
В прошлый понедельник начали рассказ о теоретических основах контроля качества. Сегодня продолжение темы: контрольные материалы и порядок проведения ВКК.
Контрольные материалы: виды, требования, рекомендации по выбору и правила использования
Контрольным называется однородный материал, результаты исследования которого используются для оценки погрешности выполняемого аналитического измерения. Как правило, исследование контрольных материалов выполняется на аналитическом этапе лабораторного исследования и, соответственно, позволяет оценить погрешности, возникающие только на этом этапе. Контрольный материал не может быть использован одновременно в качестве калибровочного.
1. Виды контрольных материалов
При внутрилабораторном контроле используются контрольные материалы промышленного изготовления, допущенные
в установленном порядке к применению на территории России. Вместе с тем, при невозможности приобрести контрольные материалы промышленного изготовления, в лаборатории могут использоваться контрольные материалы, которые готовятся из неиспользованных остатков образцов пациентов — слитые сыворотки, плазма, моча, приготовленные в самой лаборатории.
Контрольные материалы промышленного производства выпускаются как с исследованными (установленными, аттестованными),
так и неисследованными значениями контролируемых параметров. В инструкции (паспорте) к аттестованным контрольным материалам указываются установленные значения и, как правило, допустимые диапазоны результатов измерения, определенные производителем. Контрольные материалы с исследованным содержанием используются для контроля правильности и воспроизводимости результатов лабораторного анализа, с неисследованным — для контроля воспроизводимости.
Для биохимических, иммунохимических и гормональных исследований выпускаются контрольные материалы (контрольные сыворотки) промышленного производства, которые разделяются на универсальные и специальные. Универсальные содержат большое количество компонентов, концентрация или активность которых исследована
по широкому спектру методов.
Специальные контрольные сыворотки предназначены для контроля качества определения отдельных показателей, исследуемых
с определенной диагностической целью, например для диагностики анемий, повреждения сердечной мышцы (креатинкиназа, лактатдегидрогеназа и их изоферменты), отдельных компонентов (С-реактивного белка; ревматоидного фактора; гормонов; этанола; аммиака; газов крови (водные, забуференные растворы); компонентов, определяемых при терапевтическом мониторинге лекарств, в том числе методами тонкослойной и высокоразрешающей жидкостной хроматографии; компонентов, исследуемых методами «сухой» химии на отражательных фотометрах.
2. Рекомендации по выбору и приобретению контрольных материалов
При выборе контрольных материалов следует обращать внимание на следующие его характеристики:
— срок годности стабилизированной формы материала
— срок годности материала после вскрытия флакона или растворения
лиофилизированного содержимого
— время растворения (реконструкции) лиофилизированных форм
— тип матрикса матрицы контрольного материала (предпочтительнее
использование материалов с матриксомцей человеческого происхождения, в отсутствие таковых допускается использование контрольных материалов животного происхождения, за исключением некоторых аналитических методов)
— значения определяемых показателей должны находиться в клинически значимом диапазоне.
Для осуществления ежесерийного внутрилабораторного контроля рекомендуется использовать два контрольных материала со значениями определяемых показателей в нормальном и патологических диапазонах соответственно. При использовании во внутрилабораторном
контроле только одного контрольного материала желательно, чтобы эти значения были близки к «границе принятия решения» (граница нормальных и патологических значений). Соответствие перечня аналитов в закупаемом контрольном материале аналитам, исследуемым в лаборатории:
— наличие в паспорте контрольного материала установленных метод- зависимых значений, соответствующих методам, используемым
в лаборатории;
— достаточность количества закупаемого контрольного материала
для возможности его использования в течение длительного времени (от 6 месяцев до 3 лет, в зависимости от срока годности контрольного материала).
3. Использование контрольных материалов
Перед использованием контрольного материала необходимо тщательно изучить инструкцию (паспорт) к нему. Несмотря на то, что в инструкции изготовителей обычно содержатся сведения
об отсутствии в контрольном материале антигенов вирусных гепатитов и ВИЧ, обращаться с ним следует как с потенциально инфекционным. Перед вскрытием флакона необходимо зарегистрировать серию и номер контрольного материала. Подготовка контрольного материала к исследованию проводится
в соответствии с инструкцией производителя. Особое внимание следует обращать на:
— аккуратное вскрытие флакона, чтобы избежать потерь материала;
— точное пипетирование растворителя бидистиллированной
или деионизированной воды (для анализа кальция, фосфора, железа,
хлоридов);
— осторожное перемешивание содержимого после того, как флакон
закрыт пробкой так, чтобы омыть частички материала на пробке
(не допуская пенообразования);
— соблюдение времени растворения.
Для уменьшения погрешности пипетирования необходимо
при добавлении растворителя использовать одну и ту же стеклянную пипетку (класса а или другую тщательно откалиброванную весовым способом), хорошо отмытую и отвечающую требованиям для анализа кальция, фосфора, железа.
Для экономного использования контрольного материала содержимое флакона после его растворения и перемешивания разливают в пробирки или флаконы с герметичными крышками на объемы, достаточные
для поведения контроля исследований в течение одного дня (но не менее 0,5 мл), и замораживают при –20 °С и более низких температурах. Материал, из которого изготовлены пробирки или флаконы, не должен при длительном хранении адсорбировать кальций, альбумин и другие компоненты. Допускается только однократное замораживание
и оттаивание контрольной сыворотки и только для тех компонентов
и методов, для которых оно допустимо. Оттаивание контрольной сыворотки следует проводить при комнатной температуре. Далее работа с ней проводится так же, как с жидкими контрольными материалами. При этом всегда должно соблюдаться правило: контрольные материалы должны исследоваться так же, как обычные пробы пациентов,
т.е. в тех же сериях и в тех же условиях.
Результаты исследования компонентов в контрольной сыворотке сравниваются с метод-зависимыми установленными значениями, указанными в инструкции (паспорте) производителя (контроль правильности). При выборе установленного значения учитываются: принцип метода, прибор, а при определении ферментов — температура реакции, буфер, субстрат, активирующие добавки
в реактивы (например, наличие или отсутствие пиридоксальфосфата для методов определения аспартат- и аланинаминотрансфераз, N-ацетилцистеина — для креатинкиназы, трансфосфорилирующего буфера для щелочной фосфатазы и др.).
Порядок проведения внутрилабораторного контроля качества
Введение и дальнейшее осуществление внутрилабораторного контроля качества для каждой из методик состоят из трех последовательных стадий:
1. Оценка внутрисерийной воспроизводимости методики
2. Оценка систематической погрешности и общей воспроизводимости методики, построение контрольной контрольных карты
3. Оперативный (текущий) внутрилабораторный контроль качества
Первая стадия может быть выполнена с использованием пробы пациента или контрольного материала со значением определяемого показателя
в нормальном диапазоне, т.е. проведение оперативного (текущего) контроля качества результатов лабораторных исследований в каждой аналитической серии.
Для выполнения третьей, основной стадии внутрилабораторного контроля лаборатория должна располагать достаточным количеством одного (допускается) или двух разных (рекомендуется) неаттестованных контрольных материалов, которые используются также и на второй стадии. Помимо этого, для выполнения второй стадии требуется использование одного (допускается) или двух разных (рекомендуется) разных аттестованных контрольных материалов. Как уже указывалось, при использовании двух контрольных материалов значениями определяемых показателей в них должны соответствовать нормальному и патологическому диапазонам соответственно. при использовании одного контрольного материала желательно, чтобы эти значения
были близки к границае между нормальными и патологическими значениями со значениями определяемых показателей в нормальном
и патологических диапазонах соответственно, а также двух неаттестованных контрольных материалов, выбранных лабораторией для использования в третьей стадии внутрилабораторного контроля,
с аналогичными значениями определяемых показателей.
1. Стадия 1 (вводная): оценка внутрисерийной воспроизводимости методики
На данной стадии проводится проверка соответствия внутрисерийной воспроизводимости методики установленным нормам точности. с этой целью проводится 10 измерений определяемого показателя в одном
и том же материале (контрольный материал или проба пациента со значением определяемого показателя в нормальном диапазоне) в одной и той же аналитической серии. из полученных 10 результатов по формулам 2–4 рассчитывается коэффициент внутрисерийной вариации методики (CVвс) и проверяется, что он не превышает половины предельно допустимого значения коэффициента общей аналитической вариации для 10 измерений CV10 в таблице Приложения),
т.е. выполняется неравенство:
CVвс ≤ 0,5 · СV10
Если это неравенство не выполняется, т.е. коэффициент внутрисерийной вариации методики составляет больше половины предельно допустимого значения коэффициента общей аналитической вариации, следует провести работу по снижению внутрисерийной вариации данной методики или избрать другую методику определения данного показателя с лучшей внутрисерийной воспроизводимостью.
Если внутрисерийная вариация методики отвечает установленным нормам, переходят к следующей стадии.
2. Стадия 2 (вводная): оценка смещения и коэффициента общей аналитической вариации методики, построение контрольной карты
На данной стадии одновременно решаются две задачи:
— во-первых, оценивается соответствие величин систематической
погрешности (смещения) и коэффициента общей аналитической вариации методики установленным нормам, т.е. окончательно решается вопрос о возможности ее использования для целей лабораторной диагностики, и
— во-вторых, для каждого из двух (одного) контрольных материалов, предназначенных для использования на третьей стадии, создается контрольная карта (диаграмма) — основной инструмент внутрилабораторного контроля качества количественных исследований.
Для решения первой задачи выполняют следующее:
- В 10 аналитических сериях измеряют значение определяемого показателя, выполняя по 1 измерению в каждой серии одновременно в двух неаттестованных контрольных материалах, выбранных
для оперативного (ежесерийного) контроля, и в двух аттестованных контрольных материалах. - Указанные 10 серий рекомендуется выполнять по одной в день. При необходимости сократить период их выполнения (например, из-за ограниченного срока годности реактивов, приготовленных из готового набора) допускается проведение по 2–3 серии в день (например, утром, днем, вечером).
- По 10 результатам, полученным для каждого из двух аттестованных материалов, с использованием формулы 1 рассчитывают соответственно две величины относительного смещения (В10).
- По 10 результатам, полученным для каждого из двух неаттестованных материалов, с использованием формул 2–4 рассчитывают соответственно два значения коэффициента общей аналитической вариации (СV10).
- Проверяют, что полученные значения В10 и СV10 не превышают
их предельно допустимых значений, приведенных в таблице 1 Приложения 3 данного документа. Если последнее выполняется, переходят к выполнению следующего шага (пункт 6). В случае превышения одной одним из полученных значений В10 или СV10 соответствующих или обеими величинами В10 и/или СV10 предельно допустимых значений проводят работу по устранению источников повышенных смещения и/или вариации или избирают другую методику определения данного показателя (с более высокими аналитическими характеристиками), после чего выполняют пункты 1–4 заново. - Таким же образом, как описано в пункте 1, выполняют измерения в 10 дополнительных аналитических сериях.
- Для каждого аттестованного материала по 20 результатам, полученным для каждого из двух аттестованных материалов в 20 выполненных сериях, с использованием формулы 1 рассчитывают соответственно две величины относительного смещения (В20).
- Для каждого неаттестованного материала по 20 результатам, полученным для каждого из двух неаттестованных материалов
в 20 выполненных сериях, с использованием формул 2–4 рассчитывают соответственно два значения коэффициента общей аналитической вариации (СV20). - Проверяют, что полученные значения В20 и СV20 не превышают
их предельно допустимые значения, приведенные в таблице 1 Приложения 3 данного документа. Если это условие выполняется, делают окончательный вывод о возможности использования рассматриваемой методики для целей лабораторной диагностики
и переходят к построению контрольных карт. В случае превышения одним из полученных значений одной или обеими величинами В20 и/или СV20 соответствующих предельно допустимых значений проводят дополнительную работу по устранению источников повышенных смещения и/или вариации или избирают другую методику определения данного показателя (с более высокими аналитическими характеристиками).
Для решения второй задачи (построения контрольной карты) выполняют следующее:
Из полученных 20 результатов исследований определяемого показателя для каждого из двух контрольных материалов, предназначенных предназначенного для текущего ежесерийного контроля, рассчитывают:
— Среднюю арифметическую величину Х,
— Среднее квадратическое отклонение S,
— Контрольные пределы: Х±1S, Х±2S и Х±3S.
Если для в ряду результатов, полученных для одного из контрольных материалов, результатов есть значение, выходящее за пределы
±3S, то его отбрасывают и для этого материала проводят еще одну аналитическую серию, после чего снова подсчитывают значения Х и S.
Для каждого из материалов с использованием рассчитанных значений строят контрольную карту. Последняя представляет собой график,
на оси абсцисс которого откладывают номер аналитической серии (или дату ее выполнения), а на оси ординат — значения определяемого показателя в контрольном материале (рис. 1). Через середину оси ординат проводят линию, соответствующую средней арифметической величине Х, и параллельно этой линии отмечают линии, соответствующие контрольным пределам:
Х±1S — контрольный предел — «1 среднее квадратическое отклонение»;
Х±2S — контрольный предел — «2 средних квадратических отклонения»;
Х±3S — контрольный предел — «3 средних квадратических отклонения».
Последовательность процедур при введении внутрилабораторного контроля качества и рассчитываемые при этом показатели приведены в таблице.
| Название процедуры | Исследуемый материал | Число серии | Число измерений в серии | Рассчитываемые показатели |
|---|---|---|---|---|
| Стадия 1 | ||||
| Оценка внутрисерийной вариации методики | Контрольный материал или проба пациента | 1 | 10 | CVВС |
| Стадия 2 | ||||
| Предварительная оценка систематической погрешности методики | Аттестованные контрольные материалы | 10 | 1 | B10 |
| Предварительная оценка воспроизводимости методики | Контрольные материалы для текущего ежесерийного контроля | 10 | 1 | CV10 |
| Окончательная оценка систематической погрешности методики | Аттестованные контрольные материалы | 20 | 1 | B20 |
| Окончательная оценка воспроизводимости методики | Контрольные материалы для текущего ежесерийного контроля | 20 | 1 | CV20 |
| Построение контрольной карты | Контрольные материалы для текущего ежесерийного контроля | 20 | 1 | Х, S |
Стадия 3 (основная): оперативный (текущий) внутрилабораторный контроль качества
С использованием построенных контрольных карт осуществляют оперативный (текущий) контроль качества результатов определения исследуемого показателя. с этой целью (который проводится в каждой аналитической серии) проводится по одному измерению в каждом
из двух контрольных материалов; или два измерения в одном и том же контрольном материале, если используется единственный материал (в последнем случае на контрольную карту наносят по две точки на серию). При этом образцы контрольных материалов распределяют равномерно среди анализируемых проб пациентов,
в каждой серии для каждого из двух материалов выполняют по одному определению распределяют равномерно среди анализируемых проб пациентов.
Оценку результатов исследования контрольных материалов проводят с использованием по соответствующим контрольным правилам (признаков/ам) Westgard, получившим название (по имени их автора) множественных правил “Westgard” «вручную» или с помощью специальных компьютерных программ.
«Контрольные» правила Вестгарда (Westgard):
12S — если одно контрольное измерение оказалось за пределами Xср±2S, тогда проводится проверка нижеследующих контрольных признаков:
13S — одно контрольное измерение выходит за пределы (Xср±3S);
22S — два последних контрольных измерения превышают предел (Xср±2S);
R4S — два контрольных измерения одной аналитической серии находятся по разные стороны Xср±2S (этот признак не проверяется при одном измерении в серии одного контрольного материала);
41S — четыре последних контрольных измерения превышают предел (Xср±1S);
10x — десять последних контрольных измерений лежат по одну сторону Xср±1S;
Если присутствует хотя бы один из вышеперечисленных контрольных признаков, аналитическая серия бракуется. Следует найти источник ошибки, устранить причину, после чего переделывается вся серия
— и контрольные материалы и пробы пациентов. если ни один из признаков Вестгарда не определяется, серия принимается, и результаты пациентов сообщаются лечащим врачам.
Целесообразность использования данного алгоритма для проверки стабильности работы заключается в простоте его применения в случае «ручного» способа интерпретации контрольной карты. Применение правила 12S в качестве предупредительного позволяет экономить время и усилия, поскольку не нужно проверять весь набор признаков, если текущее контрольное измерение находится в пределах Хср±2S. Использование компьютерных программ (например, Vision QC) для ведения внутрилабораторного контроля качества позволяет не только автоматизировать все расчеты, построение контрольных карт,
анализ по правилам для всех контролируемых тестов, но и предоставляет дополнительные возможности лаборатории при интерпретации результатов оперативного контроля. Лаборатория может по желанию применять для проведения оперативного контроля дополнительный набор «предупредительных» правил (по выбору). Предупредительные правила сигнализируют о возможной недопустимой ошибке до того, как обнаружится «контрольное» правило. При этом можно выявить
и устранить причины, приводящие к изменению характеристик метода, пока ситуация не вышла из-под контроля.
Примеры «предупредительных» правил:
12S — Результат находится за пределами Хср±2S.
7х — Семь результатов подряд лежат по одну сторону от среднего;
7t — Семь результатов подряд имеют тенденцию к возрастанию
или убыванию;
31S — Три результата подряд находятся за пределами Хср–1S или Xcp–1S.
5х — Пять результатов подряд лежат по одну сторону от среднего.
Контрольная карта позволяет контролировать как правильность, так и воспроизводимость метода.
Пример контрольных карт для двух контрольных материалов,на которых представлены серии, являющиеся неудовлетворительными ввиду нарушения разных контрольных правил, приведен на рисунке. Пул а — контрольный материал с нормальными значениями: Х = 100, S = 4
Аналогичный пример контрольной карты в случае использования одного контрольного материала с двумя измерениями в серии представлен
на риcунке ниже. Пул А — контрольный материал с нормальным значением: Хср = 100, S = 4
Дополнительные критерии в системе внутрилабораторного контроля качества
Хорошим дополнением к контрольным правилам Westgard, в практической работе КДЛ, могут быть использованы:
— метод кумулятивных сумм (CUSUM)
— индекс среднеквадратичного отклонения (SDI)
— повторные измерения пробы пациента
1. CUSUM — метод кумулятивных сумм
Для выявления небольших систематических погрешностей
в вызывающем сомнении тесте можно использовать данный подход. При этом подразумевается, что для каждого исследуемого субстрата, содержание которого измеряется в контрольном материале, определено среднее арифметическое значение (Хср) и среднеквадратическое отклонение (S). Используя расчетные показатели, устанавливают некоторый верхний и нижний пределы для каждого уровня контрольных материалов и пороговое значение CUSUM. Появление любого результата, выходящего за один из пределов, инициирует вычисление CUSUM. Вычисление продолжается для последовательных результатов контрольных измерений до тех пор, пока кумулятивная сумма
либо выходит за пределы порогового показателя, что характеризуется как выход результатов измерения исследуемого аналита из-под контроля, либо изменит знак.
Для постоянного использования этого метода во внутрилабораторном контроле Westgard рекомендует устанавливать эти значения следующим образом: ±0,5S от средней арифметической в качестве пределов
для начала подсчета CUSUM и ±5,1S в качестве порогового значения CUSUM. Это обеспечивает низкую вероятность ложной выбраковки результатов и выявление минимальной систематической погрешности.
2. Пример применения метода CUSUM
Предположим в ходе расчета среднего значения (Хср) аналита лактатдегидрогеназы (ЛДГ) получен показатель равный 117 Ед/л,
а среднеквадратическое отклонение (S) — 5 Ед/л. Соответственно критерием для начала подсчета CUSUM (±0,5S = 5/2 =2,5 Ед/л ) будет — 114,5 (117 – 2,5 = 114,5 Ед/л) и 119,5 (117 + 2,5 = 119,5 Ед/л). Пороговое значение, определяемое данным методом будет ±5,1S (±5,1S = 5,1 × 5Ед/л = 25,5 Ед/л).
Наблюдение ведется за каждым контрольным измерением. Вычисление CUSUM начинается в случае, если полученное значение выходит
за пределы, установленных заранее (в нашем примере, нижнее
значение — 114,5 и верхний предел — 119,5 Ед/л). Разность между каждым новым полученным значением и установленными пределами накапливается с учетом знака этой разницы и сравнивается с величиной порогового значения (в нашем примере — 25,5 Ед/л). Вычисление CUSUM продолжается до тех пор, пока не произойдет изменение знака или значение не выйдет за пороговое значение.
| Дата | Серия | Значение | Разность | CUSUM | Комментарий |
|---|---|---|---|---|---|
| 02.01 | 1 | 119 | |||
| 02.01 | 2 | 117 | |||
| 02.01 | 1 | 108 | –6,5 | –6,5 | Начало вычисления CUSUM |
| 03.01 | 1 | 123 | +8,5 | +2,0 | Конец CUSUM |
| 04.01 | 3 | 119 | |||
| 05.01 | 3 | 126 | +6,5 | +6,5 | Начало вычисления CUSUM |
| 06.01 | 1 | 127 | +7,5 | +13,5 | |
| 07.01 | 1 | 126 | +6,5 | +20,0 | |
| 07.01 | 1 | 126 | +6,5 | +26,5 | Выход из-под контроля |
В приведенном примере первые два значения для контрольного материала не выходят за установленные границы. Третий результат (108 Ед/л) ниже установленного минимального предела
(114,5 – 108,0 = 6,5) на 6,5 Ед/л. Начинаем расчет CUSUM. Последующее значение (123 Ед/л) выше предела, но в этом случае в вычислении CUSUM учитывается разность с нижним допустимым пределом
(123,0 – 114,5 = 8,5), которое было нарушено предыдущим котрольным значением (108,0 Ед/л). Исходя из расчетов разница составила
+8,5; а значение CUSUM составила +2,0 (+8,5 – 6,5 = 2,0). В данном случае произошло изменение знака, после чего накопление CUSUMостанавливается и значение обнуляется. это хороший качественный признак. Шестой результат (126,0) превышает верхнее пограничное значение, и вычисление CUSUM возобновляется. Все последующие уровни ЛДГ превышают максимальные значения, следовательно показатель CUSUM только увеличивается. Расчет CUSUM прекращается на девятом показателе, т.к. нарушено верхнее пограничное значение. В этом случае требуется тщательная аналитическая
проверка методики исследования ЛДГ, выявление возможных ошибок и их устранение.
Данная методика оценки (CUSUM) позволяет более детально
по сравнению с правилами Westgard выявить лабораторные ошибки
в системе внутрилабораторного контроля качества. Семь из девяти значений были выше среднего и четыре значения — на грани основного контрольного правила Westgard: Х±2S, которое «включает» применение других критериев для уточнения ситуации.
Применяется и другой подход к расчету пороговых пределов CUSUM: ±1S/±2,75S. Однако данный расчет обладает меньшей чувствительностью выявления систематической ошибки.
В целом, характеризуя метод CUSUM, следует указать, что методика расчета вручную весьма затруднительна и трудоемкая. В век компьютерных технологий, используя соответствующие программы метод кумулятивных сумм (CUSUM) широко используется для ведения внутрилабораторного контроля качества (ВКК).
3. Индекс среднеквадратического отклонения (SDI)
Как правило, SDI применяют в системах внешней оценки качества, однако его можно использовать и для слежения за ВКК. Например, если возникает подозрение на появление дрейфа результатов контрольных измерений. Дрейф — это тенденция к отклонению
в одном направлении или постепенное, часто едва заметное, увеличение или уменьшение результатов контрольных измерений. Тип систематической ошибки.
В случае если требуется выявить дрейф, для расчета индекса надо использовать не результаты группы сравнения, а кумулятивные статистические параметры лаборатории — среднее арифметическое значение и среднеквадратическое отклонение, полученные
во всех предыдущих сериях, и среднее арифметическое контрольных измерений в 20 последних сериях. Выражение для SDI в этом случае будет выглядеть следующим образом:
SDI = (Х20последних – Хкумулятивное)/Sкумулятивное
где Х20последних — среднее арифметическое контрольных измерений в 20 последних сериях; Хкумулятивное и Sкумулятивное — среднее арифметическое и среднеквадратическое всех предыдущих контрольных измерений.
Значение SDI, превышающее ±1,5, означает, что дрейф весьма вероятен. при таких значениях требуется провести обслуживание прибора и/или перекалибровку аналитической системы. После чего повторить контрольные измерения.
На этом теоретическая часть завершена. Через неделю лабораторный практикум — рассмотрим контроль качества на примере исследования содержания гемоглобина. Не пропустите!

Ваша Вест Медика.
From Wikipedia, the free encyclopedia
The Westgard rules are a set of statistical patterns, each being unlikely to occur by random variability, thereby raising a suspicion of faulty accuracy or precision of the measurement system. They are used for laboratory quality control, in «runs» consisting of measurements of multiple samples. They are a set of modified Western Electric rules, developed by James Westgard and provided in his books and seminars on quality control.[1] They are plotted on Levey–Jennings charts, wherein the X-axis shows each individual sample, and the Y-axis shows how much each one differs from the mean in terms of standard deviation (SD). The rules are:[2]
| Rule | Criteria | Suspected | Example |
|---|---|---|---|
| 12s | One measurement exceeds 2 standard deviations either above or below the mean of the reference range. | Inaccuracy and/or imprecision | 
|
| 13s | One measurement exceeds 3 standard deviations either above or below the mean of the reference range. | Inaccuracy and/or imprecision | 
|
| 22s | 2 consecutive measurements exceed 2 standard deviations of the reference range, and on the same side of the mean. | Inaccuracy and/or imprecision | 
|
| R4s | Two measurements in the same run have a 4 standard deviation difference (such as one exceeding 2 standard deviations above the mean, and another exceeding 2 standard deviations below the mean). | Imprecision. | 
|
| 41s | 4 consecutive measurements exceed 1 standard deviation on the same side of the mean. | Inaccuracy. | 
|
| 10x | 10 consecutive measurements are on the same side of the mean. | Inaccuracy. | 
|
The recommended consequences when any of the above patterns occur is to reject the run, except for the rule of 12s (top in table), which serves as a warning and a recommendation of careful inspection of the data.[2]
See also[edit]
- Western Electric rules
- Nelson rules
References[edit]
- ^ Ofer Harel; Enrique F. Schisterman; Albert Vexler & Marcus D. Ruopp (July 2008). «Monitoring Quality Control: Can We Get Better Data?». Epidemiology. 19 (4): 621. doi:10.1097/ede.0b013e318176bfb2. PMC 2625303. PMID 18496467.
- ^ a b Heidi Hanes. «Westgard Rules — Guidelines». SMILE, Johns Hopkins University. Review date: 1 April 2020
External links[edit]
- Official website
From Wikipedia, the free encyclopedia
The Westgard rules are a set of statistical patterns, each being unlikely to occur by random variability, thereby raising a suspicion of faulty accuracy or precision of the measurement system. They are used for laboratory quality control, in «runs» consisting of measurements of multiple samples. They are a set of modified Western Electric rules, developed by James Westgard and provided in his books and seminars on quality control.[1] They are plotted on Levey–Jennings charts, wherein the X-axis shows each individual sample, and the Y-axis shows how much each one differs from the mean in terms of standard deviation (SD). The rules are:[2]
| Rule | Criteria | Suspected | Example |
|---|---|---|---|
| 12s | One measurement exceeds 2 standard deviations either above or below the mean of the reference range. | Inaccuracy and/or imprecision | 
|
| 13s | One measurement exceeds 3 standard deviations either above or below the mean of the reference range. | Inaccuracy and/or imprecision | 
|
| 22s | 2 consecutive measurements exceed 2 standard deviations of the reference range, and on the same side of the mean. | Inaccuracy and/or imprecision | 
|
| R4s | Two measurements in the same run have a 4 standard deviation difference (such as one exceeding 2 standard deviations above the mean, and another exceeding 2 standard deviations below the mean). | Imprecision. | 
|
| 41s | 4 consecutive measurements exceed 1 standard deviation on the same side of the mean. | Inaccuracy. | 
|
| 10x | 10 consecutive measurements are on the same side of the mean. | Inaccuracy. | 
|
The recommended consequences when any of the above patterns occur is to reject the run, except for the rule of 12s (top in table), which serves as a warning and a recommendation of careful inspection of the data.[2]
See also[edit]
- Western Electric rules
- Nelson rules
References[edit]
- ^ Ofer Harel; Enrique F. Schisterman; Albert Vexler & Marcus D. Ruopp (July 2008). «Monitoring Quality Control: Can We Get Better Data?». Epidemiology. 19 (4): 621. doi:10.1097/ede.0b013e318176bfb2. PMC 2625303. PMID 18496467.
- ^ a b Heidi Hanes. «Westgard Rules — Guidelines». SMILE, Johns Hopkins University. Review date: 1 April 2020
External links[edit]
- Official website
