Слезозаместительная терапия синдрома «сухого глаза»
Искусственные заменители слезы
Одним из основных направлений лечения синдрома «сухого глаза» (ССГ) на современном этапе является применение искусственных заменителей слезы, содержащих водную основу и повышающих вязкость смазочных веществ на основе природных или синтетических полимеров. Данные компоненты, воздействуя на водный и муциновый слои прероговичной слезной пленки (СП), смешиваются с остатками нативной слезы и образуют собственную прероговичную СП [1]. Благодаря этому достигается гомеостатическое равновесие между постоянным испарением слезной жидкости и ее выработкой.
Искусственные заменители слезы в зависимости от степени вязкости подразделяются на средства низкой, средней, высокой вязкости и гели. К препаратам данной фармакологической группы предъявляются следующие требования [2]: стерильность; соответствие физиологическому значению рН естественной слезы (уровень pH=7,2–7,4); изотоничность; соответствующая осмолярность (181–354 мОсмоль/л); оптимальная вязкость, превышающая вязкость слезной жидкости, — 15–30 сПз или 5–15 мПа-с; бесцветность и прозрачность (без отрицательного влияния на оптические свойства глаза); отсутствие механических включений и риска загрязнения микрофлорой; отсутствие эффекта привыкания; хорошая переносимость и отсутствие токсичности; возможность применения при ношении контактных линз.
Фармацевтический рынок на сегодняшний день предлагает широкий ассортимент полимерных слезозаменителей (лубрикантов), содержащих полусинтетические (кармеллоза и гидроксипропилметилцеллюлоза) и синтетические полимеры (полиэтиленгликоль, пропиленгликоль, поливинилпирролидон, поливиниловый спирт, повидон, карбомер). В ряде препаратов используются природные полисахариды (натриевая соль гиалуроновой кислоты, гидроксипропилгуар, декстран, трегалоза, TS-полисахарид), обладающие максимальными восполняющими свойствами при патологии водного и муцинового слоев СП и стимулирующие регенерацию эпителия глазной поверхности [2, 3]. Помимо полимерной основы препараты искусственной слезы могут содержать электролиты, буферные растворы, регуляторы вязкости, а также консерванты, препятствующие росту микроорганизмов при вскрытии флакона [2].
Одним из традиционных компонентов искусственных слезозаменителей является гиалуроновая кислота (ГК), получившая широкое распространение благодаря образованию эффективной связи с водой, устойчивости к высыханию и отличной биосовместимости. ГК впервые была выделена из стекловидного тела глазного яблока в 1934 г. немецким биохимиком K. Meyer и его американским ассистентом J. Palmer, а позже была обнаружена также в слезной железе, эпителии роговицы, конъюнктиве и слезной жидкости [4]. Необходимо отметить, что офтальмологические препараты, изготовленные на основе ГК, полностью биосовместимы и при инстилляции в конъюнктивальную полость не вызывают чувства инородного тела [4, 5]. ГК является природным полимером и относится к группе полисахаридов, которые также называют полисахаридами соединительной ткани, мукополисахаридами или гликозаминогликанами [4, 6]. Данная группа веществ влияет на распределение воды в соединительной ткани, в т. ч. и в строме роговицы [7]. Так, например, ГК обладает выраженной способностью удерживать воду за счет большого количества гидроксильных групп, образующих водородные связи [7, 8]. Согласно исследованиям данная кислота способна удержать количество воды, в 1000 раз превышающее ее собственную массу [7]. При повышении градиента давления и температуры окружающей среды ГК снижает вязкоэластические свойства раствора [7, 8]. Помимо этого, ГК обладает противовоспалительными свойствами [4] и способна стимулировать миграцию эпителиоцитов, способствуя заживлению эрозий роговицы, устранению неровностей глазной поверхности и стабилизируя состояние СП [8]. I.C. You et al. отмечают, что наибольший терапевтический эффект наблюдается на фоне применения 0,3% раствора ГК: более высокая концентрация препарата благотворно влияет на процесс заживления эрозий роговицы, увеличивает плотность бокаловидных клеток конъюнктивы, снижает апоптоз эпителиоцитов роговой оболочки [9].
Другими компонентами искусственных заменителей слезы, применяемыми при лечении ССГ, являются карбоксиметилцеллюлоза и гидроксипропилцеллюлоза. Эти полисахариды увеличивают вязкость слезной жидкости, способствуют восстановлению эпителиальных клеток роговицы и применяются, как правило, в сочетании с ГК. Растворимая гидроксипропилцеллюлоза используется в препарате Lacrisert (Bausch&Lomb, США), который помещается в нижний конъюнктивальный свод и, растворяясь в течение 12 ч, утолщает СП. Препарат рекомендуется к применению у пациентов с умеренной и тяжелой степенью ССГ, однако противопоказан при высокой чувствительности к гидроксипропилцеллюлозе [6].
Гидроксипропилгуар — водорастворимый природный полисахарид, являющийся производным гуаровой камеди, наиболее эффективный и часто используемый компонент слезозаменителей, восполняющий муциновый слой СП. В составе капель с гидроксипропилгуаром обязательными составляющими являются борная кислота, при взаимодействии с которой образуется структурированный гелеобразный раствор, и сорбитол, препятствующий преждевременной связи гидроксипропилгуара с борат-ионами. Попадая на глазную поверхность, борная кислота взаимодействует с двухвалентными ионами кальция, магния и цинка слезной жидкости, благодаря чему связь с гидроксипропилгуаром становится более прочной. Образующаяся на поверхности роговицы тонкая высокомолекулярная пленка эффективно увлажняет глазную поверхность, повышает время разрыва СП, минимизирует испарение слезы за счет снижения ее осмолярности и препятствует тем самым высыханию роговицы [6, 10].
Большое число научных исследований последних лет посвящено изучению влияния природного дисахарида трегалозы на организм человека, обладающей способностью вызывать аутофагию клеток [11, 12]. Согласно экспериментальным исследованиям in vitro и in vivo трегалоза защищает клетки роговицы от высыхания, препятствует апоптозу эпителиоцитов роговицы и конъюнктивы и их ультрафиолет (УФ) -индуцированному окислительному повреждению [6, 13]. Установлено, что под воздействием этого дисахарида существенно снижается содержание конъюнктивальных провоспалительных цитокинов и восстанавливается осмотический баланс слезы у лабораторных мышей [6, 14]. При лечении поврежденной роговицы трегалозой отмечается быстрое купирование воспаления, подавляются формирование рубца и неоваскуляризация роговой оболочки. Отсутствие токсичных свойств у данного дисахарида позволяет применять его у человека в течение длительного времени [13]. Наибольший терапевтический эффект трегалозы наблюдается при совместном применении с ГК. Добавление трегалозы способствует улучшению переносимости и эффективности проводимого лечения с точки зрения облегчения симптомов (по данным опросника OSDI (Ocular Surface Disease Index — индекс поражения поверхности глаза)), по сравнению с инстилляциями фармакологического препарата, содержащего в своем составе только гиалуронат, что, по мнению исследователей, демонстрирует биопротекторное действие трегалозы [15].
Согласно клиническим исследованиям благотворное влияние на течение ССГ оказывает применение осмопротекторов. Установлено, что L-карнитин и эритрит подавляют активацию с-Jun-N-концевых киназ и митоген-активированных протеинкиназ, тем самым снижая гиперосмолярность слезной жидкости [16, 17]. L-карнитин, эритрит и бетаин оказывают значительное супрессивное действие на синтез и секрецию провоспалительных цитокинов и хемокинов, уменьшают апоптоз эпителиальных клеток. Кверцетин, эпигаллокахетин, N-пропилгаллат и галловая кислота препятствуют повреждению клеток активными формами кислорода, воздействуя на такой механизм развития ССГ, как окислительный стресс [6, 17].
Для профилактики роста микроорганизмов после вскрытия флакона с каплями многие производители включают в состав мультидозных форм слезозаменителей консерванты, известные своей токсичностью и неблагоприятным влиянием на глазную поверхность. В связи с этим отдельные фармацевтические фирмы разработали формы флаконов, препятствующие проникновению микроорганизмов внутрь флакона, исключив контаминацию раствора без применения консерванта. В настоящее время такими флаконами являются известный в России флакон системы COMOD (URSAFARM, Германия), а также Container-OSD (TRB Chemedica, Швейцария) и ABAK Bottle (Thea Pharmaceuticals, Франция). Помимо риска инфицирования и развития осложнений, связанных с применением консервантов, многоразовые флаконы с глазными каплями имеют и ряд других недостатков: их материал способен поглощать консерванты и действующие вещества (полиэтилен абсорбирует бензалкония хлорид), а красители, входящие в состав стенок флакона, могут проникать в лекарственный раствор. Для устранения этих побочных явлений отдельные производители наладили выпуск одноразовых тюбик-капельниц, содержащих дозу слезозаменителя для однократной инстилляции в оба глаза («single-dose» или «unit-dose») [18].
Бензалкония хлорид является наиболее часто используемым консервантом, входящим в состав большинства глазных капель, при этом данное вещество индуцирует апоптоз эпителиоцитов роговицы и конъюнктивы, оказывает токсическое действие на нервные окончания роговой оболочки и замедляет регенерацию повреждений роговицы. В эксперименте in vitro показано, что раствор бензалкония хлорида, превышающий концентрацию 0,005%, значительно нарушает липидный слой СП [19, 20]. Новые варианты консервантов оказывают менее губительное воздействие на глазную поверхность. Так, например, поликватерниум не оказывает детергентного действия и не разрушает липидный слой СП, благодаря чему нежелательные эффекты в отношении глазной поверхности сведены к минимуму [21]. Существует также группа окислительных консервантов, распадающихся при контакте со слезой. К ним относят перборат натрия — после инстилляции в конъюнктивальную полость консервант преобразуется в воду и кислород; а также стабилизированный оксихлорокомплекс — консервант, состоящий из хлорита, хлората натрия и диоксида хлора и распадающийся под действием света [21]. Однако необходимо отметить, что даже так называемые «исчезающие консерванты» могут оказывать некоторое негативное воздействие на глазную поверхность, поэтому предпочтительной формой слезозаменителей остаются бесконсервантные монодозные препараты [22].
Отдельную роль в составе слезозаменителей играет наличие электролитов. При ССГ их концентрация в слезной жидкости увеличивается вследствие испарения и/или недостаточной выработки слезы. Установлено, что относительно высокий уровень калия в слезной жидкости способствует защите эпителия роговицы от УФ-воздействия и поддержанию нормальной толщины роговицы. Кроме того, целостность и светорассеивающие свойства роговичного эпителия в значительной степени зависят от колебаний концентраций в слезе калия, кальция, магния, бикарбоната и хлорида натрия [6].
Биологические заменители слезы
Производство и применение биологических замени-телей слезы для лечения ССГ в настоящее время ограничено требованиями законодательства разных стран к препаратам крови, обязательным серологическим исследованием на наличие вируса иммунодефицита человека, гепатитов и других инфекций, а также коротким сроком хранения препаратов данной группы с соблюдением особого температурного режима. Однако, несмотря на указанные сложности, биологические заменители слезы имеют и ряд существенных преимуществ при лечении ССГ. Так, например, аутологичная сыворотка имеет pH, сходный с таковым слезной жидкости, а также содержит витамины и биологически активные вещества (эпителиальный фактор роста, фактор роста нервов и т. д.). Кроме того, сыворотка ингибирует высвобождение провоспалительных цитокинов, повышает количество бокаловидных клеток в конъюнктиве и стимулирует выработку муцина [23, 24]. Для применения в клинической практике на сегодняшний день разработано также много препаратов на основе тромбоцитов: обогащенная тромбоцитами плазма; плазма, обогащенная факторами роста; лизат тромбоцитов. Согласно результатам исследования J.L. Alio et al. инстилляции плазмы, обогащенной тромбоцитами, 4–6 р/сут больным ССГ способствуют уменьшению симптомов заболевания на 89% уже через 1 мес. после начала лечения [25].
Применение криоконсервированной амниотической мембраны при лечении ССГ купирует воспалительную реакцию за счет индукции апоптоза нейтрофилов и моноцитов, уменьшения инфильтрации нейтрофилами и макрофагами. Кроме того, доказана способность амниотической мембраны стимулировать регенерацию роговичных нервов благодаря присутствию фактора роста нервов [26].
Препараты, стимулирующие секрецию слезы
Еще одной группой препаратов для слезозаместительной терапии являются секретагоги — стимуляторы слезо-течения, которые доступны или находятся в стадии разработки в других странах. Существуют стимуляторы водного, муцинового и/или липидного слоев СП. Препарат Diquafosol tetrasodium (Diquas, Santen, Япония) одобрен к применению в качестве 3% офтальмологического раствора в Японии и Южной Корее. Данный препарат стимулирует водный компонент СП и секрецию муцина из эпителиальных и бокаловидных клеток конъюнктивы [27]. По данным Y.S. Byun, инстилляции Diquafosol tetrasodium способствуют эффективному заживлению эпителиальных дефектов роговицы [28]. Препарат Rebamipide (Mucosta; Otsuka pharmaceutical, Япония) в настоящее время одобрен в Японии для лечения ССГ как стимулятор муциноподобных гликопротеинов в роговичном эпителии, повышающий уровень экспрессии мукопротеинов MUC1, MUC4 и MUC16 [29, 30].
Альтернативным методом стимуляции слезопродукции при лечении ССГ является назальная нейростимуляция, основанная на усилении выработки слезной жидкости после химического или механического раздражения слизистой оболочки носовой полости с помощью специального устройства [31]. Интраназальный стимулятор TrueTear (Allergan, США) состоит из ручного блока-стимулятора с одноразовым гидрогелевым наконечником и наружного зарядного устройства. Согласно результатам клинических исследований применение интраназального стимулятора способствует значительному уменьшению симптомов сухости и раздражения глазной поверхности у больных ССГ (по данным опросника OSDI), а также улучшению показателей теста Ширмера и увеличению объема выработки слезы [32].
Противовоспалительная терапия синдрома «сухого глаза»
Консервативное лечение ССГ, особенно средней и тяжелой степени, на сегодняшний день невозможно без местной противовоспалительной терапии с назначением нестероидных противовоспалительных средств (НПВС), кортикостероидов, антиметаболитов. Однако применение препаратов данных фармакологических групп требует тщательного контроля за состоянием глазной поверхности больных ССГ в связи с риском развития осложнений (присоединение вторичной инфекции, изъязвление поверхности роговицы, транзиторное повышение офтальмотонуса, прогрессирование катаракты) [32].
В настоящее время для достижения противовоспалительного эффекта при лечении ССГ достаточно широко применяются инстилляции 0,05% раствора циклоспорина (Рестасис, Allergan, США) из группы антиметаболитов [33]. Механизм действия препарата связан с ингибированием серин/треонин фосфатазы (кальциневрин) и последующим снижением экспрессии генов, участвующих в активации Т-клеток. Следствием этого является подавление антиген-зависимой секреции активированными Т-лимфоцитами провоспалительных лимфокинов [34]. Согласно клиническим исследованиям инстилляции 0,05% раствора циклоспорина при лечении ССГ способствуют увеличению объема секретируемой слезы, повышению плотности бокаловидных клеток конъюнктивы, а также улучшают субъективные ощущения у больных, уменьшая при этом риск повреждения эпителия роговицы [35, 36].
Одно из базовых средств противовоспалительной терапии ССГ — 0,1% раствор дексаметазона фосфата, который блокирует факторы транскрипции: ядерный фактор κB и активатор белка, ингибируя тем самым транскрипцию интерлейкина-2. Помимо этого, под действием дексаметазона фосфата уменьшается число Т- и В-лимфоцитов, снижается выработка иммуноглобулинов и компонентов системы комплемента. Однако длительное применение данного препарата сопряжено с риском развития большого числа побочных эффектов. Под руководством профессора В.В. Бржеского для лечения ССГ разработан лекарственный препарат, содержащий 0,01% раствор дексаметазона фосфата, 6% раствор поливинилпирролидона и 1,5–5,5% раствор декстрозы, показавший высокую клиническую эффективность в комплексной терапии ССГ [34, 37].
Механизм действия НПВС связан с ингибированием циклооксигеназы в каскаде окисления арахидоновой кислоты, благодаря чему снижается синтез простагландинов, ответственных за развитие воспалительной реакции. Однако простагландины необходимы для синтеза белка и ДНК в эпидермальных клетках. Кроме того, НПВС, особенно при длительном местном применении, вызывают дистрофические изменения со стороны эпителия конъюнктивы и роговицы с развитием поверхностного точечного кератита. В связи с этим вопрос о целесообразности и эффективности применения препаратов данной фармакологической группы при лечении ССГ остается открытым [34, 38].
Для лечения дисфункции мейбомиевых желез как одной из основных причин ССГ многие исследователи рекомендуют системное и местное применение антибактериальных препаратов. Так, например, антибиотики тетрациклинового ряда (доксициклин) ингибируют продукцию бактериальных липаз, улучшая тем самым липидный профиль мейбомиевых масел. Местное применение азитромицина оказывает и антибактериальное, и противовоспалительное действие [39, 40].
Одним из новых препаратов с противовоспалительным действием для лечения ССГ является 5% раствор Lifitegrast (Xiidra, Novartis, Швейцария), представляющий собой функционально-ассоциированный антагонист антигена лимфоцитов-1 (Lymphocyte function-associated antigen-1, LFA-1). Препарат блокирует взаимодействие белков клеточной поверхности LFA-1 с молекулами межклеточной адгезии-1, а также ингибирует миграцию Т-клеток и высвобождение провоспалительных цитокинов при ССГ [41, 42].
В настоящее время при разработке препаратов для лечения ССГ с целью улучшения доступности лекарств используются нанотехнологии. Препаратами, изготовленными на основе данных технологий, являются KPI-121 (Kala Pharmaceuticals, США) — наночастичный препарат кортикостероида, а также лотепреднол этабонат и OTX-101 (Seciera, Sun Pharma, Индия) — наномицеллярные препараты циклоспорина и RGN-259 (ReGenTree, США) — синтетическая копия природного белка тимозина β4, который, как предполагается, способствует миграции эпителиоцитов роговицы и уменьшает выраженность воспаления [42].
Хирургические методы лечения синдрома «сухого глаза»
Хирургическое лечение ССГ проводится при тяжелых формах течения заболевания, когда фармакотерапия не позволяет достичь ожидаемого эффекта, что отрицательно сказывается на качестве жизни больного. Необходимо отметить, что оперативные вмешательства при ССГ сопряжены с риском повреждения роговицы и конъюнктивы и присоединения вторичной инфекции в послеоперационном периоде.
Одним из щадящих методов хирургического лечения заболевания является закрытие просвета слезных точек с помощью обтураторов для уменьшения оттока слезной жидкости и удержания ее на глазной поверхности. Обтураторы, состоящие из ателоколлагена — коллагена, предварительно обработанного протеазами, после установки в слезные точки превращаются в гель, который постепенно, в течение 1–16 нед. растворяется. Нерастворимые обтураторы слезных точек изготавливаются из силикона и имеют различный дизайн. Для временной окклюзии слезных точек используется также цианакрилатный клей. Кроме того, возможно проведение диатермокоагуляции нижней слезной точки. Основными осложнениями данных операций являются спонтанное выталкивание обтуратора из слезной точки и присоединение вторичной инфекции [43, 44].
Ранее, в особо тяжелых случаях ССГ с изменениями роговицы ксеротического характера, выполняли такие операции, как пересадка протока околоушной слюнной железы, трансплантация подчелюстной слюнной железы. В настоящее время указанные хирургические вмешательства выполняются довольно редко [45, 46]. К операциям, ограничивающим испаряемость слезной жидкости, относятся канторафия (ушивание век с медиального или латерального угла глазной щели) и тарзорафия (полное или частичное сшивание краев век). Также в настоящее время весьма успешно при хирургии ССГ используется биологическое покрытие роговицы с целью снижения патологического воздействия внешних факторов на глазную поверхность.
Немедикаментозные способы лечения синдрома «сухого глаза»
Соблюдение рекомендаций для исключения или минимизации воздействия внешних факторов риска, способствующих развитию и прогрессированию ССГ, позволяет существенно облегчить и/или улучшить состояние больного. Общеизвестно, что глазная поверхность наиболее подвержена воздействию ветра, низкой относительной влажности, пониженной или повышенной температуры, УФ-излучения, загрязняющих веществ, табачного дыма и др. [47–49]. На начальном этапе лечения больным ССГ рекомендуется использование увлажнителей воздуха или специальных очков для увлажнения воздуха рядом с глазом. Пользователям компьютеров и других гаджетов рекомендуется делать перерывы при зрительной работе и размещать монитор устройства ниже уровня глаз, благодаря чему уменьшается площадь открытой глазной поверхности [8].
В последние годы разработано большое количество пищевых добавок, содержащих омега-3 и омега-6 полиненасыщенные жирные кислоты (ПНЖК). Согласно научным исследованиям биодобавки с омега-3 ПНЖК способствуют повышению стабильности СП за счет модифицирования внутриклеточных липидов в слезных железах. Комбинация омега-3 и омега-6 ПНЖК также оказывает положительное влияние на качество и количество внутриклеточных липидов в мейбомиевых железах. При этом эффективность приема пероральных добавок существенно повышается, если основным компонентом добавки является омега-3 ПНЖК в отдельности или с меньшей долей омега-6 ПНЖК [50].
Заключение
На сегодняшний день существует большое число консервативных и хирургических методов лечения ССГ, применение которых позволяет облегчить течение заболевания и улучшить качество жизни больных. Выбор того или иного варианта лечения должен носить исключительно персонализированный характер, с обязательным учетом возраста больного и его рода деятельности, факторов риска и степени тяжести ССГ, наличия сопутствующих офтальмологических и системных заболеваний. При этом проводимое лечение не всегда обеспечивает достижение желаемого терапевтического эффекта с облегчением состояния больного. Поэтому поиск и разработка новых лечебно-профилактических мероприятий при лечении ССГ являются на сегодняшний день одной из актуальных проблем современной офтальмологии.
Сведения об авторах:
Татарникова Елена Борисовна — заочный аспирант кафедры офтальмологии, ORCID iD 0000-0003-3038-8117;
Кривошеина Ольга Ивановна — д.м.н., профессор, заведующая кафедрой офтальмологии, ORCID iD 0000-0001-7509-5858.
ФГБОУ ВО СибГМУ Минздрава России. 634050, Россия, г. Томск, Московский тракт, д. 2.
Контактная информация: Татарникова Елена Борисовна, e-mail: elenka.morozova.92@inbox.ru. Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах. Конфликт интересов отсутствует. Статья поступила 01.06.2020.
About the authors:
Elena B. Tatarnikova — distant postgraduate student of the Department of Ophthalmology, ORCID iD 0000-0003-3038-8117;
Olga I. Krivosheina — Doct. of Sci. (Med.), Professor, Head of the Department of Ophthalmology, ORCID iD 0000-0001-7509-5858.
Siberian State Medical University. 2, Moskovskiy tract, Tomsk, 634050, Russian Federation.
Contact information: Elena B. Tatarnikova, e-mail: elenka.morozova.92@inbox.ru. Financial Disclosure: no authors have a financial or property interest in any material or method mentioned. There is no conflict of interests. Received 01.06.2020.
КЛИНИЧЕСКАЯ МЕДИЦИНА
УДК 617.711-004.1
СОВРЕМЕННЫЕ КЛАССИФИКАЦИЯ И ФАРМАКОТЕРАПИЯ СИНДРОМА «СУХОГО ГЛАЗА»
Анисимова С.Г., Мазина Н.К., Абрамова Т.В.
ФГБОУ ВО «Кировский государственный медицинский университет» Минздрава России, Киров, Россия (610027, г. Киров, ул. К. Маркса, 112), e-mail: SvetLANa-43bk@mail.ru
В обзоре литературы проанализированы современные классификации синдрома «сухого глаза», учитывающие многофакторность заболевания. В зависимости от этиологии, механизмов и стадий развития заболевания приведены актуальные принципы лечения.
Ключевые слова: синдром «сухого глаза», слезная пленка, искусственные слезы, митохондрия.
MODERN CLASSIFICATION AND PHARMACOTHERAPY OF «DRY EYE» SYNDROME
Anisimova S.G., Mazina N.K., Abramova T.V.
Kirov State Medical University, Kirov, Russia (610027, Kirov, K. Marx Street, 112), e-mail: SvetLANa-43bk@mail.ru
The literature review analyzes the current classification of the dry eye syndrome taking into account the multifactorial nature of the disease. Some up-to-date treatment guidelines are described depending on the etiology, mechanisms and stages of the disease progression.
Key words: dry eye syndrome, tear film, artificial tears, mitochondrion.
В современном мире за последние два десятилетия достигнуты огромные успехи в лечении ССГ в связи с повышением знаний о патофизиологии заболевания [53]. Повышение знаний по диагностике и лечении ССГ обеспечивает улучшение качества жизни пациента и способствует предотвращению осложнений на ранних сроках заболевания [53].
Классификация ССГ
В 2003 году в Мадриде группой экспертов была предложена тройная классификация ССГ [54], которая позднее была модифицирована более широкой группой экспертов [55]: ССГ является многофакторным заболеванием, связанным с неадекватным взаимодействием между слезной пленкой и эпителием поверхности глаза, возникающим в результате качественных и количественных нарушений в одной или обеих структурах.
Мадридская тройная классификация с учетом многофакторности заболевания включает три крите-
рия: этиология (более 100 причин сгруппированы в 10 семейств), вид пораженных желез и тяжесть заболевания [54, 55].
На основании полиэтиологичности и многофакторности заболевания в 2002 г. В.В. Бржеский и соавт. предложили все случаи ССГ разделить на две клинические группы: синдромальный у пациентов с системными заболеваниями и симптоматический, развивающийся при анатомических изменениях глазной щели, воздействиях на роговицу и другое [2].
Клиническая классификация ССГ Е.Е. Сомова от 2002 г. включает в себя следующие проявления: хронические конъюнктивит и блефарит, их сочетания, рецидивирующие микро- и макроэрозии эпителия роговицы, сухой кератоконъюнктивит, ксероз конъюнктивы и роговицы, «нитчатый», буллезно-нитчатый кератит, кератомаляцию [10].
McCulley с соавторами предложили использовать термины ССГ: гипосекреторный и связанный с повышенным испарением [38]. В рамках конференции National Eye Institute, Bethesda были выделены две патогенетические группы ССГ [46, 43, 21]: дефицит продукции водянистого слоя из-за нарушения функции слезной железы и повышенное испарение слезной жидкости вследствие нарушения функций мейбомиевых желез.
В 2003 году в Москве профессором Г.С. Полуниным с соавторами была опубликована классификация ССГ также по этиологическому фактору: системно-органная, блефароконъюнктивальная, экзогенная, роговичная и комбинированной формы [8].
В 2007 году Международный комитет по ССГ (International Dry Eye Workshop, DEWS) выделил в развитии заболевания три основных постулата [27]:
1. Многофакторность этиологии заболевания.
2. Любые формы ССГ могут взаимодействовать и усиливать друг друга, образуя замкнутый круг. В звеньях патогенеза ССГ ведущая роль отведена гипер-осмолярности и воспалению.
3. Рациональная фармакотерапия ССГ в зависимости от тяжести заболевания.
Также Международный комитет разработал следующие классификации ССГ в зависимости от этиологии, механизмов и стадий развития заболевания [27]:
Недостаточность слезопродукции:
1. Ассоциированный с синдромом Шегрена: первичный и вторичный.
2. Неассоциированный с синдромом Шегрена: недостаточность слезы, нарушение иннервации, обструкция слезных протоков, системное влияние лекарственных препаратов.
Нарушение испарения слезной жидкости:
1. Внутренние причины: прием лекарственного препарата «Аккутан» (ретиноиды), снижение мигательных движений, нарушение формы век и разреза глазной щели, снижение мейбомиевого секрета желез.
2. Внешние причины: перенесенные заболевания передней поверхности глазного яблока (аллергические, инфекционные, вирусные), использование контактной коррекции, авитаминоз А, токсическое действие консервантов в глазных каплях.
По тяжести заболевания классификация представлена в таблице 1.
Таблица 1
Классификация ССГ по тяжести симптомов
Симптомы Степень тяжести ССГ
1 2 3 4
Дискомфорт (тяжесть и частота) Легкий, эпизодический (неблагоприятные факторы среды) Средний, эпизодический или хронический (может возникать независимо от действия неблагоприятных факторов среды) Тяжелый, частый или постоянный (независимо от действия факторов окружающей среды) Тяжелый, постоянный, значительно затрудняющий жизнедеятельность
Зрительные симптомы Нет или эпизодическая легкая усталость Эпизодические, легкие, ограничивающие деятельность Хронические и постоянные, ограничивающие деятельность Постоянные и значительно ограничивают деятельность
Инъекция конъюнктивы Нет или легкая Нет или легкая +/- +/++
Прокрашивание конъюнктивы Нет или легкое Непостоянное От умеренного до выраженного Выраженное
Тяжесть прокрашивания роговицы Нет или легкое Непостоянное Выраженное в центральной зоне Глубокие точечные эрозии
Поражение роговицы и нарушение слезной пленки Нет или легкое Включения, уменьшение слезного мениска Нитчатый кератит, нити муцина, увеличение включений Нитчатый кератит, нити муцина, увеличение включений, эрозирование
Поражение век и мейбомиевых желез Может наблюдаться дисфункция мейбомиевых желез (ДМЖ) Может наблюдаться ДМЖ Часто ДМЖ Трихиаз, ороговение, симблефарон
Время разрыва слезной пленки Непостоянное < 10 с < 5 с Незамедлительно
Проба Ширмера Непостоянная <10 мм/5 мин < 5 мм/5 мин <2 мм/5 мин
Таким образом, анализируя вышеизложенные классификации, ССГ является интегрированной патологией слезной пленки, век и поверхности глаза.
Современная фармакотерапия ССГ
Клиническая классификация ССГ отражает многообразие этиологических и патогенетических факторов, следовательно, проводимое лечение должно быть направлено на следующие аспекты:
1. Минимизация избыточного процесса испарения, гиперосмолярности.
2. Стабилизирование слезной пленки.
3. Предотвращение и лечение повреждений роговицы.
4. Стимулирование железистой секреции.
5. Повышение качества и объема слезной пленки.
6. Предотвращение воспалительного процесса
[33].
Современные подходы к лечению ССГ включают использование актуальных смазочных материалов (искусственные слезы или биологические заменители), системных антибиотиков (тетрациклин, доксициклин, миноциклин), актуальной противовоспалительной терапии (например, кортикостероиды или иммуномодуляторы, циклоспорин), диеты (употребление омега-3 жирных кислот), а также стимуляторов секреции (например, холинергические препараты) [32]. Кроме фармакологической коррекции заболевания важна роль контроля внешних факторов (например, влажность, электромагнитное излучение, дым, смог) [32].
По мнению Д.Ю. Майчука, комплексное лечение ССГ должно включать 3 аспекта [5]: обязательная противовоспалительная терапия, искусственные слезы, построение алгоритма патогенетической терапии на основе клинической картины ССГ.
Наиболее полно лечение было представлено на Международном комитете (DEWS) в 2007 году в зависимости от тяжести заболевания [27].
Искусственные слезы (смазывающие препараты)
При использовании только монотерапии искусственными слезами наблюдается снижение симптомов проявления ССГ, но они не могут быть полностью устранены [20].
Искусственные слезы должны обладать следующими свойствами:
1. Гипотонические или изотонические растворы, содержащие электролиты (калий, бикарбонаты), поверхностно-активные вещества, различные вязкие агенты.
2. В идеале не должны содержать консерванты.
3. Нейтральная или слабощелочная рН.
4. Осмолярность раствора должна составлять 181-354 мосмоль/л [42].
Электролиты или ионы зарекомендовали себя в лечении ССГ, например, калий участвует в поддержании равномерной толщины роговицы, эпителия, а гидрокарбонаты — муцина [25].
У пациентов с ССГ наблюдается гиперосмо-лярность (коллоидная осмолярность) слезы, которая вызывает биохимические и морфологические изме-
нения в эпителии. Таким пациентам рекомендованы слезы с гипоосмолярностью [35]. К таким искусственным слезам относятся Hypotears® (230 мосм/л (Novartis Ophtalmics, СЩА) и TheraTears® (181 мосм/л, Advanced Vision, США).
В составе слез в различных концентрациях используют поливиниловый спирт, полиэтиленгликоль, гликоль 400, пропиленгликоль и гидроксипропилцел-люлозу. Но все высоковязкие агенты имеют свойство насыхать на ресницах, вызывают косметический дискомфорт и пациент может отказаться от лечения. Для решения этой проблемы стали использовать препараты с агентами низкой вязкости. К таким агентам относится гидроксипропил-гуар, который добавлен в качестве гелеобразующего агента в раствор, содержащий гликоль 400 и пропиленгликоль, способного связываться с гидрофобными поврежденными участками, обеспечивая им временную защиту [18,19]. К этой группе относится препарат Систейн® (Alcon, США). Во флаконе глазные капли с pH 7.0 находятся в виде жидкости, после инстилляции в конъюнкти-вальную полость, где pH 7.5-7.8, преобразуется в гель, равномерно покрывая поверхность глаза.
Одним из активных компонентов выделена также гиалуроновая кислота 0,2%, которая себя положительно зарекомендовала в исследованиях [39]. Натриевая соль гиалуроновой кислоты является природным мукополисахаридом, гликозаминогликаном, обладающим мукомиметическим, репаративным и отчасти противовоспалительным эффектом [15]. Ре-паративное действие проявляется стимулированием регенерации эпителия роговицы и конъюнктивы за счет вовлечения в репаративный процесс рецептора натрия гиалуроната — молекулы СD44 [15]. Количество данного рецептора увеличивается с тяжестью ССГ [15]. Гиалуронат натрия редуцирует экспрессию СD44 выраженнее, чем карбоксиметилцеллюлоза [45]. В искусственных слезах используется в виде натриевой соли (натрия гиалуроната), в водной среде преобразуется в вязкий гель.
К таким препаратам относятся Хило-комод® (Ursapharm, Германия) и Вид-Комод® (Ursapharm, Германия). Отличительной особенностью Хило-ко-мода® является отсутствие консерванта, поэтому данный препарат можно применять и у пациентов с ССГ аллергического генеза. Вид-комод® содержит поливинилпиролидон, обладающий необходимой вязкостью и хорошими адгезивными свойствами по отношению к передней поверхности глаза [7].
На основе гиалуроновой кислоты созданы препараты Артелак Всплеск® и Артелак Баланс® (Baush & Lomb, Германия). Артелак Всплеск содержит 0,24% гиалуроновой кислоты, которая, связываясь с молекулами воды, быстро восстанавливает слезную пленку и показан при лечении транзиторного ССГ [3]. Артелак Баланс®, имеющий в составе 0,15% гиа-луроновой кислоты и витамин В12, обладающий ан-тиоксидантным действием, рекомендован при легкой и умеренной форме ССГ. Его применение приводит к уменьшению субъективных жалоб, понижению гипер-осмолярности и воспаления [59].
К этой группе относится препарат Оксиал® (Baush & Lomb, Германия), содержащий 0,15% гиа-луроновой кислоты, и показан для лечения ССГ хронической формы у лиц старше 55 лет [3].
Одной из новых разработок в улучшении муци-нового слоя слезной пленки является применение по-
лисахарида семян тамаринда, получаемого из семян растения Таmаrindus тйтса [22]. Компонентом семян является беззарядный нейтральный полисахарид, состоящий из основной (напоминающий целлюлозу) и боковых цепей (ксилоза и галактоксилоза) [22]. Наличие разветвленной структуры схоже со строением трансмембранных белков муцинового слоя слезной пленки с осмолярностью 300 мосм/кг, близкой к ос-молярности слезной пленки. Полисахарид также обладает способностью повышать свою вязкость с ростом рН, что в свою очередь увеличивает пребывание его на поверхности глазного яблока. К этой группе относится препарат Визин Чистая слеза® (Pfizer, США).
Ряд авторов отмечают, что искусственные слезы на гелевой основе обладают пролонгированным действием, формируя более устойчивую слезную пленку на поверхности роговицы [11]. Такими препаратами являются Офтагель (Santen, Финляндия), Видисик (Baush & Lomb, Германия), Систейн (Alcon, США), Хило-комод (Ursapharm, Германия) и Вид-Комод (Ursapharm, Германия).
Основным компонентом Офтагеля (Santen, Финляндия) является карбомер 974Р, 2,5 мг/г, относящийся к группе химически инертных нерастворимых и нетоксичных акриловых полимеров, который связывает воду на поверхности роговицы, компенсируя муциновый слой [11].
Основой препарата Видисик (Baush & Lomb, Германия) является полиакриловая кислота, которая при смыкании век преобразуется в жидкую фазу, а при открытых веках cтруктурируется в гелевую. Таким образом, создавая коллоидную систему, полиакриловая кислота способна изменяться под действием механических сил [11].
Таким образом, искусственные слезы достаточно эффективны в лечении ССГ. Выбор слезозаменителя производится путем пробных инстилляций препаратов в течение 2-3-х суток. Пациент самостоятельно, руководствуясь субъективными симптомами, определяет наиболее приемлемые для него капли и частоту их инсталляций. Жалобы, возникшие вновь, купируют последовательной инстилляцией препарата. Но следует иметь в виду, что частые (свыше 5 раз в день) инстилляции слезозаменителей способствуют вымыванию из конъюнктивальной полости нативной слезы.
Противовоспалительная терапия
Гиперосмолярность слезной жидкости при ССГ стимулирует выработку медиаторов воспаления, приводящих к дисфункции продуцирующих компонентов слезы клеток или их значительному сокращению с развитием «порочного» круга в патогенезе заболевания [36, 40].
Во многих масштабных исследованиях показана эффективность применения в лечении воспаления при ССГ селективного иммуносупрессивного препарата циклоспорина в различных лекарственных формах [51, 49]. При инстилляции эмульсии 0,05% отмечается улучшение субъективных симптомов, а при 0,1% — объективных. Исследования показали, что при применении циклоспорина А наблюдается увеличение плотности бокаловидных клеток до 200%. Кроме этого наблюдалось снижение экспрессии иммунных маркеров воспаления (HLA-DR), маркеров апоптоза клеток (FAS-зависимого апоптоза) и провоспали-тельного цитокина ИЛ-6 со стороны эпителиальных клеток конъюнктивы [17, 57]. При этом также наблю-
дается снижение инфильтрации желез лимфоидными клетками [31, 47].
Кортикостероиды также обладают противовоспалительным эффектом в лечении ССГ. В исследованиях лечения ССГ в комплексной терапии с добавлением кортикостероидов (метилпреднизолон или фторметалон плюс) в сравнении с искусственными слезами и обтурацией слезных каналов отмечалось снижение жалоб на раздражение роговицы и инструментально уменьшение зон прокрашивания роговицы флюоресцеином без побочных стероидных эффектов [13, 48]. В.В. Бржеский с соавторами в своих исследованиях показали клиническую эффективность применения 0,01% дексаметазона в сочетании с «гемодезом» [1]. Авторы рекомендуют инстилля-ции 0,05% раствора дексаметазона при наличии воспалительного процесса, фолликулярного конъюнктивита [1]. Кортикостероиды переносятся пациентами намного лучше, чем нестероидные противовоспалительные препараты [1].
Системные антибиотики из группы тетрацикли-нов (миноциклин, доксициклин) обладают тремя важными свойствами в лечении ССГ: антибактериальное, противовоспалительное, антиангиогенное. Антибактериальное свойство проявляется в бактерицидном действии за счет подавления синтеза белка, ингибиро-вания липазы, что способствует нормализации микрофлоры, улучшению состава мейбомиевого секрета [50]. Это свойство тетрациклинов, в частности док-сициклина, благотворно сказывается в лечении мей-бомиевого блефарита [50]. Противовоспалительное действие тетрациклинов проявляется в способности снижать активность коллагеназы, фосфолипазы А2, металлопротеиназы, интерлейкина-1и альфа-1 — фактора некроза опухоли [34]. Антиангиогенные свойства тетрациклинов проявились в купировании новообразования кровеносных сосудов в исследованиях на роговицах кроликов (миноциклин) [26]. Это в будущем будет иметь клиническое значение при таких заболеваниях, как розацеа и опухолевые процессы [58].
Препараты, стимулирующие секрецию
Ограничением к применению данной категории препаратов служит недостаток резервных возможностей слезопродукции.
К таким препаратам относится агонист P2Y2 рецепторов Диквафосол (разрешен к применению в Японии и Южной Корее), стимулирующий секрецию водного и муцинового компонентов слезной пленки [52]. Также в 2015 г. было доказано, что Диквафосол на 3% эффективнее улучшает состояние роговицы (по данным пробы с флюоресцеином, теста Ширме-ра, времени разрыва слезной пленки), чем гиалуронат натрия при той же частоте побочных эффектов [30, 29], но при их комбинации лечебный эффект выше, чем в отдельности [56].
Стимуляцией слезопродукции также обладают М-холиномиметик пилокарпин в дозе 5 мг перораль-но у пациентов с синдромом Шегрена. У таких пациентов наблюдалось улучшение состояния роговицы, но нарушалась рефракция в результате побочного эффекта в виде миоза и наблюдалась повышенная потливость [41, 44].
Стимуляция слезопродукции осуществляется также путем местного или системного использования препаратов, улучшающих микроциркуляцию конъюнктивы или слезной железы. Так, двухстороннее лимфотропное введение в течение 8 дней лекар-
ственной смеси, состоящей из 1,0 мл трентала и 2% раствора лидокаина, в точку на 1,0 см ниже и 1,0 см медиальнее вершины сосцевидного отростка, богатой лимфатическими узлами, приводит к купированию хронической ишемии и гипоксии. Тем самым увеличивается слезопродукция и состояние глазной поверхности [4].
Выявлено, что эффективными методами стимуляции продукции слезы при гиполакримии умеренной и значительной степеней выраженности являются системный прием пентоксифиллина и прямое или чрезкожное облучение сводов коньюнктивы гелий-неоновым лазером или их комбинация [6].
Биологические заменители слезной жидкости
В качестве заместителей слезы могут использоваться аутосыворотка, сыворотка пуповинной крови, а также секрет слюнных желез [23, 24].
Незаменимые жирные кислоты не могут синтезироваться самостоятельно в организме, поступают с пищей. Омега-6 жирные кислоты являются прекурсором арахидоновой кислоты и некоторых про-воспалительных медиаторов липидов (PGE2 и ЦГВ4) [28]. Омега-3 жирные кислоты (ЕРА в рыбьем жире) ингибируют синтез этих липидных медиаторов и образование ИЛ-1 и альфа-ФНО [28]. В исследованиях для улучшения состояния глазной поверхности рекомендуют прием перорально 2 раза в день линолевую и гамма-линолевую кислоты [14].
Таким образом, ССГ у каждого пациента имеет свои причины и свою индивидуальную патологию. В зависимости от тяжести заболевания на Международном подкомитете в 2007 году предложена следующая схема лечения [20, 37, 16]:
Уровень 1 (степень тяжести 1): Коррекция питания и действия неблагоприятных факторов среды, учитывая санитарно-гигиенические и образовательные нормы, устранение системных побочных эффектов при приеме лекарственных препаратов, применение слезозаменителей (капли, мази, гели), гигиена век.
Уровень 2 (степень тяжести 2, при неэффективности уровня 1): Слезозаменители без консервантов, противовоспалительные средства, применение антибиотиков тетрациклинового ряда (мейбомиит или ро-зацеа), окклюзия слезных точек при отсутствии воспаления, стимуляция секреции, применение очков с увлажняющей камерой.
Уровень 3 (степень тяжести 3, при неэффективности уровня 2): Применение препаратов аутосыво-роток, контактные лечебные линзы, постоянная обту-рация слезных точек.
Уровень 4 (степень тяжести 4, при неэффективности уровня 3): Системные противовоспалительные средства, хирургическое лечение.
iНе можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
В зависимости от классификации ССГ по этиологическому фактору профессором Г.С. Полуниным с соавторами предложены следующие схемы лечения [8].
1. Этиотропное лечение системно-органной формы ССГ: основная терапия (цитостатики, аминохино-линовые препараты), антибактериальные препараты (тобрекс, флоксал, нормакс и др.), противовоспалительная терапия (нестероидные противовоспалительные средства: наклоф, диклоф; кортикостероиды: дексаметазон и др.), десенсибилизирующая терапия (глюконат кальция + аскорбиновая кислота и др.); эфферентная терапия (гемосорбция, плазмаферез), репа-ративная восстанавливающая терапия (Корнерегель, Хилозар-Комод, ВитА-ПОС и др.).
2. Этиотропное лечение блефароконъюнкти-вальной формы ССГ: гигиена век (Блефаролосьон, Блефарогели 1 и 2), противовоспалительные и антисептические препараты (Тобрекс, Окуметил, Фуци-талмик, Флоксал и др.), антигистаминная терапия (Лекролин, Аллергодил и др.), физиолечение (маг-нитофорез, фонофорез, электрофорез), репаративная терапия (Корнерегель, Хилозар-Комод, ВитА-ПОС и
др.) [9].
3. Лечение роговичной формы ССГ: противовоспалительная: нестероидная терапия (Неванак, На-клоф, Диклофенак и др.), кортикостероидная терапия (Дексаметазон и др.), антибактериальная терапия (Тобрекс, Флоксал и др.), десенсибилизирующая терапия (Супрастин, Тавегил и др.), репаративная восстанавливающая терапия (Корнерегель, Хилозар-Ко-мод, ВитА-ПОС и др.).
4. Лечение экзогенной формы ССГ: репаративная восстанавливащая терапия (Корнерегель, Хило-зар-Комод, ВитА-ПОС и др.), средства для гигиены век (Блефаролосьон, Блефарогель 1, Блефарогель 2).
5. Лечение комбинированной формы ССГ.
Лечение пациентов с комбинированной формой
ССГ проводится с учетом каждого компонента, вызывающего ССГ.
Для профилактики и лечения ССГ разрабатываются методы системной фармакологической регуляции полноценной слезопродукции и восстановления клеток роговицы и конъюнктивы. Новое направление фармакологии — биоэнергетическая фармакология, которая изучает и разрабатывает способы медикаментозной коррекции нарушенных функций органов и систем через влияние на активность клеточных систем энергопродукции — митохондрий (МХ). В настоящее время основными средствами, регулирующими функции МХ органов и тканей, вовлеченных в патологический процесс, являются регуляторы энергетического обмена (РЭО), содержащие субстраты цикла трикарбоновых кислот (янтарную, глутаминовую, яблочную кислоты и их соли), или их композиции с кофакторами биологического окисления, биофла-воноидами. Для энерготропной фармакологической коррекции функций органа зрения применяются РЭО, содержащие янтарную кислоту (ЯК) [12].
Фармакологические регуляторы энергетического обмена оказывают следующие эффекты на организм в целом: повышение неспецифической резистентности организма и его систем, антистрессорный, антиишемический, иммуномодулирующий, цитопро-текторный, антигипоксический, антитоксический, антиоксидантный, антиацидотический (метаболический ацидоз), повышение фармакотерапии заболевания, снижение побочных эффектов лекарств [12]. В связи с этим для повышения клинико-экономической эффективности схем фармакотерапии распространенных заболеваний рекомендуется дополнительное применение препаратов, содержащих янтарную кислоту, в дозах, рекомендованных производителем [12]. Доказано, что применение препаратов янтарной кислоты до 40% повышает клиническую эффективность фармакотерапии основного заболевания, обеспечивая существенный фармакоэкономический эффект в виде снижения коэффициента «затраты-эффективность».
Таким образом, разработка препаратов, увеличивающих продукцию собственной слезы, является более перспективным и физиологичным направлением фармакотерапии. Дальнейший прогресс в рас-
сматриваемой области связан с внедрением лекарств, стимулирующих и сохраняющих нативную слезу без использования инвазивных методов лечения, которые были бы ориентированы на различные патогенетические типы ССГ и вдобавок обладали ресурсосберегающими свойствами и клинико-экономической эффективностью.
Список литературы
1. Бржеский В.В., Астахов Ю.С., Кузнецова Н.Ю. Заболевания слезного аппарата // Пособие для практикующих врачей. Санкт-Петербург, 2009. 108 с.
2. Бржеский В.В., Сомов Е.Е. Роговично-конъ-юнктивальный ксероз (диагностика, клиника, лечение). СПб.: «Сага». 2002. 142 с.
3. Егоров Е.А. Гиалуроновая кислота: применение в офтальмологии и терапии синдрома «сухого глаза» // Научно-клиническое рецензионное издание «Клиническая офтальмология». 2013. № 2. С. 71-73.
4. Еременко А.И., Янченко С.В. Возможности использования лимфотропной терапии в лечении синдрома «сухого глаза» // РМЖ «Клиническая офтальмология». 2010. № 1. С. 20.
5. Майчук Д.Ю. Патогенетическое обоснование лечения и профилактики вторичных нарушений слезообразования: автореф. дис. … д-ра мед. наук. Москва, 2005. 76 с.
6. Матевосова Э.А. Возможности стимуляции секреции слезы у больных с гиполакримией при синдроме «сухого» глаз // автореферат дис….кан.мед. наук. Москва. 2009. 24 с.
7. Мосунова Е.П., Абрамова Т.В. Опыт применения раствора Хило-комод фирмы Урсафарм при синдроме «сухого глаза» в Кировской областной клинической больнице // Новое в офтальмологии. 2010. № 2. С. 34-35.
8. Полунин Г.С., Сафонова Т.Н., Полунина Е.Г. Новая клиническая классификация синдрома сухого глаза// Рефракционная хирургия и офтальмология. 2003. № 3. С. 53-56.
9. Полунин Г.С., Каспарова Е. А., Полунина Е.Г., Забегайло А. Блефариты // Медицинская газета. 2007. № 31. С. 9.
10. Сомов Е. Е. Бржеский В.В. Краткое руководство по обследованию и лечению больных с синдромом «сухого глаза» // Руководство для врачей. Санкт-Петербург: Вель. 2003. 32 с.
11. Фалхут О.С., Полунина Е.В. Рациональный подход в диагностике и лечении синдрома «сухого глаза» // Медицинский совет. 2010. № 5-6. С.100-104.
12. Шешунов И.В., Мазина Н.К., Хазанов В.А., Мазин П.В. Фармако-экономические эффекты регуляторов энергетического обмена как фактор улучшения качества медицинской помощи // Экономика здравоохранения. 2006. № 12. С. 39-46.
13. Avunduk A.M., Avunduk M.C., Varnell E.D., Kaufman H.E. The comparison of efficacies of topical corticosteroids and nonsteroidal anti-inflammatory drops on dry eye patients: A clinical and immunocytochemical study // Am J Ophthalmol. 2003. № 136. Р. 593-602.
14. Barabino S., Rolando M,. Camicione P., [et al.] Systemic linoleic and gammalinolenic acid therapy in dry eye syndrome with an inflammatory component // Cornea. 2003. № 22. Р. 97-101.
15. Baudouin C. The pathology of dry eye // Surv Ophthalmol. 2001. Vol. 45. Suppl. 2. Р. 211-220.
16. Behrens A., Doyle J.J., Stern L., et al. Dysfunctional tear syndrome: A Delphi approach to treatment recommendations // Cornea 2006. № 25. P. 900-907.
17. Brignole F., Pisella P.J., De Saint Jean M., [et al.] Flow cytometric analysis of inflammatory markers in KCS: 6-month treatment with topical cyclosporine A // Invest Ophthalmol Vis Sci. 2001. № 42. P. 90-95.
18. Christiansen M., Cohen S., Rinehart J., [et al.] Clinical evaluation of an HP -guar gellable lubricant eye drop for the relief of dryness of the eye// Curr Eye Res. 2004. Vol. 28. P. 55-62.
19. Di Pascuale M.A., Goto E., Tseng S.C. Sequential changes of lipid tear film after the instillation of a single drop of a new emulsion eye drop in dry eye patients // Ophthalmology. 2004. Vol. 111. P. 783-791.
20. Dry Eye Workshop Management and therapy of dry eye disease: Report of the Management and Therapy Subcommittee of the International Dry Eye Workshop// Ocul Surf. 2007. Vol. 5, № 2. P. 163-178.
21. Foulks G.N. Treatment of dry eye disease by the non-ophthalmologist // Rheum Dis Clin North Am. 2008. Vol. 34, № 4. P. 987-1000.
22. Gayton J. L. Etiology, prevalence, and treatment of dry eye disease // Clin Ophthalmol. 2009. Vol. 3. P. 405-412.
23. Geerling G., Daniels J.T., Dart J.K., [et al.] Toxicity of natural tear substitutes in a fully defined culture model of human corneal epithelial cells// Invest Ophthalmol Vis Sci. 2001. P. 42948-42956.
24. Geerling G., Honnicke K., Schroder C., [et al.] Quality of salivary tears following autologous submandibular gland transplantation for severe dry eye // Graefes Arch Clin Exp Ophthalmol. 2000. № 238. P. 45-52.
25. Green K., MacKeen D.L., Slagle T., Cheeks L. Tear potassium contributesto maintenance of corneal thickness // Ophthalmic Res 1992. Vol. 24. P. 99-102.
26. Habif T.P. Clinical dermatology, 4th ed // St Louis:Mosby-Year Book. 2004. P. 162-189.
27. International Dry Eye Workshop. The definition and classification of dry eye disease: Report of the Definition and Classification Subcommittee of the International Dry Eye Workshop//Ocul Surf. 2007. Vol. 5, № 2. P. 75-92.
28. JamesM.J., Gibson R.A., ClelandL.G. Dietary polyunsaturated fatty acids and inflammatory mediator production // Am J Clin Nutr. 2000 №71(1 Suppl). P. 343-348.
29. Kamiya K., Nakanishi M., Ishii R., Kobashi H., Igarashi A., Sato N., Shimizu K. Clinical evaluation of the additive effect of diquafosol tetrasodium on sodium hyaluronate monotherapy in patients with dry eye syndrome: a prospective, randomized, multicenter study//Eye (Lond). 2012. № 26, Vol. 10. P. 1363-1368.
30. Keating G.M. Diquafosol ophthalmic solution 3 %: a review of its use in dry eye // Drugs. 2015. № 75, Vol. 8. P. 911-922.
31. Kunert K.S., Tisdale A.S., Stern M.E., Smith J.A. Analysis of topical cyclosporine treatment of patients with dry eye syndrome: effect on conjunctival lymphocytes // Arch Ophthalmol. 2000. № 118. P. 14891496.
32. LempM.A. Management of dry eye disease// Am J Manag Care. 2008. Vol. 14, № 3 (Suppl). P. 88-101.
33. Lemp M.A., Foulks G.N., Devgan U., Trattler W.B., Nichols K.K. The therapeutic role of lipids:
Managing ocular surface disease// Refractive Eyecare for Ophthalmologists. 2005. Vol. 9 (Suppl). P. 3-15.
34. Li D.Q., Luo L., Chen Z., [et al.] JNK and ER K MAP kinases mediate induction of IL -lbeta, TNF-alpha and IL -8 following hyperosmolar stress in human limbal epithelial cells // Exp Eye Res. 2006. № 82. P. 588-596.
35. Luo L., Li D., Corrales R., Pflugfelder S. Hyperosmolar saline is a proinflammatory stress on the mouse ocular surface// Eye Contact Lens 2005. Vol. 31. p. 186-193.
36. Luo L., Li D.Q., Doshi A., [et al.] Experimental dry eye stimulates productionof inflammatory cytokines and MMP-9 and activates MAP K signaling pathways on the ocular surface // Invest Ophthalmol Vis Sci. 2004. № 45. P. 4293-4301.
37. Matoba A.Y., HarrisD.J., MarkD.B., [etal.]Dry eye syndrome, American Academy of Ophthalmology. 2003.
38. McCulley J.P., Shine W.E., Aronowicz J. [et al.] Presumed Hyposecretory/Hyperevaporative KCS: Tear Characteristics// Trans Am Ophthalmol Soc. 2003. Vol. 101. P. 141-154.
39. Nelson J.D., Farris R.L. Sodium hyaluronate and polyvinyl alcohol artificial tear preparations a comparison in patients with keratoconjunctivitis sicca // Arch Ophthalmol. 1988. Vol. 106. P. 484-487.
40. Niederkorn J.Y., Stern M.E., Pflugfelder S.C., [et al.] Desiccating stress induces T cell-mediated Sjogren’s syndrome-like lacrimal keratoconjunctivitis // J Immunol. 2006. № 176. P. 3950-3957.
41. Papas A.S., Sherrer Y.S., Charney M., [ et al.] Successful treatment of dry mouth and dry eye symptoms in Sjogren’s syndrome patients with oral pilocarpine: A randomized, placebo-controlled, dose-adjustment study// J Clin Rheumatol. 2004. № 4. P. 169-177.
42. Perrigan D.M., Morgan A., Quintero S., [et al.] Comparison of osmolarity values of selected ocular lubricants // AR VO 2004 poster session 449.
43. Perry H.D. Dry eye disease: Pathophysiology, classification, and diagnosis // Am J Manag Care. 2008. Vol. 4, № 3 Suppl. P. 79-87.
44. Petrone D., Condemi J.J., Fife R., [et al.] Double-blind randomized placebocontrolled study of cevimeline in Sjogren’s syndrome patients with xerostomiaand keratoconjunctivitis sicca // Arthritis Rheum. 2002. № 46. P. 748-754.
45. Pflugfelder S. C., Solomon A. Dry eye // Ocular surface disease / Ed. by. — E. J. Holland, M. J. Mannis, Springer. New York. 2001. P. 49-57.
46. Pflugfelder S. C., Solomon A. Dry eye A. / Ocular surface disease // Ed. by. — New York. 2001. P. 49-57.
47. Pflugfelder S.C., Maskin S.L., Anderson B., [et al.] A randomized, doublemasked, placebo-controlled, multicenter comparison of loteprednol etabonate ophthalmic suspension, 0.5%, and placebo for treatment of keratoconjunctivitis sicca in patients with delayed tear clearance // Am J Ophthalmol. 2004. № 138. P. 444-457.
48. Sainz de la Maza Serra S.M., Simon Castellvi C., Kabbani O. Nonpreserved topical steroids and punctal occlusion for severe keratoconjunctivitis sicca// Arch Soc Esp Oftalmol. 2000. № 75. P. 751-756.
49. Sall K., Stevenson O.D., Mundorf T.K., Reis B.L. Two multicenter, randomized studies of the efficacy and safety of cyclosporine ophthalmic emulsion in moderate to severe dry eye disease // Ophthalmology. 2000. № 107. P. 631-639.
50. Shine W.E., McCulley J.P., Pandya A.G. Minocycline effect on Meibomian gland lipids in meibomianitis patients // Exp Eye Res. 2003. № 76. P. 417-420.
51. Stevenson D., Tauber J., Reis B.L. Efficacy and safety of cyclosporin A ophthalmic emulsion in the treatment of moderate-to-severe dry eye disease. A doseranging, randomized trial // Ophthalmology. 2000. № 107. P. 967-974.
52. Tauber J., Davitt W.F., Bokosky J.E., [et al.] Double-masked, placebo-controlled safety and efficacy trial of diquafosol tetrasodium (INS365) ophthalmic solution for the treatment of dry eye// Cornea. 2004. № 23. p. 784-792.
53. The Epidemiology of dry eye disease: report of the Epidemiology Subcommittee of the International Diy Eye Workshop / Ocul Surf. 2007. Vol. 5, № 2. P. 174.
54. The Madrid Triple Classification of Dry Eye / J. Murube [et al.] // Arch. Soc. Esp. Oftalmol. 2003. Vol. 78., № 11. P. 587-594.
55. The triple classification of dry eye for practical clinical use / J. Murube [et al.] // Eur. J. Ophthal. 2005. Vol. 15. P. 660-667.
56. Toda I., Ide T., Fukumoto T., Ichihashi Y., Tsubota K. Combination therapy with diquafosol tetrasodium and sodium hyaluronate in patients with dry eye after laser in situ keratomileusis//Am J Ophthalmol. 2014. № 157, Vol. 3. P. 616-622.
57. Turner K., Pflugfelder S.C., Ji Z., [et al.] Interleukin-6 levels in the conjunctival epithelium of patients with dry eye disease treated with cyclosporine ophthalmic emulsion// Cornea. 2000. №19. p.492-496.
58. Velicer C.M., Heckbert S.R., Lampe J.W., [et al.] Antibiotic use in relation to the risk of breast cancer // JAMA. 2004. № 291. P. 827-835.
59. Versura P., Profazio V., Giannaccare G., Fresina M., Campos E.C. Discomfort symptoms reduction and ocular surface parameters recovery with Artelac Rebalance treatment in mild-moderate dry eye // Eur J Ophthalmol. — 2013. №23, Vol. 4. P. 488-495.
References
1. Brzheskii V.V., Astakhov Y. S., Kuznetsova N. Yu. Zabolevaniya sleznogo apparata. Posobie dlya praktikuyushchikh vrachey (Diseases of the lacrimal apparatus. A Handbook for practitioners). Saint-Petersburg, 2009. 108 p.
2. Brzheskii VV, Somov E.E. Rogovichno-kon»yunktival’nyykseroz (diagnostika, klinika, lechenie) [Corneal conjunctival xerosis (diagnostics, clinic, treatment)]. SPb, Saga Publ., 2002. 142 p.
3. Egorov E. A., Nauchno-klinicheskoe retsenzionnoe izdanie «Klinicheskaya oftal’mologiya», 2013, no. 2, pp. 71015073.
4. Eremenko A. I., Yanchenko S. V., RMZh «Klinicheskaya oftal’mologiya», 2010, no. 1, p. 20.
5. Maychuk D.Yu. Patogeneticheskoe obosnovanie lecheniya i profilaktiki vtorichnykh narusheniy slezoobrazovaniya. Avtoreferat diss. doktora med. nauk [Pathogenetic substantiation of the treatment and prevention of secondary disorders of tear production. Abstract of Diss. Dr. med. Sciences]. Moskow, 2005, 76 p.
6. Matevosova E.A. Vozmozhnosti stimulyatsii sekretsii slezy u bol’nykh s gipolakrimiey pri sindrome «sukhogo» glaza. [The possibility of stimulating the secretion of tears in patients with hyponatremia in the syndrome of «dry» eye]. Abstract of Diss. Cand. of med. Sciences. Moskow, 2009, 24 p.
7. Mosunova, E. P., Abramova T. V, Novoe v oftal’mologii, 2010, no. 2, pp. 34-35.
8. Polunin G. S., Safonova T. N., Polunina E. G.,
Refraktsionnaya khirurgiya i oftal’mologiya, 2003, no. 3, pp. 53-56.
9. Polunin G. S., Kasparova E. A., Polunina E. G., Meditsinskaya gazeta, 2007, no. 31, P. 9.
10. Somov E. E., Brzheskii VV Kratkoe rukovodstvo po obsledovaniyu i lecheniyu bol’nykh s sindromom «sukhogo glaza». Rukovodstvo dlya vrachei [A quick guide to examination and treatment of patients with dry eye syndrome» // Manual for doctors]. Saint Petersburg, Vel Publ., 2003. 32 p.
11. Falgout O. S., Polunina E. V., Meditsinskiy sovet, 2010, no. 5-6, pp. 100-104.
12. 12 Sheshunov I. V., Mazina N. K., Khazanov V. A., Mazin P. V., Ekonomika zdravookhraneniya, 2006, no. 12, pp. 39-46.
13. Avunduk A.M., Avunduk M.C., Varnell E.D., Kaufman H.E. The comparison of efficacies of topical corticosteroids and nonsteroidal anti-inflammatory drops on dry eye patients: A clinical and immunocytochemical study. Am J Ophthalmol. 2003. No136. pp. 593-602.
14. Barabino S., Rolando M., Camicione P., [et al.] Systemic linoleic and gammalinolenic acid therapy in dry eye syndrome with an inflammatory component. Cornea. 2003. № 22. pp. 97-101.
15. Baudouin C. The pathology of dry eye. Surv Ophthalmol. 2001. Vol. 45. Suppl. 2. pp. 211-220.
16. Behrens A., Doyle J.J., Stern L., et al. Dysfunctional tear syndrome: A Delphi approach to treatment recommendations. Cornea. 2006. No 25. pp. 900-907.
17. Brignole F., Pisella P.J., De Saint Jean M., [et al.] Flow cytometric analysis of inflammatory markers in KCS: 6-month treatment with topical cyclosporine A. Invest Ophthalmol Vis Sci. 2001. № 42. pp. 90-95.
18. Christiansen M., Cohen S., Rinehart J., [et al.] Clinical evaluation of an HP -guar gellable lubricant eye drop for the relief of dryness of the eye. Curr Eye Res. 2004. Vol. 28. pp. 55-62.
19. Di Pascuale M.A., Goto E., Tseng S.C. Sequential changes of lipid tear film after the instillation of a single drop of a new emulsion eye drop in dry eye patients. Ophthalmology. 2004. Vol. 111. pp. 783-791.
20. Dry Eye Workshop Management and therapy of dry eye disease: Report of the Management and Therapy Subcommittee of the International Dry Eye Workshop. Ocul Surf. 2007. Vol. 5, No 2. pp.163-178.
21.Foulks G.N. Treatment of dry eye disease by the non-ophthalmologist. Rheum Dis Clin North Am. 2008. Vol. 34, № 4. pp. 987-1000.
22. Gayton J. L. Etiology, prevalence, and treatment of dry eye disease. Clin Ophthalmol. 2009. Vol. 3. pp. 405-412.
23. Geerling G., Daniels J.T., Dart J.K., [et al.] Toxicity of natural tear substitutes in a fully defined culture model of human corneal epithelial cells. Invest Ophthalmol Vis Sci. 2001. pp. 42948-42956.
24. Geerling G., Honnicke K., Schroder C., [et al.] Quality of salivary tears following autologous submandibular gland transplantation for severe dry eye. Graefes Arch Clin Exp Ophthalmol. 2000. № 238. pp. 45-52.
iНе можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
25. Green K., MacKeen D.L., Slagle T., Cheeks L. Tear potassium contributesto maintenance of corneal thickness. Ophthalmic Res. 1992. Vol. 24. pp. 99-102.
26.Habif T.P. Clinical dermatology, 4th ed. St Louis:Mosby-Year Book. 2004. pp. 162-189.
27. International Dry Eye Workshop. The definition and classification of dry eye disease: Report of the Definition and Classification Subcommittee of the International Dry Eye Workshop. Ocul Surf. 2007. Vol. 5, No 2. pp. 75-92.
28. James M.J., Gibson R.A. , Cleland L.G. Dietary polyunsaturated fatty acids and inflammatory mediator production . Am J Clin Nutr. 2000. No 71. 1 Suppl. pp. 343-348.
29.Kamiya K., Nakanishi M., Ishii R., Kobashi H., Igarashi A., Sato N., Shimizu K. Clinical evaluation of the additive effect of diquafosol tetrasodium on sodium hyaluronate monotherapy in patients with dry eye syndrome: a prospective, randomized, multicenter study. Eye (Lond). 2012. No 26, Vol. 10. pp. 1363-1368.
30. Keating G.M. Diquafosol ophthalmic solution 3 %: a review of its use in dry eye. Drugs. 2015. No 75, Vol. 8. pp. 911-922.
31.Kunert K.S., Tisdale A.S., Stern M.E., Smith J.A. Analysis of topical cyclosporine treatment of patients with dry eye syndrome: effect on conjunctival lymphocytes. Arch Ophthalmol. 2000. No 118. pp. 14891496.
32.Lemp M.A. Management of dry eye disease. Am J Manag Care. 2008. Vol. 14, No 3 (Suppl). pp. 88-101.
33.Lemp M.A., Foulks G.N., Devgan U., Trattler W.B., Nichols K.K. The therapeutic role of lipids: Managing ocular surface disease. Refractive Eyecare for Ophthalmologists. 2005. Vol. 9 (Suppl). pp. 3-15.
34. Li D.Q., Luo L., Chen Z., [et al.] JNK and ER K MAP kinases mediate induction of IL -1beta, TNF-alpha and IL -8 following hyperosmolar stress in human limbal epithelial cells. Exp Eye Res. 2006. No 82. pp. 588-596.
35.Luo L., Li D., Corrales R., Pflugfelder S. Hyperosmolar saline is a proinflammatory stress on the mouse ocular surface. Eye Contact Lens. 2005. Vol. 31. pp. 186-193.
36.Luo L., Li D.Q., Doshi A., [et al.] Experimental dry eye stimulates productionof inflammatory cytokines and MMP-9 and activates MAP K signaling pathways on the ocular surface. Invest Ophthalmol Vis Sci. 2004. No 45. pp. 4293-4301.
37.Matoba A.Y., Harris D.J., Mark D.B., [et al.] Dry eye syndrome, American Academy of Ophthalmology. 2003.
38.McCulley J.P., Shine W.E., Aronowicz J. [et al.] Presumed Hyposecretory/Hyperevaporative KCS: Tear Characteristics. Trans Am Ophthalmol Soc. 2003. Vol. 101. pp. 141-154.
39. Nelson J.D., Farris R.L. Sodium hyaluronate and polyvinyl alcohol artificial tear preparations a comparison in patients with keratoconjunctivitis sicca. Arch Ophthalmol. 1988. Vol. 106. pp. 484-487.
40.Niederkorn J.Y., Stern M.E., Pflugfelder S.C., [et al.] Desiccating stress induces T cell-mediated Sjogren’s syndrome-like lacrimal keratoconjunctivitis. J Immunol. 2006. No 176. pp. 3950-3957.
41.Papas A.S., Sherrer Y.S., Charney M., [ et al.] Successful treatment of dry mouth and dry eye symptoms in Sjogren’s syndrome patients with oral pilocarpine: A randomized, placebo-controlled, dose-adjustment study. J Clin Rheumatol. 2004. No 4. pp. 169-177.
42.Perrigan D.M., Morgan A., Quintero S., [et al.] Comparison of osmolarity values of selected ocular lubricants. AR VO 2004 poster session 449.
43. Perry H.D. Dry eye disease: Pathophysiology, classification, and diagnosis. Am J Manag Care. 2008. Vol. 4, No 3 Suppl. pp. 79-87.
44.Petrone D., Condemi J.J., Fife R., [et al.] Doubleblind randomized placebocontrolled study of cevimeline in Sjogren’s syndrome patients with xerostomiaand keratoconjunctivitis sicca. Arthritis Rheum. 2002. No 46. pp. 748-754.
45.Pflugfelder S. C., Solomon A. Dry eye. Ocular surface disease. Ed. by. — E. J. Holland, M. J. Mannis, Springer. 2001. pp. 49-57.
46. Pflugfelder S. C., Solomon A. Dry eye A. Ocular surface disease. Ed. by. — New York. 2001. pp. 49-57.
47.Pflugfelder S.C., Maskin S.L., Anderson B., [et al.] A randomized, doublemasked, placebo-controlled, multicenter comparison of loteprednol etabonate ophthalmic suspension, 0.5%, and placebo for treatment of keratoconjunctivitis sicca in patients with delayed tear clearance. Am J Ophthalmol. 2004. No 138. pp .444-457.
48. Sainz de la Maza Serra S.M., Simon Castellvi C., Kabbani O. Nonpreserved topical steroids and punctal occlusion for severe keratoconjunctivitis sicca. Arch Soc Esp Oftalmol. 2000. No 75. pp. 751-756.
49. Sall K., Stevenson O.D., Mundorf T.K., Reis B.L. Two multicenter, randomized studies of the efficacy and safety of cyclosporine ophthalmic emulsion in moderate to severe dry eye disease. Ophthalmology. 2000. No 107. pp. 631-639.
50. Shine W.E., McCulley J.P., Pandya A.G. Minocycline effect on Meibomian gland lipids in meibomianitis patients. Exp Eye Res. 2003. No 76. pp. 417-420.
51. Stevenson D., Tauber J., Reis B.L. Efficacy and safety of cyclosporin A ophthalmic emulsion in the treatment of moderate-to-severe dry eye disease. A doseranging, randomized trial. Ophthalmology. 2000. No 107. pp. 967-974.
52. Tauber J., Davitt W.F., Bokosky J.E., [et al.] Double-masked, placebo-controlled safety and efficacy trial of diquafosol tetrasodium (INS365) ophthalmic solution for the treatment of dry eye. Cornea. 2004. No 23. pp. 784-792.
53. The Epidemiology of dry eye disease: report of the Epidemiology Subcommittee of the International Dry Eye Workshop. Ocul Surf. 2007. Vol. 5, No 2. P. 174.
54. The Madrid Triple Classification of Dry Eye. J. Murube [et al.] Arch. Soc. Esp. Oftalmol. 2003. Vol.78, No 11. pp. 587-594.
55. The triple classification of dry eye for practical clinical use. J. Murube [et al.] Eur. J. Ophthal. 2005. Vol. 15. pp. 660-667.
56. Toda I., Ide T., Fukumoto T., Ichihashi Y., Tsubota K. Combination therapy with diquafosol tetrasodium and sodium hyaluronate in patients with dry eye after laser in situ keratomileusis. Am J Ophthalmol. 2014. No 157, Vol. 3. pp. 616-622.
57. Turner K., Pflugfelder S.C., Ji Z., [et al.] Interleukin-6 levels in the conjunctival epithelium of patients with dry eye disease treated with cyclosporine ophthalmic emulsion. Cornea. 2000. No 19. pp. 492-496.
58. Velicer C.M., Heckbert S.R., Lampe J.W., [et al.] Antibiotic use in relation to the risk of breast cancer. JAMA. 2004. No 291. pp. 827-835.
59. Versura P., Profazio V., Giannaccare G., Fresina M., Campos E.C. Discomfort symptoms reduction and ocular surface parameters recovery with Artelac Rebalance treatment in mild-moderate dry eye. Eur J Ophthalmol. 2013. No 23, Vol. 4. pp. 488-49
Дата публикации 11 ноября 2019Обновлено 26 апреля 2021
Определение болезни. Причины заболевания
Синдром сухого глаза (сухой кератоконъюнктивит) — это воспалительное состояние глаза, при котором слёзная плёнка изменяется по своему химическому и количественному составу. Проявляется комплексом симптомов, таких как жжение, чувство рези и инородного тела в глазу.
По данным различных авторов, сухость глаза встречается примерно у 15-17 % взрослых, проживающих в развитых странах. Этот показатель каждый год увеличивается. За последние 30 лет синдром сухого глаза стал встречаться в 4,5 раза чаще [1].
Одна из причин такого увеличения распространённости синдрома связана с развитием рефракционных хирургических вмешательств — лазерного кератомилёза, фоторефракционной кератэктомии, передней радиальной кератотомии и других. Во время этих операций нарушается иннервация роговицы.
На рост данной патологии также оказывают влияние:
- повсеместное использование смартфонов, планшетов, компьютеров, другого офисного оборудования, а также кондиционеров, так как они высушивают воздух;
- ношение мягких контактных линз;
- регулярный приём лекарств — мочегонных, противоаллергических препаратов, антидепрессантов, средств для снижения холестерина, бета-блокаторов, противозачаточных таблеток [1].
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы синдрома сухого глаза
Часто встречаемые симптомы [11]:
- раздражение (покраснение) глаз;
- ощущение инородного тела в глазах;
- чувство жжения;
- слизистое отделяемое в виде нитей;
- периодические «затуманивание».
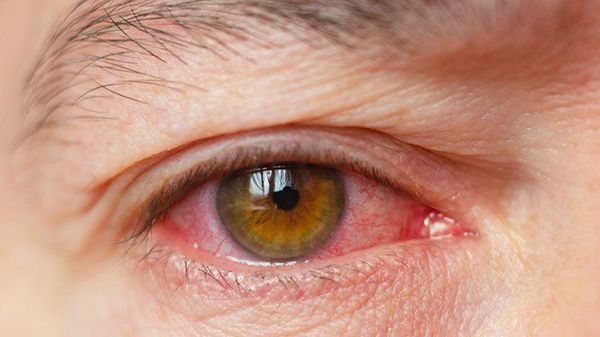
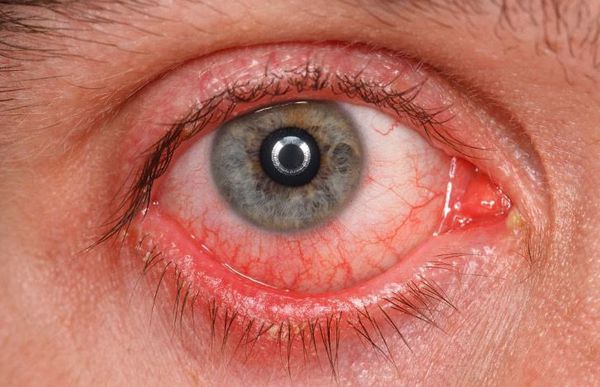
Реже наблюдается зуд в глазу, светобоязнь, утомление или чувство тяжести в глазах. При этом чувства стянутости и давления за глазами не возникают.
Как правило, все перечисленные симптомы проявляются на обоих глазах, но иногда они возникают только в одном глазном яблоке.
Любопытно, что пациенты с синдромом сухого глаза редко жалуются на сухость глаз, хотя иногда они отмечают нехватку эмоциональных слёз или отсутствие слезотечения в ответ на раздражитель, например, лук. В некоторых случаях пациентов беспокоит слезотечение, особенно на улице, так как там много раздражающих факторов — яркое солнце, ветер, холод. От возникающего слезотечения они испытывают дискомфорт.
Признаки сухого кератоконъюнктивита часто усиливаются из-за воздействия внешних факторов, связанных с повышенным испарением слезы от ветра, кондиционера, отопления или при длительном чтении, так как человек начинает реже моргать. При закрытых веках симптомы уменьшаются [5].
Патогенез синдрома сухого глаза
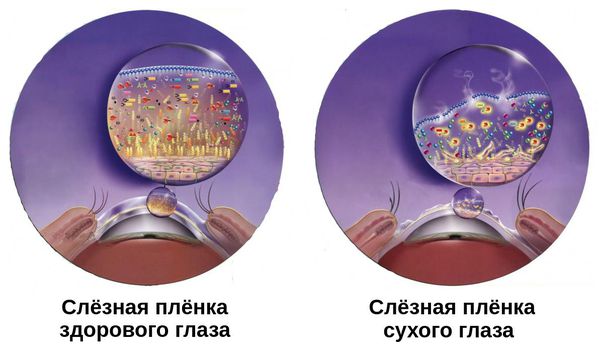
Патогенез сухого кератоконъюнктивита связан с нарушением стабильности слёзной плёнки. Она покрывает переднюю поверхность глаза. В норме её толщина составляет около 10 мкм. При развитии синдрома она становится тоньше.
Распределение слёзной плёнки поверхности глаза происходит благодаря рефлекторному морганию. Для её эффективного распределения должны сочетаться несколько факторов:
- нормальный моргательный рефлекс;
- контакт век и глазной поверхности;
- нормальный эпителий (внешний слой) роговицы.
Слёзная плёнка неоднородна. Она имеет три слоя:
- первый (внешний) слой — липидный — вырабатывается мейбомиевыми железами;
- второй слой — водный — вырабатывается слёзными железами;
- третий слой — муциновый — вырабатывается бокаловидными клетками роговицы.
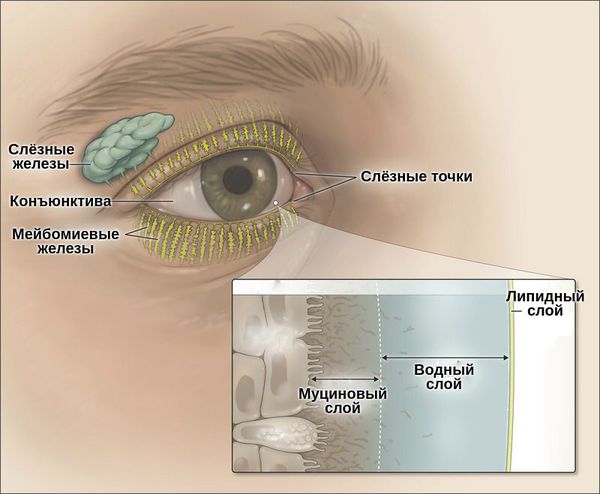
Липидный слой — самый тонкий. Его основная задача — задерживать испарения водного слоя и поддерживать слёзную плёнку. При его нехватке увеличивается испаряемость слезы, что приводит к «сухому глазу».
Водный слой является основой слёзной плёнки. Он состоит из воды, электролитов и белков. За счёт непрерывного обновления он выполняет своё предназначение — доставляет кислород к эпителию роговицы, защищает от бактерий, вымывает инородные тела, обеспечивает гладкость и ровность оптической поверхности.
Муциновый слой состоит из муцинов, которые помогают слёзной плёнке удерживаться на роговице. Он увлажняет и смазывает роговичный эпителий. Его дефицит может быть вызван как нехваткой водного слоя, так и высокой испаряемостью слёзной жидкости. Другой причиной нарушения муцинового слоя может стать повреждение бокаловидных клеток, которые его продуцируют. Это происходит при рубцующемся конъюнктивите, нехватке витамина А, химических ожогах, токсическом воздействии медикаментов [3].
Исходя из особенностей строения слёзной плёнки, патогенез сухого кератоконъюнктивита затрагивает несколько звеньев образования и функционирования слёзной плёнки [1]:
- выработка слезы, муцинов и липидов;
- скорость испарения слёзной плёнки;
- образование слёзной плёнки на поверхности эпителия роговицы.
Классификация и стадии развития синдрома сухого глаза
Единой классификации данного синдрома пока нет, но существует несколько авторских классификаций. Вот некоторые из них.
Национальный глазной институт Америки выделяет две основные категории синдрома:
- Снижение выработки слезы:
- синдром Шегрена — нарушение работы слюнных и слёзных желёз, которое приводит к развитию синдрома сухого глаза;
- снижение выработки слезы, не связанное с синдромом Шегрена.
- Увеличение испарения слезы:
- воспалительное заболевание мейбомиевой железы;
- атрофия мейбомиевых желёз.
Доктор B. Dohlman классифицирует синдром в зависимости от причин снижения слезопродукции слёзным железами:
- Дефицит слезопродукции — обычно связан со скоплением лимфоцитов в ткани слёзной железы:
- синдром Шегрена;
- коллагеноз (синдром Райли — Дея) — редкое наследственное заболевание, которое поражает периферическую нервную систему.
- Дефицит муцина:
- синдром Стивенса Джонсона — тяжёлая системная аллергия, которая снижает защитные свойства муцина;
- глазной пемфигоид — хроническое заболевание глаз аутоиммунного генеза, приводит к недостатку муцина;
- авитаминоз витамина А, который входит в состав муцина.
- Изменённая поверхность роговицы — наблюдается при трахоме (хроническом конъюнктивите, вызванном хламидиями), простом герпесе, роговичных дистрофиях. Повреждённые места уязвимы для инфекций и появления язв.
- Недостаточность увлажнения. Связана с нейропаралитическим кератитом — воспалительно-дистрофическим изменением роговицы на фоне поражения тройничного нерва. Проявляется снижением или отсутствием чувствительности роговицы, невралгическими болями, помутнением и язвой роговицы.
Азиатское общества сухих глаз (ADES) также классифицирует синдром по причинам его возникновения [2]:
- дефицит воды;
- снижение смачиваемости;
- увеличение испарения.
По клиническим проявлениям — жжению, зуду, рези, ощущению тяжести и инородного тела в глазах, слезотечению, светобоязни, уменьшению симптомов после закрытия глаз — синдром сухого глаза бывает:
- слабым — 1-2 симптома;
- умеренным — 3-5 симптомов;
- тяжёлым — более 5 симптомов.
Осложнения синдрома сухого глаза
В зависимости от стадии синдрома у человека может временно ухудшаться зрение, которое восстанавливается при моргании.
Сухость глаза повышает вероятность возникновения бактериального кератита и частого изъязвления, которые могут стать причиной появления перфорации роговицы [5]. Клинически бактериальный кератит проявляется:
- острой болью в глазу;
- отёком;
- корнеальным синдромом — светобоязнью, слезотечением, непроизвольным «зажмуриванием»;
- выраженной воспалительной инъекцией глазного яблока;
- слизисто-гнойными выделениями;
- помутнениями роговицы;
- поверхностными или глубокими изъязвлениями роговицы.
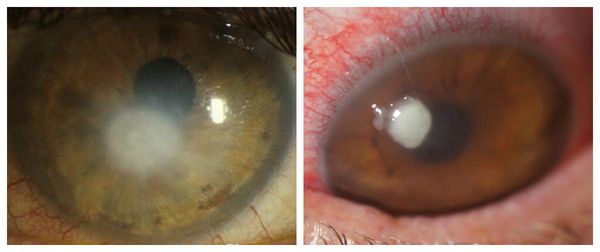
Перфорация роговицы опасна серьёзным снижением зрения, которое может потребовать пересадку роговицы.
Диагностика синдрома сухого глаза
При проведении биомикроскопии врач-офтальмолог может разглядеть признаки нарушения слёзной плёнки и роговицы.
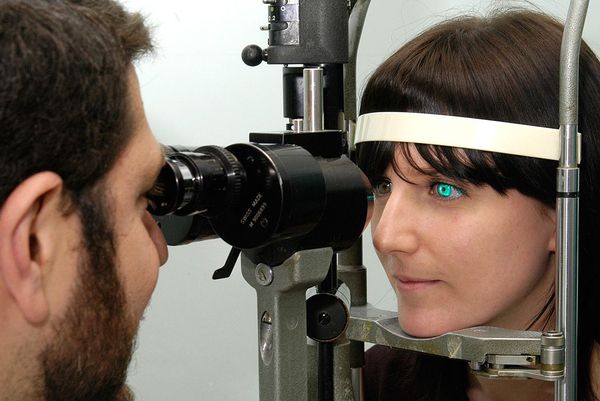
Нарушения слёзной плёнки:
- Появление нитей муцина — признак раннего сухого кератоконъюнктивита. В здоровом глазу после разрыва слёзной плёнки муциновый и липидный слои смешиваются и быстро смываются. При синдроме сухого глаза муцин также смешивается с липидным слоем, но не вымывается, а скапливается в слёзной плёнке и смещается при мигании.
- Уменьшение слёзного мениска — объёма водного слоя слёзной плёнки. В норме он представляет собой выпуклую полосу с правильным верхним краем. При сухом кератоконъюнктивите слёзный мениск становится вогнутым, неравномерным, тонким, а иногда вовсе исчезает.
- Отделяемое в виде пены — возникает в слёзной плёнке или по краю века при нарушении работы мейбомиевых желёз.
Нарушения роговицы:
- Точечная эрозия роговицы — возникает в нижней половине роговицы.
- Появление роговичных нитей. Они состоят из небольших комочков слизи в форме запятой. Одни концы нитей прикрепляются к поверхности роговицы, другие свободно двигаются при мигании.
- Наличие нитчатых инфильтратов — полупрозрачные бело-серые немного выпуклые образования. Как правило, их обнаруживают одновременно с нитями слизи во время окрашивания бенгальским розовым красителем [5].
Для подтверждения и постановки диагноза сухости глаз также проводят различные тесты. Чем выраженнее синдром, тем они надёжнее. Во время тестов измеряют следующие параметры [3]:
- стабильность слёзной плёнки и время её разрыва;
- выработка слезы — тест ширмера, осмолярность слезы;
- заболевание глазной поверхности — окрашивание поверхности глаза.
Тест на время разрыва слёзной плёнки
Время разрыва слёзной пленки — показатель её стабильности. Его измеряют следующим образом:
- в нижний свод конъюнктивы закапывают флуоресцеин;
- просят пациента мигнуть несколько раз, а затем не моргать;
- через щелевую лампу с кобальтовым синим фильтром исследуют срез слёзной плёнки.
Через некоторое время в окрашенной плёнке возникают чёрные линии или пятна, которые указывают на появление сухих участков. Важно зафиксировать время между последним миганием и появлением первых сухих участков. Если данный промежуток длится менее 10 секунд, то это отклонение от нормы.
Тест Ширмера
Данный тест проводят для оценки слезопродукции. С его помощью измеряют увлажнённую часть специальными бумажными фильтрами. Тест проводят следующим образом:
- осторожно убирают имеющуюся слезу;
- согнутый бумажный фильтр помещают в полость конъюнктивы, не касаясь роговицы;
- просят пациента не закрывать глаз и моргать как обычно;
- через пять минут фильтры убирают и оценивают уровень увлажнения: 6-10 мм — это норма, диапазон менее 6 мм указывает на снижение выработки слезы.
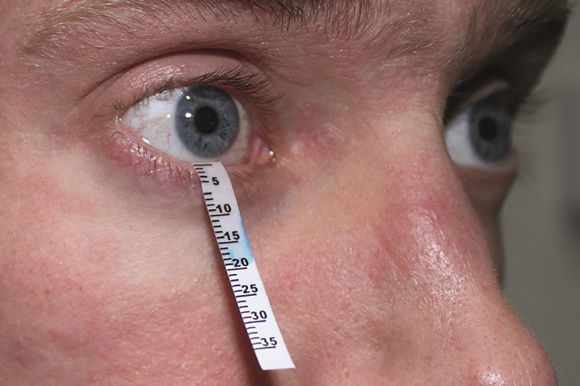
Тест с окрашиванием глазной поверхности
Специальные красители используют для окрашивания нежизнеспособных клеток муцина. Бенгальский розовый краситель прокрашивает изменённую поверхность роговицы в виде двух треугольников. Роговичные нити и инфильтраты также окрашиваются, но ещё интенсивнее. Минусом бенгальского розового в том, что он может вызвать гиперемию (покраснение) глаз, особенно при выраженном синдроме [5]. Тест с лиссаминовым зелёным вызывает меньше раздражения.
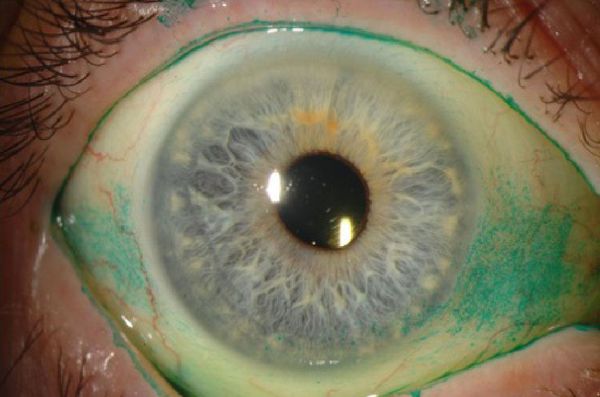
Другие способы диагностики
Помимо основных перечисленных методов диагностики иногда используют следующие тесты [3]:
- осмолярность слёзной плёнки;
- измерение состава слезы;
- слёзная менискометрия;
- импрессионная цитология;
- тест на лактоферрин;
- тест красной нити фенола;
- клиренс-флюоресцииновый тест.
Также применяется мейбография — бесконтактная визуальная оценка структуры мейбомиевых желёз. Она проводится независимо от возраста и пола пациента [9]. Данный метод диагностики используется редко, так как он достаточно новый и не везде есть нужное оборудование.
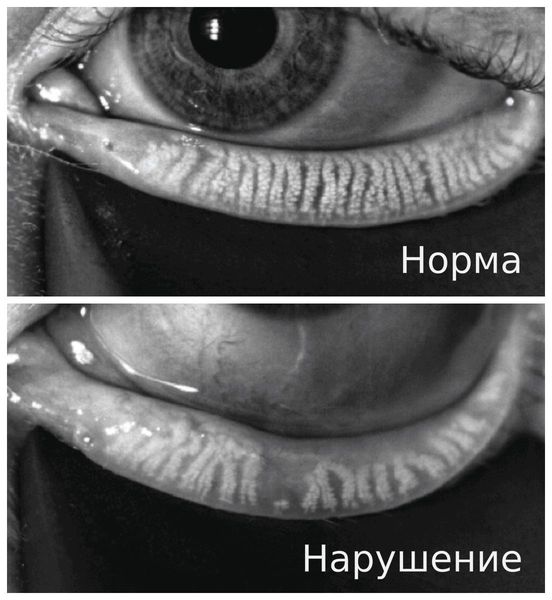
Лечение синдрома сухого глаза
Главная задача при лечении «сухого глаза» — уменьшить неприятные ощущения, сохранить оптическую поверхность роговицы и не допустить повреждения её структур. Одновременно можно применять сразу несколько способов лечения [5].
Сохранение вырабатываемой слезы:
- Уменьшение комнатной температуры — позволяет минимизировать испарения слёзной плёнки.
- В помещении можно использовать увлажнители воздуха, но чаще всего это не даёт результатов. Аппарат не способен значительно увеличить относительную влажность воздуха. Местно повысить влажность можно при помощи специальных очков. У них есть съёмная прокладка, которая защищает глаза от ветра и других раздражающих факторов.

- Частичная боковая тарзорафия — операция, которая заключается в полном или частичном ушивании краёв век. Она уменьшает расстояние между веками глаза, чем может благотворно повлиять на состояние пациента.
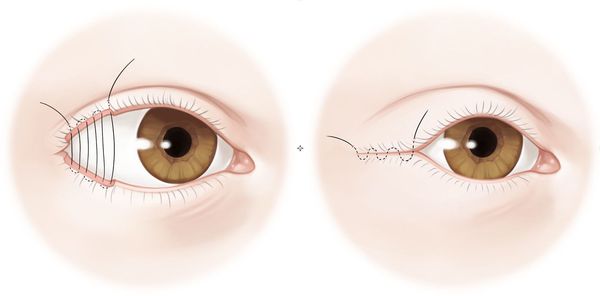
Заместители слезы:
- Капли используются довольно часто. Их главный недостаток — короткий период действия и развитие чувствительности к консерванту.
- Гели состоят из карбомеров — заместителей слезы. Их приходится наносить не так часто, как капли, поэтому использование гелей предпочтительней.
- Также используют мази, которые содержат вазелин и минеральные липиды.
- Спреи для век обычно содержат средство на основе липосома. Они позволяют уменьшить испарение и стабилизировать слёзную плёнку.
Муколитические препараты
Ацетилцистеин 5 % в форме капель можно использовать для лечения пациентов с нитчатым кератитом и инфильтратами. Капли применяют четыре раза в день. Они могут вызвать покраснение после закапывания.
Уменьшение оттока слезы
Окклюзия (закупорка) слёзной точки сохраняет отток слезы и продлевает эффект воздействия искусственных слёз. Это процедура показана пациентам с выраженным синдромом, особенно из-за токсичности консервантов.
Временная закупорка слёзной точки происходит при помещении коллагеновой заглушки в слёзные канальцы. Самая важная задача временной окклюзии — убедиться в том, что после неё не возникнет обильное слезотечение. Для временной окклюзии на несколько месяцев используются силиконовые заглушки. Постоянная окклюзия проводится пациентам с выраженным сухим кератоконъюнктивитом.
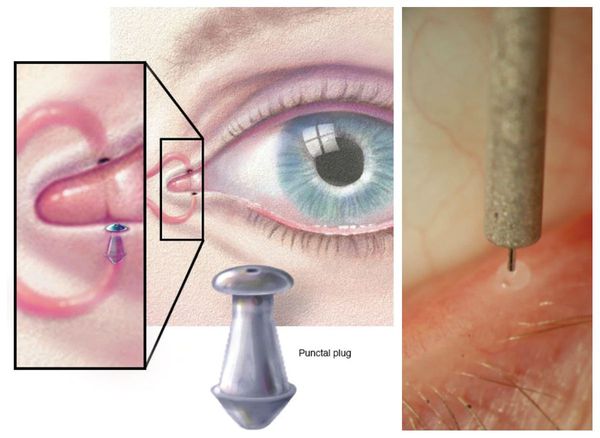
Другие варианты лечения:
- Местное использование циклоспорина 0,05 % или 0,1 % — безопасный, хорошо переносимый и эффективный препарат. Он позволяет уменьшить воспаление слёзной плёнки на уровне клеток.
- Системный приём холинергических препаратов типа пилокарпина — весьма эффективен в лечении ксеростомии — сухости во рту. У 40 % пациентов с сухим кератоконъюнктивитом наблюдается положительный эффект.
Лечение мейбомиевых желёз
Нарушение работы данных желёз является основной причиной появления синдрома сухого глаза. Существует множество вариантов его лечения. Консервативные меры включают тёплые компрессы и гигиену век — наложение тёплых ватных дисков на пять минут, использование специальных гелей для век. Потенциальные медицинские методы лечения включают в себя антибиотики, нестероидные и стероидные противовоспалительные средства, добавки незаменимых жирных кислот, гормональную терапию и контроль инвазии демодекса — распространения клеща Demodex. Процедуры включают внутрипротоковое исследование мейбомиевых желёз, использование электронных нагревательных приборов, интенсивную импульсную световую терапию и интраназальную нейростимуляцию — электростимуляция нервных окончаний увеличивают производство слезы [7].
Прогноз. Профилактика
Причинные процессы, вызывающие сухость глаза, как правило, необратимы, поэтому лечение строится вокруг контроля симптомов и предотвращения повреждения поверхности.
Пациенту необходимо пересмотреть свой образа жизни:
- не носить контактные линзы дольше, чем рекомендует производитель;
- прекратить использование препаратов с потенциально токсическим воздействием (капли с консервантами);
- следить, чтобы уровень влажности в помещении был достаточным;
- чаще моргать во время чтения, просмотра телевизора или работы за компьютером;
- располагать экран так, чтобы он был ниже уровня глаз.
Интересно, что при ношении гарнитуры виртуальной реальности толщина липидного слоя и стабильность слёзной плёнки становится лучше, чем при использовании обычного настольного компьютера [8].
Выраженная сухость глаза у курильщиков электронных сигарет и вейперов указывают на потенциальный вред паров электронных сигарет и вейпов по отношению к глазам. Они ухудшают качество слёзной плёнки, из-за чего синдром сухого глаза становится умеренным или тяжёлым. Помимо пара на слёзную плёнку воздействуют опасные побочные продукты вейпа [4].
На качество слёз также влияет индекс массы тела. Как показало недавнее исследование, качество слезы у людей с высоким индексом массы тела было ниже, чем у людей с нормальным весом [10]. Поэтому правильно питание может снизить риск развития нарушений обмена веществ в организме, а следовательно и синдрома сухого глаза.
Хирургическое вмешательство является наиболее эффективным средством для повышения остроты зрения при катаракте. И хотя современные способы лечения катаракты безопасны и эффективны, после операции может развиться несколько осложнений, таких как кистозный макулярный отёк, а также сухость глаза. Причины послеоперационного «сухого глаза» пока не установлены. Поэтому если пациент планирует лазерную рефракционную операцию, то врач должен предупредить его, что эта процедура может привести к синдрому сухого глаза или усугубить его [3].
Препаратов, предназначенных для профилактики послеоперационного сухого глаза, пока не разработано. И хотя использование нестероидных противовоспалительных средств эффективно снижает частоту и степень послеоперационного кистозного макулярного отёка, они могут вызывать побочные эффекты, включая аномалии поверхности и сухость глаз. В связи с этим послеоперационные лекарства должны тщательно отбираться, чтобы улучшить результаты лечения и не допустить развитие сухого кератоконъюнктивита [6].
Синдром «сухого» глаза – болезнь цивилизации
Завершен 12 октября 2022, 12:49 (Мск)
12 октября 2022, 12:00 (Мск)
Видео доступно только зарегистрированным пользователям
В программе вебинара:
- В рамках вебинара будет возможность больше узнать о том, как правильно позаботиться о своем зрении.
- Почему синдром сухого глаза (ССГ) является болезнью цивилизации и почему наши глаза нуждаются в уходе и заботе?
- Распространенность ССГ
- Существующие методы диагностики, лечения и профилактики ССГ.
- Препараты для коррекции ССГ
- Слезозаменитель покрывающий все потребности потребителей с ССГ– миф или реальность?
Всё это разберём на примере препарата СТИЛЛАВИТ®
Если у вас не отображается форма регистрации на вебинар, отключите блокировку всплывающих окон в браузере или перейдите по ссылке
Примечание: пользователям мобильных устройств необходимо установить мобильное приложение Webinar и зарегистрироваться в нем.
Приложение для iOS
Приложение для Android
Лектор:
Анжелла Щербакова
бренд-менеджер компании STADA
Как подготовиться к вебинару
При подключении к серверу уровень сигнала должен быть хорошим. Если уровень сигнала слабый или отсутствует подключение к одному из серверов, в вебинаре могут быть недоступны видео и звук. Рекомендуем обратиться к своему системному администратору для решения проблемы.
Обновить Flash Player до последней версии
Использовать браузеры не ниже следующих версий:
Internet Explorer 11 / Edge; Google Chrome 48 и выше; Mozilla Firefox 43 и выше; Safari 8.0.8 и выше; Яндекс.Браузер 16.7

ВВЕДЕНИЕ
В последние годы все большую актуальность для клинической практики приобретает синдром «сухого глаза», клинически проявляющийся роговично-конъюнктивальным ксерозом различной выраженности. По этой причине оба термина достаточно правомочны при обозначении рассматриваемого заболевания и широко используются в литературе.
В целом, к cиндрому «сухого глаза» относят комплекс клинико-функциональных признаков высыхания (ксероза) поверхности роговицы и конъюнктивы вследствие длительного нарушения стабильности слезной пленки, покрывающей роговицу.
Синдром «сухого глаза» в настоящее время служит одной из нередких причин хронического раздражения глаза, воспалительной инъекции сосудов конъюнктивы и, соответственно, «красного глаза».
Рассматриваемое заболевание характеризуется главным образом обилием субъективных симптомов при относительно менее выраженных объективных признаках. Вместе с тем ксеротические процессы в роговице и конъюнктиве, свойственные синдрому «сухого глаза», зачастую достигают и такой выраженности, когда приходится предпринимать экстренные хирургические вмешательства для сохранения зрительных функций и глазного яблока пациента.
ЭПИДЕМИОЛОГИЯ СИНДРОМА «СУХОГО ГЛАЗА»
По данным разных авторов, рассматриваемое заболевание распространено в среднем у 15-17% всего взрослого населения развитых стран мира. Причем этот показатель имеет тенденцию к повышению из года в год. Так, за последние 30 лет частота обнаружения синдрома «сухого глаза» возросла в 4,5 раза!
Увеличение распространенности синдрома «сухого глаза» в последние годы связано также с дальнейшим развитием кераторефракционных хирургических вмешательств (ЛАЗИК, ЛАСИК, ФРК, уходящая в прошлое передняя радиальная кератотомия и др.).
На рост заболеваемости синдромом «сухого глаза» влияние также оказывают широкое распространение компьютерных мониторных систем, кондиционеров и другого офисного оборудования, совершенствование средств контактной коррекции зрения и других «составляющих» жизни современного цивилизованного общества. Важным «вкладом» в распространенность синдрома «сухого глаза» также является систематическое применение современных медикаментозных препаратов самой различной направленности, использование косметических средств (и косметических операций на коже лица), ухудшение экологической обстановки.
ПАТОГЕНЕЗ СИНДРОМА «СУХОГО ГЛАЗА»
В основе возникновения рассматриваемого заболевания лежит нарушение стабильности слезной пленки, в норме покрывающей переднюю поверхность глазного яблока.
Известно, что толщина слезной пленки у здоровых людей в среднем составляет всего 10 мкм. В структурном отношении слезная пленка неоднородна.
Снаружи она покрыта тонкой пленкой липидов, препятствующей чрезмерному испарению влаги, а также теплоотдаче с поверхности эпителия роговицы и конъюнктивы.
Второй, водянистый слой (продукт секреции добавочных и главной слезных желез), составляет основу слезной пленки. Непрерывное его обновление обеспечивает метаболические, защитные и другие биологические функции слезной пленки.
Важным структурным составляющим водянистого слоя служит его муциновый компонент. Муцины продуцируют бокаловидные клетки конъюнктивы. Основная их функция заключается в придании гидрофобному эпителию роговицы гидрофильных свойств, позволяющих удерживать слезную пленку на роговице (рис. 1).
Нарушения процессов физиологического обновления слезной пленки у здоровых людей лежит в основе патогенеза синдрома «сухого глаза» (рис. 2). При этом они весьма разнообразны и могут касаться различных звеньев формирования и функционирования слезной пленки (схема 1):
— продукции слезы, муцинов и липидов;
— скорости испарения слезной пленки;
— формирования слезной пленки на поверхности эпителия роговицы.
КЛИНИЧЕСКАЯ КЛАССИФИКАЦИЯ СИНДРОМА
«СУХОГО ГЛАЗА»
Клиническая классификация синдрома «сухого глаза» представлена в таблице 1.
КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ СИНДРОМА
«СУХОГО ГЛАЗА»
Рассматриваемое заболевание проявляет себя обилием неспецифических субъективных симптомов, которые сочетаются с менее выраженными объективными проявлениями патологии и определяют ее тяжесть.
Легкая клиническая форма ксероза характеризуется наличием микропризнаков заболевания, которые развиваются на фоне компенсаторно повышенной слезопродукции. На первый взгляд парадоксально, однако таких пациентов беспокоит слезотечение.
Причем оно заметно усиливается при воздействии на глаз неблагоприятных факторов внешней среды.
Особого внимания заслуживают специфические признаки ксероза. Характерна негативная реакция больных на закапывание в конъюнктивальную полость даже вполне индифферентных глазных капель, так как оно сопровождается ощущением жжения или рези в глазу. Закапывание же в него обычно раздражающих капель сопровождается появлением резко выраженных болей.
Встречается также симптом плохой переносимости кондиционированного воздуха, тепловентиляторов, ветра, дыма и смога. Аналогичные явления также наблюдают некоторые пациенты при просмотре телевизора, работе за компьютером или при чтении, особенно в вечернее время.
Среди объективных признаков специфическим, однако относительно редким симптомом служит характерное отделяемое из конъюнктивальной полости. При туалете век оно вследствие высокой вязкости вытягивается в виде тонких слизистых нитей, тягостно переносимых больными.
Достаточно демонстративным объективным признаком ксероза служит замедленное разлипание тарзальной и бульбарной конъюнктивы при оттягивании нижнего века, свидетельствующее о дефиците муцинов в конъюнктивальной полости.
Кроме рассмотренных специфических микропризнаков, у больных с легким роговично-конъюнктивальным ксерозом одновременно отмечены и косвенные его симптомы.
Клиническое течение глазного ксероза средней степени тяжести определяется, как правило, совокупностью тех же микропризнаков роговично-конъюнктивального ксероза, которые рассмотрены выше. Однако частота их обнаружения и степень выраженности заметно превышают таковые при легком ксерозе.
Кроме того, у таких больных уже отсутствует рефлекторное слезотечение и появляются признаки дефицита слезопродукции.
В частности, у них заметно уменьшаются или полностью отсутствуют у краев век слезные мениски. Место отсутствующего мениска обычно занимает отекшая и потускневшая конъюнктива, «наползающая» на свободный край века (так называемый конъюнктивохалазис).
Тяжелый роговично-конъюнктивальный ксероз встречается в виде одной из трех клинических форм — нитчатого кератита, «сухого» кератоконъюнктивита и рецидивирующей эрозии роговицы.
Нитчатый кератит характеризуется образованием на роговице единичных, а чаще множественных эпителиальных разрастаний в виде нитей, фиксированных одним концом к ее эпителию (рис. 3). Свободный конец такой нити смещается по роговице при мигании и раздражает глаз, что вызывает роговичный синдром, но, как правило, без воспалительных изменений конъюнктивы.
«Сухой» кератоконъюнктивит наряду с признаками нитчатого кератита и микропризнаками ксероза проявляет себя выраженными изменениями поверхности глазного яблока воспалительно-дегенеративного характера. При этом наблюдаются изменения рельефа эпителия роговицы в виде блюдцеобразных эпителизированных или неэпителизированных углублений, субэпителиальных ее помутнений различной выраженности, эпителиальных нитей (рис. 4). Она теряет в ряде случаев также свой блеск, становится тусклой и шероховатой. Зачастую расширяется и зона поверхностной перилимбальной васкуляризации. Бульбарная конъюнктива тускнеет, наблюдается ее «вялая» гиперемия и отек у краев век. При мигании она увлекается веками, смещаясь по глазному яблоку в большей степени, чем у здоровых людей. Течение заболевания хроническое, с частыми обострениями и ремиссиями.
Рецидивирующая эрозия роговицы характеризуется периодическим возникновением поверхностных микродефектов эпителия роговицы. Обычно они связаны со слипанием заднего ребра века с эпителием роговицы во сне вследствие дефицита липидного слоя слезной пленки. При пробуждении (или во время быстрой фазы сна) веко смещается относительно роговицы, отрывая часть ее эпителиальных клеток. Однако, несмотря на небольшую площадь, такие эрозии сохраняются достаточно долго (до 2-3 суток и более), медленно эпителизируясь (рис. 5). Характерен выраженный роговичный синдром, сменяющийся длительным дискомфортом даже по завершении эпителизации эрозии. Однако уже через 2-3 месяца, а иногда и раньше, заболевание обычно вновь рецидивирует.
Особо тяжелый роговично-конъюнктивальный ксероз развивается обычно у больных с полным или частичным несмыканием глазной щели вследствие лагофтальма различного генеза с нарушением иннервации роговицы, пемфигусом или с выраженным недостатком в организме витамина А. При этом заболевание проявляется в одной из четырех нозологических форм:
— кератит вследствие несмыкания глазной щели;
— ксеротическая язва роговицы;
— рубцующий пемфигоид (пемфигус глаза);
— ксероз конъюнктивы и роговицы на почве недостаточности витамина А.
Кератит вследствие несмыкания глазной щели достаточно хорошо известен каждому врачу, и поэтому не нуждается в подробном описании. Необходимо лишь иметь в виду, что у ослабленных больных он может осложниться развитием язвы с последующей перфорацией роговицы.
Ксеротическая язва роговицы характеризуется образованием дефекта роговицы с захватом ее стромы и тенденцией к дальнейшему углублению (чаще — без расширения по площади), вплоть до перфорации. Язва почти всегда локализуется в пределах открытой глазной щели (рис. 6). Клиническое течение заболевания затяжное с медленным прогрессированием, несмотря на активно проводимую терапию.
Рубцующий пемфигоид (так называемый пемфигус глаза) характеризуется изолированным поражением всех отделов конъюнктивы с прогрессирующим рубцеванием, укорочением сводов конъюнктивы и развитием сосудистого паннуса (рис. 7). Заболевание медленно, но упорно прогрессирует. Зрение снижается, когда помутнение захватывает оптическую зону роговицы.
Ксерофтальмия на почве выраженного авитаминоза А еще относительно недавно была характерна в основном для жителей (преимущественно детей) стран Южной и Восточной Азии, некоторых районов Африки, Ближнего Востока и Латинской Америки. Однако таких больных можно встретить и в нашей стране (дети с плохим усвоением витамина А, с тяжелой формой аллергии и т.п.). В патогенезе рассматриваемой патологии лежит недоразвитие эпителиальных и бокаловидных клеток конъюнктивы, дифференцирование которых в норме регулируют метаболиты витамина А. В результате развивается чешуйчатая метаплазия эпителия с последующей кератинизацией конъюнктивы.
Ксерофтальмия рассматриваемого генеза в своем развитии проходит несколько стадий, являющихся, с другой стороны, и самостоятельными нозологическими формами: стадию конъюнктивального ксероза (рис. 8), паренхиматозного ксероза роговицы, ксеротической язвы роговицы и, наконец, кератомаляции с последующей потерей глаза.
В заключение следует отметить, что в большинстве своем (пожалуй, за исключением случаев выраженного ксероза) клиническая картина синдрома «сухого глаза» характеризуется обилием неспецифических симптомов. При этом признаки, патогномоничные для рассматриваемой патологии, зачастую отступают на задний план, маскируясь косвенными симптомами.
В силу рассмотренных обстоятельств большое значение приобретают рационально спланированные диагностические мероприятия в отношении больных с данной патологией.
ДИАГНОСТИКА СИНДРОМА «СУХОГО ГЛАЗА»
Обследование пациентов с подозрением на рассматриваемое заболевание базируется на традиционных клинических методах и в сомнительных случаях дополняется постановкой специальных функциональных проб (схема 2).
Клиническое обследование больного складывается из сбора жалоб и анамнеза, ориентированного на выяснение возможных причин развития синдрома «сухого глаза», а также тщательного осмотра с помощью щелевой лампы свободного края век, роговицы и конъюнктивы.
Выяснение жалоб больного должно заключаться в активном исключении каждого субъективного симптома из перечня, представленного в таблице 2.
Сбор анамнеза должен быть целенаправлен на активный поиск общих заболеваний, которые могли бы вызвать синдром «сухого глаза». Перечень наиболее значимых из них представлен ниже.
1. Заболевания соединительной ткани (коллагенозы):
• первичный и вторичный синдром Съегрена;
• ревматоидный артрит;
• системная красная волчанка;
• узелковый периартериит (синдром Kussmaul);
• склеродермия.
2. Заболевания гемопоэтической и ретикулоэндотелиальной систем:
• ревматоидный артрит, сочетанный со спленомегалией и нейтропенией (синдром Фелти);
• аутоиммунный процесс отторжения трансплантата костного мозга, реакция «трансплантат против хозяина» и т.п.;
• гемолитическая анемия;
• хронический гепатит; первичный билиарный цирроз.
3. Эндокринные дисфункции:
• перименопауза;
• эндокринная и тиреотоксическая офтальмопатия;
• сахарный диабет.
4. Заболевания кожи и слизистых оболочек, приводящие к комбинированной недостаточности слезы и муцинов:
• пемфигус и рубцующий пемфигоид;
• токсический эпидермальный некролиз (синдром Лайла);
• эксфолиативный и герпетический дерматит и др.
Синдромом «сухого глаза» зачастую также осложняются и некоторые офтальмологические операции и повреждения органа зрения.
1. Кераторефракционные операции:
• кератомилез in situ (ЛАЗИК);
• субэпителиальная ФРК (ЛАСИК);
• фотоабляция роговицы (ФРК);
• передняя радиальная кератотомия.
2. Реконструктивные и прочие операции:
• вмешательства, сопровождающиеся нанесением разрезов на роговицу и конъюнктиву;
• экстирпация слезной железы.
3. Последствия повреждений органа зрения:
• деформация конъюнктивальной полости;
• укорочение век с неполным их смыканием;
• рубцовые изменения поверхности роговицы;
• рецидивирующая эрозия роговицы.
Следует также учитывать и артифициальные факторы, стимулирующие развитие роговично-конъюнктивального ксероза:
• кондиционированный воздух или воздух с примесью взвешенных пылевых частиц;
• усиленная конвекция воздуха от тепловентиляторов;
• электромагнитное излучение от компьютерных и телевизионных систем;
• мягкие и жесткие контактные линзы в случаях плохой индивидуальной их переносимости, дефекта подбора или погрешностей в использовании;
• косметические средства плохого качества, нанесенные на ресницы, кожу век и лица или в случаях их плохой индивидуальной переносимости;
• дым, в том числе от сигарет, смог;
• испарения различных химических веществ (лаки, краски, химические растворители и т.п.), в том числе от полимерных покрытий офисных помещений.
При расспросе больного необходимо также обращать внимание на возможное системное и местное применение им препаратов, нарушающих слезопродукцию или стабильность слезной пленки:
• средства, снижающие артериальное давление: α1- и α2-адреноблокаторы, β-адреноблокаторы;
• адреномиметические вещества;
• антиаритмические препараты;
• антидепрессанты;
• препараты для лечения язвенной болезни (холинолитики);
• «малые» транквилизаторы;
• антигистаминные препараты;
• оральные контрацептивные средства.
Необходимо отметить, что синдром «сухого глаза» могут стимулировать и некоторые глазные капли (при длительном местном применении): β-адреноблокаторы, холинолитики, глюкокортикостероиды, а также препараты, содержащие токсичные консерванты.
В ходе биомикроскопии глазной поверхности активный поиск должен быть направлен на выявление объективных микропризнаков ксероза (табл. 2). При этом следует воспользоваться диагностическими красителями: флюоресцеином натрия (окрашивает в зеленый цвет поверхностные дефекты эпителия роговицы), бенгальским розовым и лиссаминовым зеленым. Последние окрашивают, соответственно, в красный и зеленый цвет, погибшие и дегенерированные (но еще присутствующие на эпителиальной мембране роговицы и, главное, конъюнктивы) клетки, а также эпителиальные и слизистые нити (рис. 9).
В пользу диагноза синдрома «сухого глаза» свидетельствует обнаружение дегенеративных изменений на роговице и конъюнктиве в пределах открытой глазной щели (рис. 10).
Функциональное обследование больного показано в случаях, когда природа выявленных у него изменений остается неясной. Оно состоит из последовательной постановки двух специальных проб, позволяющих оценить стабильность прероговичной слезной пленки и измерить величину общей слезопродукции.
Определение стабильности слезной пленки осуществляют методом Norn M. (1969) после закапывания в конъюнктивальную полость 0,1% раствора флюоресцеина натрия. Первый разрыв в подкрашенной слезной пленке на открытом глазу (рис. 11) не должен возникнуть быстрее, чем через 10 секунд после последнего мигания.
Величину суммарной слезопродукции определяют пробой по Schirmer O. с помощью тонкой полоски (длиной 35 мм и шириной 5 мм) из фильтровальной бумаги. Полоску помещают одним концом за нижнее веко исследуемого глаза (рис. 12) и через 5 минут оценивают длину смоченной слезой части полоски. В норме смачивается не менее 15 мм тестовой полоски.
ЛЕЧЕНИЕ БОЛЬНЫХ С СИНДРОМОМ «СУХОГО ГЛАЗА»
Лечение пациентов с рассматриваемой патологией органа зрения предусматривает осуществление мероприятий следующей направленности (схема 3). Основные из них призваны купировать процессы высыхания и воспаления в тканях глазной поверхности, а также стабилизировать слезную пленку. Кроме того, большое значение также имеют лечебные мероприятия, направленные на компенсацию сопутствующих ксерозу изменений глаз и организма.
Увлажнение глазной поверхности и стабилизация слезной пленки являются основным направлением лечения больных с синдромом «сухого глаза». На практике оно включает следующие мероприятия:
— инстилляции препаратов «искусственной слезы» в виде глазных капель и гелей;
— стимулирование слезопродукции;
— обтурация слезоотводящих путей в целях сокращения оттока влаги из конъюнктивальной полости;
— пересадка слюнных желез слизистой рта в конъюнктивальную полость.
Первый этап лечения предусматривает использование в качестве базовых средств различных заменителей слезной жидкости (так называемых препаратов «искусственной слезы»), отличающихся в основном вязкостью и вариантом химического состава. Фармакологический эффект этих препаратов обусловлен их протезирующим действием на водянисто-муциновый слой прероговичной слезной пленки. Входящие в их состав гидрофильные полимеры (производные метилцеллюлозы и гиалуроновой кислоты, поливиниловый спирт, поливинилпирролидон и др.) смешиваются с остатками нативной слезы и образуют собственную прероговичную пленку. «Искусственную слезу» закапывают в конъюнктивальную полость больного глаза с периодичностью 4-6 раз в день. В результате разрывы слезной пленки возникают реже и существенно повышается ее стабильность. Ниже представлен перечень современных препаратов «искусственной слезы», зарегистрированных в нашей стране.
Препараты низкой вязкости:
— Слеза натуральная (Alcon);
— Оксиал (Santen);
— Офтолик (Promed Exports);
— Лакрисифи (Sifi);
— Хило-Комод (Ursapharm);
— Гипромелоза-П (Unimed Pharma);
— Дефислез (Синтез);
— Визмед-лайт (Robert′s Healthcare Int.).
Препараты средней вязкости:
— Лакрисин (Spofa);
— Визмед, Визмед-мульти (Robert′s Healthcare Int.).
Препараты с трансформационным эффектом (трансформируются из жидкости в гель при закапывании):
— Систейн (Alcon);
— Систейн Ультра (Alcon) /Доступен в России с февраля 2011 года/.
Глазные гели:
— Офтагель (Santen);
— Видисик (Bausch & Lomb);
— Визмед-гель (Robert′s Healthcare Int.).
Особо вязкие:
Вит-А-ПОС (Ursapharm).
Несмотря на достаточно большой ассортимент препаратов «искусственной слезы», каждый из них имеет свою «нишу» в лечении больных с рассматриваемым заболеванием. Так, препараты низкой вязкости более эффективны при легких формах, препараты средней вязкости и гели — при ССГ средней степени тяжести, а также тяжелых и особо тяжелых формах ксероза. Препараты Систейн и Систейн Ультра применяются при различной степени тяжести ССГ, так как способны становиться более или менее вязкими в зависимости от тяжести состояния (табл. 3). Препараты, содержащие в своем составе стимуляторы регенерации, целесообразно назначать при выраженных дегенеративных изменениях глазной поверхности, бесконсервантные «искусственные слезы» — при ношении контактных линз и при особо тяжелом синдроме «сухого глаза».
Стимуляция слезопродукции служит дополнительным медикаментозным способом увлажнения глазной поверхности. Среди различных мероприятий рассматриваемой направленности (магнитои лазеростимуляция, субконъюнктивальное введение трофических коктейлей на основе аутоплазмы крови) внимания заслуживает системное введение трентала. Так, по данным Луцевич Е.Э. и соавт. (2005), прием трентала по 100 мг — 2-3 раза в день в течение 2 мес. приводит к заметному увеличению основной слезопродукции.
Обтурацию слезоотводящих путей (полимерными обтураторами или хирургическими вмешательствами) используют либо при неэффективности медикаментозной терапии, либо при потребности в чрезмерно частом (свыше 6 раз в день) закапывании «искусственной слезы». Рассматриваемые мероприятия, как и операцию по пересадке слюнных желез в конъюнктивальную полость, обычно осуществляют в условиях офтальмологического стационара, куда и следует направить таких больных.
Купирование воспалительного процесса в тканях глазной поверхности служит важным звеном медикаментозной терапии синдрома «сухого глаза».
Среди препаратов рассматриваемой направленности наиболее доступными и достаточно эффективными оказались глюкокортикостероиды, безопасное применение которых возможно лишь при условии полной эпителизации роговицы. В указанных целях хорошо зарекомендовали себя инстилляции в конъюнктивальную полость дексаметазона в разведении 1:10 в гемодезе (или полиглюкине). Препарат закапывают с частотой 1-2 раза в день, продолжительность инстилляций определяют индивидуально.
Вместе с тем, даже при таком минимальном дозировании препарата, необходим контроль за толщиной роговицы, особенно в местах ее изначального истончения.
Системное применение тетрациклина (по 20 мг 2 раза в день курсами по 2 месяца) оказывает стимулирующий эффект на секрецию мейбомиевых желез век, продуцирующих липидный слой слезной пленки. Данное терапевтическое мероприятие призвано уменьшить испаряемость слезной пленки. Кроме того, клинический эффект тетрациклина связан с ингибированием выработки медиаторов воспалительной реакции в тканях глазной поверхности.
Инстилляции аутосыворотки крови (3-4 раза в день) наряду с эффектами «биологической искусственной слезы» позволяют уменьшить выраженность воспалительного процесса, а также стимулировать пролиферацию в тканях глазной поверхности за счет содержащихся в ней биологически активных веществ.
Существенным клиническим эффектом при тяжелом и особо тяжелом роговично-конъюнктивальном ксерозе обладают препараты 0,01% раствора циклоспорина-А (Restasis, фирма Allergan и др.). Препарат инстиллируют в конъюнктивальную полость больного глаза с частотой 2 раза в день в течение 3 месяцев, при необходимости курс лечения продлевают. Эффект этого известного цитостатика основан на уменьшении лимфоидной инфильтрации, а также на предупреждении выброса провоспалительных цитокинов в тканях слезных желез и конъюнктивы.
Метаболическая терапия показана больным с роговичноконъюнктивальным ксерозом, осложненным дегенеративными изменениями роговицы и конъюнктивы. Эффективными при ксерозе глазной поверхности являются препараты на основе искусственной слезы, содержащие в своем составе стимулятор регенерации декспантенол (Корнерегель, Bausch&Lomb; ХилозарКомод, Ursapharm, Гипромелоза-П, Unimed Pharma, Баларпан НЭП). Препараты инстиллируют в конъюнктивальную полость с частотой закапывания «искусственной слезы» соответствующей вязкости.
Отсутствие нормального блеска конъюнктивы, а также ее дегенеративные изменения служат показанием к 3-4-кратному местному применению препарата витамина А — ВитА-ПОС (Ursapharm), призванного нормализовать функцию бокаловидных клеток конъюнктивы, вырабатывающих муцин.
