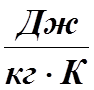Относительная
ошибка определения теплоемкости
вычисляется по формуле
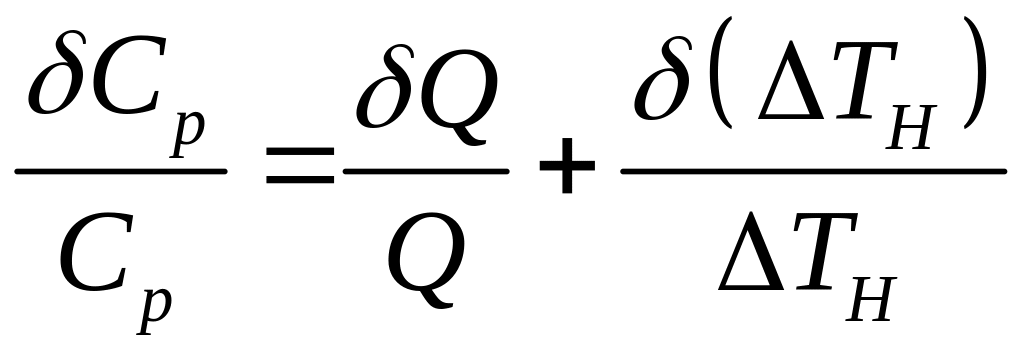
. (23.6)
Погрешность
определения
![]()
зависит от точности поддержания
адиабатических условий и линейности
температурного хода системы и составляет
около
![]()
1
10-4
К. Таким образом, ошибка в измерении
теплоемкости из-за неопределенности
хода в зависимости от
составляет:
При
= 1 градус ![]()
/
=1
10-2 %
При
= 1 10-2
градуса
/
=1
%.
Эта
ошибка может существенно возрастать
при большом времени установления
термодинамического равновесия образца,
что довольно часто наблюдается при
исследовании фазовых переходов первого
рода.
Ошибка
в определении количества тепла
,
подведенного к образцу, слагается из
ошибок измерений напряжений
и
потенциометром, ошибки измерения времени
нагрева секундомером и класса точности
используемого эталонного сопротивления.
Все это приводит к небольшой величине
![]()
0,1 %.
Таким
образом, при
= 1 К максимально возможная расчетная
погрешность определения теплоемкости
составляет
![]()
%.
23.4. Калориметрический сосуд
Калориметрический
сосуд представляет собой не только
контейнер для образца, но также является
вполне определенной частью аппаратуры,
в которой подведенное тепло и
соответствующее изменение температуры
тщательно измеряются. Простейший
калориметрический сосуд — вакуумный
контейнер, снабженный подходящими
термометром и нагревателем, а также
имеющий устройство для введения образца
внутрь и аппаратуру для подачи
теплообменного газа, облегчающего
установление теплового равновесия.
Общие
требования к такому калориметрическому
сосуду обычно сводятся к следующему.
Этот сосуд должен быть достаточно
прочным, чтобы выдержать перепад
давлений, равный, по крайней мере, 1 атм.;
не должен химически реагировать с
образцом; должен иметь хорошую
теплопроводность и хороший тепловой
контакт системы нагреватель — термометр
— калориметрический сосуд — образец.
Желательно,
что бы теплоемкость калориметра была
мала по сравнению с теплоемкостью
образца. Кроме того необходимо обеспечить
удобство заполнения калориметра
образцом.
Для
измерений теплоемкости порошкообразных
материалов целесообразно также
использовать внутренние хорошо проводящие
тепло перегородки для улучшения
выравнивания температуры внутри образца.
23.5. Измерения в режиме непрерывного нагрева
В
методе непрерывного нагрева, энергия
к нагревателю образца подается постоянно.
В этом методе производная от температуры
по времени определяется для тех моментов
времени, при которых измеряется подводимая
мощность, теплоемкость
![]()
рассчитывается из соотношения:

(23.7)
В
идеальном случае метод постоянного
(непрерывного) нагрева требует мгновенного
распределения тепла по калориметрическому
сосуду и его содержимому. Подвод энергии
делают достаточно малым, чтобы отклонение
температуры в любой части калориметрической
системы от наблюдаемой усредненной
температуры было незначительным.
Наиболее
часто этот метод используется для
квазистатического термографирования
в области фазового перехода. При этом
скорости нагрева или охлаждения
выбираются малыми
![]()
град/сек.
В
режиме непрерывного нагрева предварительно
устанавливается нулевая разность
температур между фурнитурой с образцом
и адиабатической оболочкой. В этом
случае джоулево тепло, выделяемое на
нагревателе, определяет рост температуры
в соответствии с формулой. Для снятия
термограмм в режиме охлаждения
осуществляется снижение до необходимого
уровня температуры адиабатической
оболочки относительно температуры
образца путем подачи напряжения
на вход системы регулирования
адиабатических условий. Так как скорость
изменения температуры образца зависит
от его теплоемкости, то для области
фазового перехода первого и второго
рода вид зависимости
![]()
будет разным. В точке фазового перехода
второго рода теплоемкость изменяется
скачком, соответственно в зависимости
будет излом. В случае фазового перехода
первого рода теплоемкость принимает
аномально большие значения, связанные
со скрытой теплотой перехода. Поэтому
температура исследуемого образца при
нагреве (охлаждении) не будет меняться
до тех пор, пока не завершится поглощение
(выделение) скрытой теплоты. Это приводит
к тому, что при температуре фазового
перехода на термограмме будет наблюдаться
горизонтальный участок.
Из
термограммы в режиме нагрева скрытая
теплота
вычисляется как
![]()
,
где
![]()
— мощность нагрева,
![]()
— время поглощения, определяемое
продолжительностью горизонтального
участка. Чувствительность метода
термограмм высока и позволяет
регистрировать тепловые эффекты 0,5 10-4
— 10-3 Дж.
Кроме
величины скрытой теплоты и точного
значения температуры перехода метод
термограмм позволяет получить величину
температурного гистерезиса путем
сравнения термограммы в режиме нагрева
и охлаждения. Поскольку термометр
вынесен на адиабатическую оболочку,
при определении температуры перехода
в режиме охлаждения необходимо учитывать
разность температур между образцом и
оболочкой.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
8
Контрольные задания
1. В чем заключается метод электрического нагрева для определения
теплоемкости твердых тел ?
2. Выведите формулу для экспериментального определения теплоемкости.
3. Почему во время эксперимента нагревание пустого калориметра и
калориметра с образцом необходимо производить при одной и той же
мощности нагревателя?
4. Чем ограничена максимально допустимая температура нагревания
калориметра?
5. Основные источники ошибок данного метода измерений .
8
Контрольные задания
1. В чем заключается метод электрического нагрева для определения
теплоемкости твердых тел?
2. Выведите формулу для экспериментального определения теплоемкости.
3. Почему во время эксперимента нагревание пустого калориметра и
калориметра с образцом необходимо производить при одной и той же
мощности нагревателя?
4. Чем ограничена максимально допустимая температура нагревания
калориметра?
5. Основные источники ошибок данного метода измерений.
ЛАБОРАТОРНАЯ РАБОТА № 14
ОПРЕДЕЛЕНИЕ УДЕЛЬНОЙ ТЕПЛОЕМКОСТИ ТВЕРДЫХ ТЕЛ МЕТОДОМ
НАГРЕВАНИЯ.
Цель
работы: определение удельной
теплоемкости твердого тела и проверка закона Дюлонга и Пти.
Принадлежности: установка, исследуемые тела, секундомер, термопара,
гальванометр типа М.
ТЕОРЕТИЧЕСКОЕ
ОБОСНОВАНИЕ.
Удельной теплоемкостью вещества называется физическая величина,
численно равная количеству теплоты ![]() , которое надо сообщить, чтобы нагреть 1кг вещества на
, которое надо сообщить, чтобы нагреть 1кг вещества на
1К.
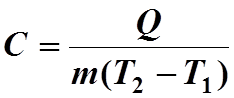 (1)
(1)
Эта формула справедлива в том случае, если
теплоемкость изменяется незначительно с изменением температуры. С учетом
зависимости теплоемкости от температуры, формула для С запишется
в виде:
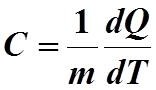 (2)
(2)
Формула (2) дает действительную теплоемкость
для каждой данной температуре, а формула (1) — среднюю теплоемкость в
интервале температур от Т1 до Т2.
У большинства тел с повышением температуры
теплоемкость увеличивается. Количество теплоты, необходимое для нагревания тела
от температуры Т1 до Т2 будет
равно:
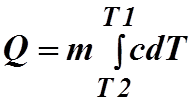 (3)
(3)
Теплоемкость тела можно найти, если известно
количество тепла ![]() , подведенного к телу, и
, подведенного к телу, и
изменение температуры ![]() :
:
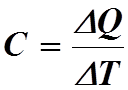 (4)
(4)
В данной работе температуру исследуемого образца
измеряют термопарой — спай двух разнородных металлов. Тепло подводится за счет
электрического нагревателя и определяется формулой:
![]() (5)
(5)
Вследствие теплопроводности стенок калориметра часть
энергии рассеивается в окружающей среде, поэтому оставшееся в калориметре количество
тепла будет:
![]() (6)
(6)
где l — коэффициент теплопроводности стенок калориметра,
T- температура тела,
Tк
— комнатная температура,
Dt – время
нагревания.
Тогда, используя (4)
получим, что:
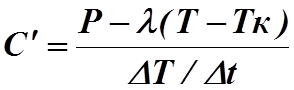
![]() (7)
(7)
Теплоемкость калориметр С0
определятся отдельно. Если не давать теплу заметных перегревов и производить
все измерения при комнатных температурах, то утечка тепла будет небольшой.
Однако при небольших нагревах возникает большая погрешность в измерении DT=T-Tк. Чтобы исключить эту трудность, измерения необходимо
производить следующим образом. Для широкого интервала температур определяют
скорость нагревания тела DT/Dt. Затем по полученным данным строят график зависимости 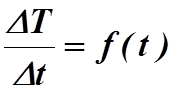 .
.
Экстраполируя график на температуру T=Tк ,
определяют скорость нагревания при комнатной температуре 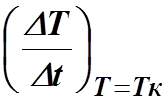
![]() .
.
Подставив полученные значения в формулу (7) и учтя, что при Т=Тк
,l(T-Tк)=0 имеем:
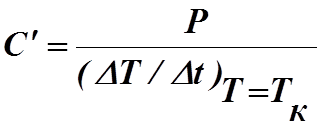 (8)
(8)
Описание
установки
2.ОПИСАНИЕ УСТАНОВКИ.
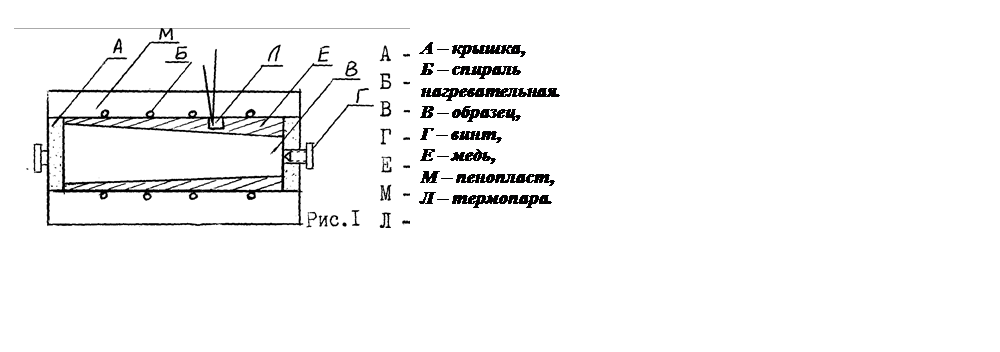
Рис. 14.1
Установка (рис.14.1)
состоит из калориметра с пенопластовой изоляцией. Внутренние стенки калориметра
выполнены из материала с высокой теплопроводностью. Для обеспечения надежного
теплового контакта исследуемые образцы и стенки калориметра выполнены в форме
усеченных конусов и плотно прилегают друг к другу. В теплоизолированную стенку
калориметра вмонтированы электронагреватель и термопара. Для выталкивания
образца служат плоскогубцы.
Cхема включения нагревателя Н
изображена на рис.14.2.
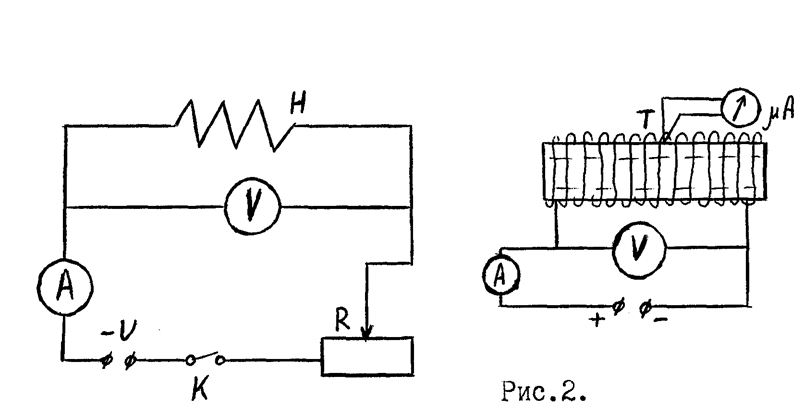
Рис. 14.2 Схема подключения нагревателя Н.
ПОДГОТОВКА
И ПРОВЕДЕНИЕ ИЗМЕРЕНИЙ.
1.
Подготовить калориметр к работе.
Установить термопару в гнездо калориметра до упора.
2.
Замкнуть ключ (рис14.2) и
установить ток в 3-4 А. Выключить нагреватель.
3.
Установить предел
измерения на деление ![]() либо 5mVи
либо 5mVи
нуль гальванометра.
4.
Замкнуть цепь нагревателя,
одновременно включить секундомер. Через каждые 2мин. записывать
показания гальванометра в течении 20мин.
5.
Определить мощность
нагревателя по показаниям амперметра и вольтметра P=IU.
6.
Построить график
зависимости температуры от времени T=f(t), используя
градуировочный график термопары n=f(T).
7.
На основе зависимости T=f(t),
постороить график зависимости скорости нагревания калориметра от температуры 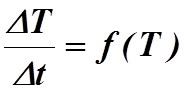 . Для этого ось абсцисс графика T=f(t)
. Для этого ось абсцисс графика T=f(t)
разделить на 10-12 одинаковых отрезков и для каждого из них определить тангенс
угла наклона 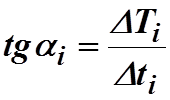 . По полученным данным значениям
. По полученным данным значениям
![]() посторить график
посторить график ![]() ,
,
где T=Tср. для
данного интервала температур.
Произведя
экстраполяцию этого графика на Тк найти значение 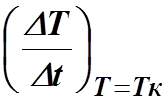
8.
Подставить значение
скорости нагрева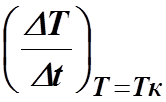 в формулу (8) и найти
в формулу (8) и найти
теплоемкость калориметра С0.
9.
Охладить калориметр,
поместить в него исследуемое тело, предварительно взвесив его, найти
теплоемкость ![]() по описанной методике (п.4-8). Теплоемкость
по описанной методике (п.4-8). Теплоемкость
исследуемого образца равна CT=![]() -C0.
-C0.
Полученные результаты занести в таблицу № 14.1 .
10.
Удельную теплоемкость
найти по формуле: 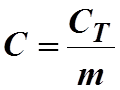 , где m– масса
, где m– масса
образца.
11.
Рассчитать молярную
теплоемкость по формуле 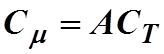 , где А –
, где А –
атомная масса вещества (для одноатомных веществ и молярная масса совпадают), СТ
– удельная теплоемкость тела.
12.
Определите основные
источники погрешности данного метода измерения.
ЭКСТРАПОЛЯЦИЯ
— приближенное определение значений функции f (x) в точках х,
лежащих вне отрезка [а,
в], по ее значениям f1…fi , в
точках хi
, принадлежащих отрезку [а, в].
Таблица № 14.1
|
I, A |
U В |
t, мин |
n, дел |
T, 0С |
0С/c |
Tср 0C |
Tк 0C |
|
с, |
с/, |
|
|
|
|||||||||||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
|
Калориметр |
0 2 4 … 20 |
||||||||||
|
Калориметр + исследуемое тело |
0 2 4 … 20 |
КОНТРОЛЬНЫЕ ВОПРОСЫ.
1. Что называется теплоемкостью? В каких единицах
она измеряется?
2. Классическая и квантовая теория теплоемкости.
3. В чем состоит закон Дюлонга и Пти?
- « первая
- 3
- 4
- 5
 (Назад)
(Назад) (Cкачать работу)
(Cкачать работу)
Функция «чтения» служит для ознакомления с работой. Разметка, таблицы и картинки документа могут отображаться неверно или не в полном объёме!
коэффициента , определить теплоемкость образца по формуле , где – ток, идущий через нагреватель; – напряжение на нагревателе; – масса образца.Вычислить молярную теплоемкость вещества по формуле , где μ-молярная масса образца (табл. величина).Оценить погрешность измерений.
Для оценки относительной погрешности данной формулы необходимо произвести следующие действия:
,
где — относительная погрешность амперметра,
— относительная погрешность вольтметра,
— относительная погрешность формулы, использовавшейся для вычисления массы.
,
где -абсолютная погрешность амперметра ( написана на приборе)
– показание амперметра
,
где — абсолютная погрешность вольтметра ( написана на приборе)
– показание вольтметра Контрольные вопросы.
Как с помощью метода электрического нагрева определить теплоемкость твердых тел?Выведите формулу для экспериментального определения теплоемкости методом нагрева.Почему во время эксперимента нагревание пустого калориметра и калориметра с образцом необходимо производить при одной и той же мощности нагревателя?Чем ограничена максимально допустимая температура нагревания калориметра?Основные источники ошибок данного метода измерений.
Литература:
Б. Н. Юдаев «Техническая термодинамика. Теплопередача : учебник для неэнергетич. спец. втузов» — М.: Высш. шк., 1988.-479 с. А. А. Детлаф «Курс физики. Учебное пособие для втузов» — М.: Высш. шк.,
1989 – 608с.
- « первая
- 3
- 4
- 5
Интересная статья: Быстрое написание курсовой работы

Более быстрый вариант температурной калибровки заключается в создании калибровочной кривой для одной заданной скорости сканирования (при которой в дальнейшем планируется проводить измерения образцов).
В современных ДСК в стандартный пакет анализа, как правило, входит функция создания калибровочной кривой. Выходящий экспериментальный сигнал формируется уже с учетом калибровки по температуре.
1.6.2. Калибровка по теплоте
Коэффициент KQ определяют по энтальпиям фазовых переходов (плавление, полиморфизм) стандартов.
H 0
KQ = tF pt Tonset . (1.6.2.1)
∫(DSC − DSCBL )dt
tS
Все операции проводят в тех же экспериментальных условиях, в которых планируется проводить измерения образцов (скорость и направление изменения температуры, скорость потока газа, конструкция и материал тиглей). В связи с тем, что калибровочный коэффициент существенно зависит от температуры, его значение определяют не менее чем в трех точках, полностью охватывающих интересующий диапазон температур.
Ниже перечислены дополнительные требования к стандартам для калибровки по теплоте.
1Небольшая протяженность пика (позволяет не учитывать на этом участке зависимость KQ от температуры (времени).
2При калибровке по энтальпии плавления рекомендуется не использовать стандарты с большой площадью поверхности (поликристаллические препараты, стружка).
3Сила адгезии стандарта к материалу тигля не должна существенно изменяться в результате фазового перехода.
Источник ограничений 2 и 3 заключается в следующем. Энтальпией реакции (в том числе и фазового перехода) называется теплота, выделившаяся или поглотившаяся в результате реакции, при
1постоянном давлении и температуре,
2отсутствии немеханических видов работ.
Фазовые переходы протекают при постоянной температуре, и в этом случае условие 1 соблюдается всегда. Однако немеханические виды работ могут присутствовать.
1Работа образования поверхности δW =γdσ существенно отличается от 0, если в результате
процесса площадь поверхности образца значительно меняется (плавление мелкодисперсных образцов с образованием одной капли расплава).
21
2При существенном изменении силы адгезии образца к материалу тигля фазовый переход сопровождается работой адгезии.
При калибровке в режиме охлаждения необходимо учитывать эффект переохлаждения
|
Tfrez |
|
|
frez H o(T )= ∫(C p,solid −C p,l )dT . |
(1.6.2.2) |
Tmelt
Точность измеренной теплоты процесса с учетом калибровки обычно составляет порядка 5%. В некоторых случаях эту величину можно понизить до 1%.
Функция создания калибровочной кривой, как правило, входит в стандартный пакет анализа современных ДСК, и выходящий экспериментальный сигнал формируется уже с учетом калибровки по теплоте.
1.6.3. Калибровка по тепловому потоку
Коэффициент пропорциональности KΦ определяют по известной теплоемкости стандарта в условиях, идентичных измерениям образцов во всем интересующем температурном диапазоне
|
по |
соотношению, |
полученному |
из |
(1.3.1.2) |
и |
(1.4.2.5) |
|
|
KΦ = |
DSCSt − DSCzeroline |
. |
(1.6.3) |
||||
|
βC p,St |
Измерения образца и стандарта необходимо проводить в одном тигле с использованием одной нулевой линии. В качестве стандарта рекомендуется синтетический сапфир (α-Al2O3). Массу стандарта подбирают таким образом, чтобы тепловой поток был близок по величине к тепловому потоку, генерируемому исследуемыми образцами.
Для ДСК теплового потока точность определения КΦ составляет порядка 1 – 1.6%.
22

p,St
2. Практическое использование метода ДСК
2.1. Измерение теплоемкости веществ2
Метод ДСК является самым быстрым способом определения величины изобарной теплоемкости вещества в широком диапазоне температур. Нижний предел определяется температурой кипения азота (~–170ºС), верхний предел – конструкцией конкретного прибора и материалом тиглей (поскольку стандартные ячейки изготавливают из алюминия, максимально допустимая температура обычно составляет 600ºС). Однако точность измерения теплоемкости методом ДСК уступает точности метода адиабатической калориметрии по ряду причин.
1В методе ДСК больше относительная погрешность при определении массы образца и измерениях, поскольку эксперименты проводятся с малой (порядка нескольких миллиграмм) величиной навески.
2Сравнительно высокая скорость сканирования (5 – 20º/мин) приводит к возникновению заметного градиента температур в объеме образца.
3В методе ДСК значительны неучтенные потери тепла за счет конвекции и теплового излучения.
В этой связи для получения достоверных значений рекомендуется проводить не менее трех независимых измерений теплоемкости и результаты статистически обрабатывать.
Способ расчета значений Cр из экспериментального сигнала основан на следующих соотношениях
|
DSCS +pan − DSCzeroline = KΦβmS C p,S |
||||||||
|
KΦ = |
DSCSt+pan − DSCzeroline |
, |
(2.1.1) |
|||||
|
βmSt C p,St |
||||||||
|
C p,S = |
DSCS +pan − DSCzeroline |
m |
St |
C p,St |
||||
|
DSCSt+pan −DSCzeroline |
||||||||
|
mS |
где DSCS+pan, DSCSt+pan – экспериментальный сигнал от образца (S) и тигля (pan), в который образец помещен, и стандарта (St) и тигля соответственно, DSCzeroline – экспериментальный сигнал от пустого тигля (нулевая линия), KФ – коэффициент чувствительности по тепловому потоку, β – скорость изменения температуры в измерительной системе, m – масса, C p,S ,C –
удельная теплоемкость. Величина коэффициента пропорциональности KФ существенно зависит от условий эксперимента и теплофизических и физических свойств образца. В этой связи при измерении теплоемкости важно соблюдать следующие правила.
1Серию экспериментов (измерения нулевой линии, образца и стандарта) проводить в одинаковых экспериментальных условиях (желательно, в один день).
21. ASTM E 1269 – 95. 2. Hohne G.W.H., Hemminger W.F., Flammersheim H.J.. Differential Scanning Calorimetry.
Second Edition. Springer, Berlin, 2003
23
2Серию экспериментов проводить в одном и том же тигле, тигель в приборе располагать одинаковым образом.
3Использовать стандарт, близкий по физическим и теплофизическим характеристикам к исследуемому образцу.
Тщательное соблюдение этих условий позволяет добиться хорошей воспроизводимости (доверительный интервал не превышает 0.5%) и точности (отклонения составляют 1 – 2%) измеренных величин теплоемкости.
Величина навески образца не стандартизована. Ее рекомендуется подбирать таким образом, чтобы сигнал ДСК от образца и стандарта имел близкую величину, что снижает суммарную погрешность при расчете по соотношению (2.1.1).
Существует несколько источников ошибок при измерении теплоемкости методом ДСК.
1 Изменение положения тигля в ячейке при измерении нулевой линии, образца и стандарта. Сигнал нулевой линии зависит, в том числе, от теплового контакта между дном тигля и сенсором, который может измениться при изменении положения тигля в ячейке. Для точного выполнения соотношений (2.1.1) необходимым условием является неизменность сигнала нулевой линии.
2 Различие в теплофизических и физических характеристиках образца и стандарта делает равенство коэффициентов пропорциональности нестрогим KΦ,S ≈ KΦ,St .
3 Отличие средней температуры образца от измеряемой температуры. Данный фактор устраняется путем соответствующей температурной коррекции (см. разделы 1.4.2.2, 1.4.2.3).
4 Дрейф нулевой линии. Сигнал нулевой линии в некоторой степени (крайне незначительно) зависит от внешних условий – в первую очередь, от температуры в помещении. В случае, когда измерение занимает продолжительное время (широкий температурный интервал, низкая скорость изменения температуры), внешние условия могут измениться, что приводит к непредсказуемому и невоспроизводимому дрейфу нулевой линии. В этой связи желательно, чтобы температурный интервал измерений не превышал 200º при β = 10º/мин. Учесть дрейф нулевой линии можно по изотермическим сегментам на экспериментальной кривой в начале и в конце измерения (рис. 2.1.1). В изотермическом режиме вся измерительная система находится при постоянной температуре, и тепловой поток (сигнал ДСК) равен 0. Обусловленные дрейфом отклонения экспериментального сигнала от нулевого значения в конце измерения можно скорректировать путем вычитания из сигнала
|
прямой |
DSC(t2 )− DSC(t1 ) |
|||
|
DSCiso (t)= DSC(t )+ |
(t −t ). |
(2.1.2) |
||
|
1 |
1 |
|||
|
t2 −t1 |
24
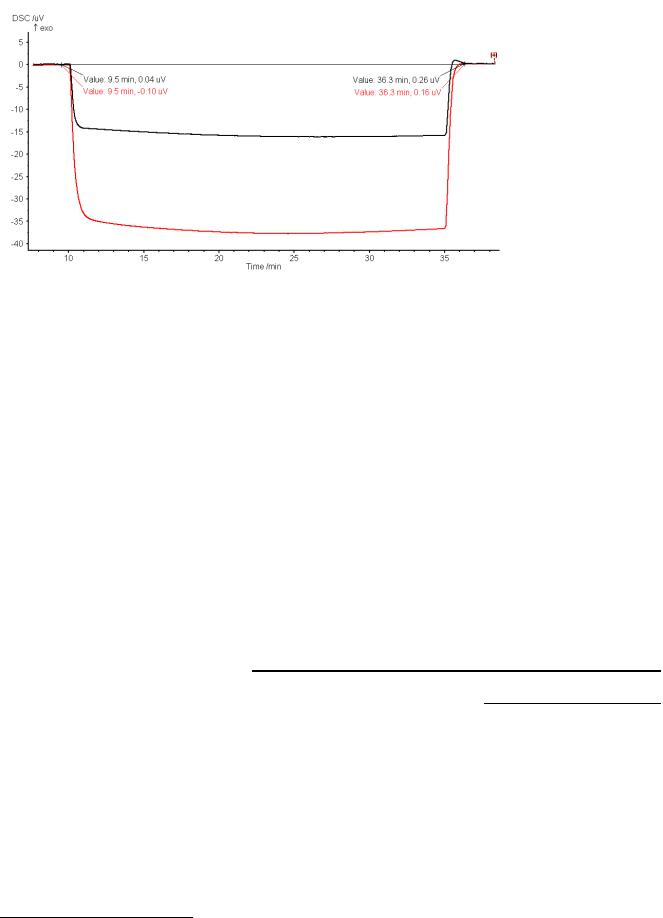
Рисунок 2.1.1. Экспериментальные сигналы ДСК стандарта (синтетический сапфир, черная кривая) и образца (LiCoO2, красная кривая); t1 = 9.5 мин, t2 = 36.3 мин
Измеренные температурные зависимости теплоемкости можно использовать для расчета
ряда термодинамических функций.
1 Интегрирование экспериментальной кривой позволяет определить температурные вклады в
|
энтальпию |
и |
энтропию |
образца |
|||||
|
T2 |
||||||||
|
HT2 − HT1 = ∫C p dT |
||||||||
|
T1 |
. |
(2.1.3) |
||||||
|
T2 |
C p |
|||||||
|
ST |
− ST |
= |
∫ |
dT |
||||
|
T |
||||||||
|
2 |
1 |
|||||||
|
T1 |
2Аппроксимация экспериментальной зависимости Cp = f(T) полиномом, и экстраполяция полинома в область низких температур позволяет оценить абсолютное значение энтропии
|
при |
Cp |
заданной |
температуре |
|
|
T |
||||
|
S(T )= ∫ |
dT . |
(2.1.4) |
||
|
0 |
T |
2.2.Определение энтальпии химических реакций
ифазовых переходов3
Теплота процесса пропорциональна площади пика на экспериментальной кривой (см. (1.4.2.4.2)). Способы моделирования базовой линии описаны в разделе 1.4.1.2.
Для корректного определения энтальпии химических реакций при подготовке образца необходимо учитывать следующее. Прессование препарата можно проводить только тогда, когда реакция протекает между твердыми веществами без выделения газообразных продуктов. В противном случае прессование затруднит контакт внутренних слоев твердого реагента с
3 1. Hohne G.W.H., Hemminger W.F., Flammersheim H.J.. Differential Scanning Calorimetry. Second Edition. Springer, Berlin, 2003. 2. Brown M.E. Introduction to Thermal Analysis. Techniques and Applications. Second Edition, Kluer Academic Publishers, Dordrecht, 2001
25
газом и отвод газообразных продуктов из зоны реакции, что исказит динамику процесса. В этой связи твердый реагент желательно диспергировать. Масса образца должна быть достаточной для хорошего соотношения полезный сигнал/шум и уменьшения относительной погрешности взвешивания.
Ниже перечислены основные источники ошибок при определении энтальпии химических реакций и фазовых переходов методом ДСК.
1 Зависимость калибровочного коэффициента KQ от температуры. При выводе соотношения (1.4.2.4.2) предполагалось, что интервал времени от начала до завершения процесса (а значит и температурный интервал) невелик, и зависимостью KQ = f(T(t)) за этот период можно пренебречь. Данное условие хорошо соблюдается для твердофазных фазовых переходов. Химические реакции могут протекать в большом (порядка 100º) температурном интервале, и сделанное приближение вносит погрешность в измеренную величину теплоты реакции.
2 Зависимость KQ от природы образца. Данный коэффициент определяется путем калибровки по стандартам, теплофизические и физические свойства которых неизбежно отличаются от свойств исследуемых образцов.
3 Изменение площади поверхности образца и силы адгезии в результате процесса связаны с протеканием немеханических видов работ в реакционной системе. Энтальпией реакции называется теплота, измеренная при отсутствии немеханических видов работ.
4 Изменение температуры образца за время реакции. Измерения методом ДСК, как правило, проводятся при сканировании оболочки по температуре. Таким образом, за период времени, в котором продолжается химическая или фазовая реакция, температура измерительной системы существенно изменяется. Это обстоятельство не имеет значения для фазовых переходов, поскольку температура образца остается постоянной до полного исчезновения одной из фаз и не зависит от температуры окружения. При протекании химических реакций температура образца до начала и после завершения реакции изменяется, что делает определение энтальпии реакции по площади пика на экспериментальной кривой некорректным. Существует два способа оценки энтальпий химических реакций из данных ДСК.
4.1. Измерение в изотермическом режиме. Образец вводится в измерительную ячейку, находящуюся при заданной температуре. В этом случае температура образца до и после процесса остается постоянной. Недостатком данного метода является погрешность, возникающая в результате нарушения стационарного режима в системе при введении образца (выход на стационарное состояние занимает не менее 10 – 15 с).
4.2. В случае, когда реакция не сопровождается образованием газообразных продуктов, поправку на изменение температуры образца можно внести по следующим соотношениям:
r H (Ts )= H P (Ts )− H R (Ts )= (H P (T f )− H R (Ts ))− (H P (T f )− H P (Ts ))
|
Tf |
Tf |
, |
(2.2.1) |
|
|
r H (Ts )= ∫C imp,ξ (T )dT − ∫C p,P (T )dT |
||||
|
Ts |
Ts |
где индексы s и f относятся к началу и завершению реакции, R и P – к реагентам и продуктам соответственно. Кажущуюся теплоемкость реакционной смеси можно рассчитать непосредственно из экспериментального сигнала ДСК после коррекции по
|
тепловому |
потоку |
и |
нулевой |
линии |
||
|
C imp,ξ = |
DSC(Ts < T < T f )− DSCzeroline |
. |
(2.2.2) |
|||
|
βKΦ |
26

Температурную зависимость теплоемкости продуктов реакции можно найти двумя способами.
4.2.3.Точное определение. Измерение теплоемкости образца после завершения реакции.
4.2.4.Оценка. Экстраполяция правого участка экспериментальной кривой в область
|
пика |
DSC(T > T f )− DSCzeroline |
(рис. |
2.2.1) |
|
|
C p,P = |
. |
(2.2.3) |
||
|
βKΦ |
Предварительно необходимо провести коррекцию сигнала по тепловому потоку и нулевой линии.
1
2
Рисунок 2.2.1. Оценка энтальпии первой стадии разложения Cu2CO3(OH)2; Ts = 200ºC, Tf = 500ºC; s H =1+2 −2 =1 =569.9 Дж/ г
В связи с вышесказанным метод ДСК можно использовать только для оценки энтальпий химических реакций.
2.3. Фазовые диаграммы бинарных систем4
Фазовые диаграммы отражают условия стабильности фаз в равновесной системе. Метод ДСК, как правило, используют для определения вида изобарных сечений фазовых диаграмм. На фазовых диаграммах полями называют области с двумя степенями свободы (в пределах поля на изобарном сечении можно менять и температуру, и состав без изменения фазового состава системы), моновариантами – области с одной степенью свободы (изменение температуры обуславливает изменение состава смеси и наоборот), нонвариантами называют точки, в которых степени свободы отсутствуют. Изменение фазового состава системы соответствует пересечению моноварианты на сечении фазовой диаграммы. При этом в системе протекает равновесный фазовый переход первого рода (плавление, кристаллизация, полиморфизм и т.д.). Любой фазовый переход первого рода сопровождается выделением или поглощением тепла.
4 1. Zhao J.-C.. Methods for Phase Diagram Determination. Elsevier, 2007, Chapter 5. 2. Hohne G.W.H., Hemminger W.F., Flammersheim H.J.. Differential Scanning Calorimetry. Second Edition. Springer, Berlin, 2003. 3. Шестак Я..
Теория термического анализа. Мир, Москва, 1987
27

Температуру данного процесса можно зафиксировать с помощью метода ДСК. Т.о., метод ДСК позволяет найти координаты моновариант на сечении фазовой диаграммы, т.е. определить температуру фазовых переходов для заданного состава системы (рис. 2.3).
Рисунок 2.35. Схема сигналов ДСК на примере простой эвтектической бинарной системы
2.3.1. Специфика эксперимента
2.3.1.1. Равновесие
При определении вида сечений фазовых диаграмм методом ДСК важно убедиться в том, что полученные результаты относятся к равновесным процессам в системе.
Скорость сканирования
Равновесным называется процесс, который протекает под действием бесконечно малой разности обобщенных сил на контрольной поверхности. Применительно к методу ДСК обобщенной силой является температура, поскольку все изменения в изучаемой системе (образце) происходят в результате его нагревания или охлаждения. Пусть при начальных условиях система находится в состоянии равновесия. Любое изменение условий (например, температуры) приведет к тому, что она выйдет из этого состояния. С течением времени образец снова достигнет состояния равновесия уже с новыми внешними условиями (при новой температуре). Время, необходимое для возвращения в равновесное состояние, называется временем релаксации. Для того чтобы процесс в образце протекал равновесно необходимо, чтобы его время релаксации было меньше, чем скорость изменения температуры в измерительной системе. Т.о., чем ниже скорость сканирования, тем выше вероятность того, что процесс в образце протекает равновесно.
С другой стороны уменьшение скорости сканирования приводит к понижению соотношения сигнал/шум, что негативно влияет на точность измерения.
5 Zhao J.-C.. Methods for Phase Diagram Determination. Elsevier, 2007, Chapter 5
28
Таким образом, при выборе условий экспериментов необходимо принять компромиссное решение относительно скорости изменения температуры в измерительной системе. Часто таким решением является скорость 2º/мин.
Масса образца
Массу образца для экспериментов следует подбирать на основании следующих соображений.
1Чем больше размер образца, тем больше градиент температур в его объеме.
2Чем ниже теплопроводность образца, тем больше градиент температур в его объеме.
3Чем меньше масса образца, тем меньше полезный сигнал ДСК, тем меньше соотношение сигнал/шум.
Здесь также следует найти компромисс между нежелательной разницей температур и точностью определения измеряемых величин. Оптимальные условия подбираются эмпирическим путем.
Диффузия в жидкой и твердой фазах
Конечная скорость диффузии в расплаве и, особенно, в кристаллической фазе приводит к неоднородности по составу образца после фазового перехода. Следующие меры можно предпринять для предотвращения связанных с этим фактором ошибок.
1 Проводить кристаллизацию и плавление образца при низкой скорости изменения температуры в измерительной системе. Оптимальную скорость сканирования находят эмпирическим путем для каждой отдельной системы.
2Проводить изотермический отжиг закристаллизованного образца при температуре, близкой к температуре плавления.
При представлении результатов по определению вида изобарных сечений фазовых диаграмм методом ДСК необходимо доказать, что равновесие в изученной системе было достигнуто. Обычно с этой целью для каждого состава проводят серию циклов нагревание/охлаждение. Доказательством является хорошая воспроизводимость результатов. В том случае, когда кристаллический образец подвергается изотермическому отжигу, доказательством того, что продолжительность отжига достаточна для достижения однородности по составу, является воспроизводимость результатов при последующем увеличении времени отжига.
29

2.3.1.2. Другие факторы, влияющие на результат измерений
Атмосфера в измерительной системе
Как правило, ДСК-эксперименты проводят в потоке газа. Скорость потока не должна быть слишком большой, чтобы уменьшить погрешность измерения в результате потери тепла за счет вынужденной конвекции. Обычно выбирают скорость 10 – 20 мл/мин. Очевидно, что газ не должен взаимодействовать с исследуемым образцом. Для уменьшения утечек тепла за счет конвекции, в измерительной системе следует использовать газ, обладающий невысокой теплопроводностью.
Тигель
Для определения вида сечений фазовых диаграмм, как правило, используются тигли, завальцованные крышкой с небольшим отверстием. Отверстие необходимо для сохранения условия постоянства давления в системе, в этой связи оно должно быть не слишком мало по сравнению с площадью испарения образца. С другой стороны, оно не должно быть слишком велико, чтобы минимизировать потери образца в результате сублимации/испарения.
Материал тигля подбирают на основании следующего:
1инертность по отношению к образцу и атмосфере,
2высокая теплопроводность для понижения инерционности измерительной системы.
2.3.2. Анализ экспериментальных данных
При изменении температуры меняется фазовый состав системы, и, следовательно, ее
|
энтальпия. |
В |
простейшем |
случае |
|
H (T )= const +CpT + |
m H (1− fs (T )). |
(2.3.2) |
Здесь H(T) – энтальпия системы, Сp – ее изобарная теплоемкость (предполагается, что Cp = Cp,L = Cp,S и не зависит от температуры), mH – энтальпия плавления системы (также полагается
|
независящей от температуры), |
fS (T )= |
nS |
= |
xL (T )− x0 |
– доля твердой фазы при температуре |
|
|
xL (T )− xS (T ) |
||||||
|
n |
Т, xL (T )= nB,L , xS (T )= nB,S – мольные доли второго компонента (В) в расплаве и твердой фазе nL nL
соответственно, х0 – исходная мольная доля второго компонента, n, nS, nL – общее число молей, число молей в твердой фазе и расплаве соответственно. На рисунке 2.3.2 представлены рассчитанные кривые температурной зависимости энтальпии простой бинарной эвтектической системы. Сплошные линии получены в предположении полной равновесности системы (состав твердой фазы одинаков в любой точке), пунктир – в предположении бесконечно малой
30
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
01.05.201512.56 Mб51ENLISH GRAMMAR (Understanding & Using).pdf
- #
Источники возможных ошибок при определении теплоемкости вещества?СРОЧНО
borovikovbogdan1989:
можете не смотреть,я предмет перепутал
Ответы
Ответ:
Ошибка при измерении теплоёмкости вещества объясняется тем что при вычислении.Мы не учитывали теплоёмкость километра и ещё при вычислении количества теплоты, не учитывали тепловые потери которые возникают при проведений измерений.Часть тепловой энергии уходит в окружающую среду.
Romashek:
Вот так пойдёт?
borovikovbogdan1989:
спасибо
Интересные вопросы
Предмет: Музыка,
автор: XBelo4kaX
Предмет: История,
автор: dimalazar1994
8
Контрольные задания
1. В чем заключается метод электрического нагрева для определения
теплоемкости твердых тел ?
2. Выведите формулу для экспериментального определения теплоемкости.
3. Почему во время эксперимента нагревание пустого калориметра и
калориметра с образцом необходимо производить при одной и той же
мощности нагревателя?
4. Чем ограничена максимально допустимая температура нагревания
калориметра?
5. Основные источники ошибок данного метода измерений .
8
Контрольные задания
1. В чем заключается метод электрического нагрева для определения
теплоемкости твердых тел?
2. Выведите формулу для экспериментального определения теплоемкости.
3. Почему во время эксперимента нагревание пустого калориметра и
калориметра с образцом необходимо производить при одной и той же
мощности нагревателя?
4. Чем ограничена максимально допустимая температура нагревания
калориметра?
5. Основные источники ошибок данного метода измерений.
Лабораторная работа №8ОПРЕДЕЛЕНИЕ ТЕПЛОЕМКОСТИ ТВЕРДЫХ ТЕЛЦель работы – определение теплоемкости образцов металлов калориметрическим методом с использованием электрического нагрева.Теория методаИз теории идеального газа известно, что средняя кинетическая энергияодноатомных молекул (изолированных частиц)3< ЕК >= ⋅ k ⋅ T ,2где k – постоянная Больцмана.Тогда среднее значение полной энергии частицы при колебательномдвижении в кристаллической решетке< U 0 >= 3 ⋅ k ⋅ T .Полную внутреннюю энергию одного моля твердого тела получим умножив среднюю энергию одной частицы на число независимо колеблющихсячастиц, содержащихся в одном моле, т.е.
на постоянную Авогадро NA:U =< U 0 > ⋅ N A = 3 ⋅ N A ⋅ k ⋅ T = 3 ⋅ R ⋅ T ,(8.1)где R – универсальная газовая постоянная, R = 8,31 Дж/(моль·К).Для твердых тел вследствие малого коэффициента теплового расширениятеплоемкости при постоянном давлении и постоянном объеме практически неразличаются. Поэтому, учитывая (8.1), молярная теплоемкость твердого телаdU(8.2)µ ⋅ С = µ ⋅ СV == 3 ⋅ R.dTПодставляя численное значение молярной газовой постоянной, получим:µC = 25 Дж/(моль·К)Это равенство, называемое законом Дюлонга и Пти, выполняется с довольно хорошим приближением для многих веществ при комнатной температуре.Со снижением температуры теплоемкости всех твердых тел уменьшаются, приближаясь к нулю при T→0.
Вблизи абсолютного нуля молярная теплоемкостьвсех тел пропорциональна Т3, и только при достаточно высокой, характерной длякаждого вещества температуре начинает выполняться равенство (8.2). Эти особенности теплоемкостей твердых тел при низких температурах можно объяснитьс помощью квантовой теории теплоемкости, созданной Эйнштейном и Дебаем.Для экспериментального определения теплоемкости исследуемое телопомещается в калориметр, который нагревается электрическим током. Если температуру калориметра с исследуемым образцом очень медленно увеличивать отначальной Т0 на ∆Т, то энергия электрического тока пойдет на нагревание образцаи калориметра:J ⋅ U ⋅ τ = m0 ⋅ c0 ⋅ ∆T + m ⋅ c ⋅ ∆T + ∆Q,(8.3)где J и U – ток и напряжение нагревателя; τ – время нагревания; m0 и m – массыкалориметра и исследуемого образца, c0 и с – удельные теплоемкости калориметра и исследуемого образца, ∆Q – потери тепла в теплоизоляцию калориметра и вокружающее пространство.Для исключения из уравнения (8.3) количества теплоты, расходованнойна нагрев калориметра, и потери теплоты в окружающее пространство, необходимо при той же мощности нагревателя нагреть пустой калориметр (без образца)от начальной температуры Т0 на ту же разность температур ∆Т.
Потери тепла вобоих случаях будут практически одинаковыми и очень малыми, если температура защитного кожуха калориметра в обоих случаях постоянная и равна комнатной:J ⋅ U ⋅ τ 0 = m0 ⋅ c0 ⋅ ∆T + ∆Q0 ,(8.4)Из уравнений (8.3) и (8.4) вытекаетJ ⋅ U ⋅ (τ − τ 0 ) = m ⋅ c ⋅ ∆T .(8.5)Уравнение (8.5) может быть использовано для экспериментального определения удельной теплоемкости материала исследуемого образца. Изменяя температуру калориметра, необходимо построить график зависимости разности времени нагрева от изменения температуры исследуемого образца: (τ-τ0) = f(∆T), поm⋅cможно определить удельную тепJ ⋅Uугловому коэффициенту которого Кα =лоемкость образца.Материал образцаДюральЛатуньСтальАтомная масса, кг/моль26,98·10-363,57·10-355,85·10-3Экспериментальная установкаДля определения теплоемкости твердых тел предназначена экспериментальная установка ФПТ1-8, общий вид которой показан на рис.
8.1.Образцы нагреваются в калориметре, схема которого показана на рис. 8.2.Калориметр представляет собой латунный корпус с коническим отверстием, куда вставляется исследуемый образец. На наружной поверхности корпусав специальных пазах размещается нагревательная спираль. Снаружи корпус калориметра теплоизолирован слоями асбеста и стекловолокна и закрыт алюминиевым кожухом.
Калориметр закрывается теплоизолирующей крышкой. Исследуемые образцы расположены в гнездах в блоке рабочего элемента 2. После окончания эксперимента образец можно вытолкнуть из конического отверстия корпусакалориметра с помощью винта. Для удаления нагретого образца из калориметра иустановки образца в нагреватель используется рукоятка, расположенная в специальном гнезде рядом с исследуемыми образцами.Температура калориметра измеряется цифровым термометром, датчиккоторого находится в корпусе калориметра. В блоке приборов 1 расположен источник питания нагревателя, мощность которого устанавливается регулятором«Нагрев».
Напряжение и ток в цепи нагревателя измеряется вольтметром и амперметром, которые расположены на передней панели блока приборов. Времянагрева калориметра измеряется секундомером, расположенным в блоке приборов. Секундомер приводится в действие при включении питания блока приборов.Атомные массы образцов приведены в таблице 8.1.Таблица 8.1№ п/п123Рисунок 8.1 Общий вид экспериментальной установки ФПТ1-8:1 – блок приборов; 2 – блок рабочего элемента, 3 – стойка, 4 – нагреватель,5 – исследуемые образцы.Порядок выполнения работы1.
Снять кожух блока рабочего элемента установки и подвесить его навинтах задней панели. Включить установку тумблером «Сеть».2. Пустой калориметр плотно закрыть крышкой. Включить тумблер «Нагрев». С помощью регулятора «Нагрев» установить необходимое напряжение вцепи.34598107512Рисунок 8.2 Схема калориметра:1 – образец; 2 – корпус; 3 – асбест; 4 – кожух; 5 – рукоятка; 6 – стекловолокно;7 – винт; 8 – датчик температуры;9 – нагреватель; 10 – крышка.U,BJ,A∆T,Kτ0 ,cτ,cτ — τ0,cc,Дж/(кг·К)Таблица 8.2µс,Дж/(моль·К)3.
При температуре калориметра t0=25 0C включить отсчет времени. Сделать 7-10 измерений времени нагрева пустого калориметра через интервал 1 0С.Результаты занести в таблицу 8.2.№изм.4. Выключить тумблер «Нагрев», открыть крышку и охладить калориметр до начальной температуры t0.5. Вращая винт влево, поместить в калориметр один из исследуемых образцов, взятый по указанию преподавателя. Плотно закрыть крышку калориметраи подождать 3 мин. для того, чтобы температуры калориметра и образца сравнялись.6. Включить нагреватель калориметра, установив такое же напряжение вцепи как и при нагревании пустого калориметра.7.
Включить отсчет времени при той же начальной температуре t0. Сделать 7-10 измерений времени нагревания калориметра с образцом τ через интервал температуры 1 0С. Результаты занести в таблицу 8.2.8. Регулятор «Нагрев» установить в крайнее левое положение, выключить тумблер «Нагрев», открыть крышку калориметра. Для удаления образца изкалориметра винт вращать вправо, после чего с помощью рукоятки вынуть нагре-тый образец.9.
Выключить установку тумблером «Сеть».4. Оценить погрешность результатов измерений.Обработка результатов измерений1. Построить график зависимости разности времени нагревания калориметра с образцом и пустого калориметра от изменения температуры калориметра(τ-τ0) = f(∆T) и определить угловой коэффициент Кα.2. Используя значение углового коэффициента Кα, определить удельнуюJ ⋅Uтеплоемкость образца по формуле С =⋅ Kα .m3. Используя данные таблицы 8.1, определить молярную теплоемкостьобразца.Контрольные задания1.
Какая величина называется теплоемкостью вещества, удельной и молярной теплоемкостью? В каких единицах СИ они измеряются?2. Выведите формулу для полной внутренней энергии и моля твердого тела.3. В чем особенности теплоемкостей твердых тел? Выведите формулу для молярной теплоемкости твердого тела4. Запишите и объясните закон Дюлонга и Пти.5. Рассчитайте, исходя из закона Дюлонга и Пти, удельные теплоемкости алюминия 23Al27 и железа 26Fe56.6. В чем заключается метод электрического нагрева для определения теплоемкости твердых тел?7. Выведите формулу для экспериментального определения теплоемкости.8. Почему во время эксперимента нагревание пустого калориметра и калориметрас образцом необходимо производить при одной и той же мощности нагревателя?9.
Чем ограничена максимально допустимая температура нагревания калориметра?10. Основные источники ошибок данного метода измерений..

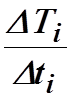
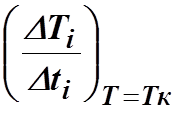 0С/c
0С/c