Содержание
- Точность метода МРТ
- Причины ошибок диагностики
- Достоверность ПЭТ КТ
- Как избежать постановки неправильного диагноза?
В случае с обследованием человеческого организма на наличие раковых заболеваний ни один из методов не может гарантировать 100% безошибочный результат. Для диагностики применяются ПЭТ КТ, МРТ, классическая КТ, УЗД — все они имеют свои плюсы и минусы. Рассмотрим более подробно МРТ и ПЭТ КТ. Могут ли они ошибаться? Если да, то каковы причины неверных результатов при диагностировании рака?
Точность метода МРТ
 Правильно поставленный диагноз является основным условием результативного лечения. Мировая медицинская практика показывает, что МРТ обследование заслуживает доверия. В результате его проведения получаются изображения тканей и сосудов высокой четкости. Обнаруженное новообразование специалист дифференцирует по признакам:
Правильно поставленный диагноз является основным условием результативного лечения. Мировая медицинская практика показывает, что МРТ обследование заслуживает доверия. В результате его проведения получаются изображения тканей и сосудов высокой четкости. Обнаруженное новообразование специалист дифференцирует по признакам:
- характер контура патологии;
- однородность содержимого;
- степень накопления контрастного вещества.
Это позволяет косвенно определить характер опухоли: доброкачественная или злокачественная. Окончательно подтвердить диагноз может только биопсия, но чем выше квалификация врача, выполняющего расшифровку, тем меньше возможность ошибки. Если соблюдать все правила проведения процедуры, то результат будет корректным.
Причины ошибок диагностики
Ошибки при заключении могут быть следствием неправильного размещения пациента на столе томографа, его движений при сканировании или появления артефактов на снимках. На всех изображениях, полученных при МРТ, есть разного рода артефакты, но они в большинстве случаев легко распознаются специалистом. Однако в некоторых ситуациях они могут имитировать патологические состояния, что требует от врача внимательности при расшифровке изображений.
Причины ошибок можно условно разделить на три группы:
- неправильная подготовка пациента к обследованию;
- недостаточная квалификация врача, проводящего процедуру;
- подбор неверной методики диагностики.
Нарушения процесса исследования из-за пациента
Одной из основных причин неправильных результатов МРТ является нарушение процесса диагностики пациентом. Чтобы подобного не случилось, человек должен:
 до начала обследования снять с себя предметы, в состав которых входит металл;
до начала обследования снять с себя предметы, в состав которых входит металл;- проинформировать лечащего врача о присутствии в теле имплантов из металла;
- в процессе обследования не совершать никаких телодвижений (соблюдать полную неподвижность).
Последний пункт имеет особое значение для точности результата. Малейшие шевеления пациента приводят к смазанности изображения. Именно поэтому лежать нужно не двигаясь, а это непросто при условии, что процесс длится достаточно долго.
Неверно подобранная методика
МРТ часто не может отличить раковые клетки от отечной жидкости и поэтому выдает неверный результат. Не всегда данный метод обследования может распознать опухоль головного мозга, а также легких из-за высокой воздушности и небольшого количества воды в тканях органов дыхания. Изучить состояние костных структур, используя МРТ, также не получится.
Для выявления новообразований лучше применить КТ. Компьютерная томография отлично справляется с поиском опухолей молочной железы и желудка, а МСКТ способна обнаружить образования величиной 2-3 мм.
Диагностические возможности аппарата напрямую зависят от его мощности. Снимки, полученные с помощью низкопольных установок, не обладают необходимой точностью. Для получения достоверных данных лучше применять оборудование с магнитным полем от 1,5 Тесла.
Недостаточная квалификация специалиста
Оборудование для МРТ очень точно воспроизводит изображение. Далее все снимки передаются рентгенологу, который должен их расшифровать. От его компетентности и уровня квалификации зависит постановка верного диагноза. Жировая клетчатка, мышцы, эпителий дают разный сигнал, поэтому иногда можно даже предположить из какой ткани состоит опухоль. К сожалению, многие врачи допускают ошибки в заключении из-за неверной расшифровки результатов.
Достоверность ПЭТ КТ
ПЭТ КТ (позитронно-эмиссионная томография, совмещенная с компьютерной томографией) — это исключительный способ радионуклидного обследования, при помощи которого осуществляется диагностика онкологических заболеваний, патологий ЦНС и эндокринной системы. Надежность исследования, в зависимости от исследуемого органа, колеблется в границах от 85 до 99%.
Несмотря на высокий процент точности, иногда ПЭТ КТ все же ошибается. Причиной этого являются разного рода объективные и субъективные факторы.
Основы работы метода
 Принцип работы ПЭТ КТ основывается на том, что раковые клетки активнее себя ведут в сравнении со здоровыми. В связи с этим поглощение и выделение продуктов жизнедеятельности носит усиленный характер. Так как ПЭТ КТ — это радионуклидный способ проведения обследования, то для обнаружения метаболических процессов, происходящих в организме, пациенту необходимо ввести РФП (радиофармпрепарат). РПФ — это безвредное вещество, не имеющее вкуса и запаха. В его состав входят радиоизотопы (фтор-18, углерод-11) и биохимические соединения (чаще всего глюкоза).
Принцип работы ПЭТ КТ основывается на том, что раковые клетки активнее себя ведут в сравнении со здоровыми. В связи с этим поглощение и выделение продуктов жизнедеятельности носит усиленный характер. Так как ПЭТ КТ — это радионуклидный способ проведения обследования, то для обнаружения метаболических процессов, происходящих в организме, пациенту необходимо ввести РФП (радиофармпрепарат). РПФ — это безвредное вещество, не имеющее вкуса и запаха. В его состав входят радиоизотопы (фтор-18, углерод-11) и биохимические соединения (чаще всего глюкоза).
Датчики ПЭТ фиксируют повышенный обмен РФП, как «горячую зону». КТ в это время делает множественные снимки, тем самым указывая точное место локализации патологии. Изображения, выполненные с применением радиофармпрепарата, накладываются поверх срезов, которые были получены при КТ.
Используя метод ПЭТ КТ, можно получить точную оценку строения органов и патологических процессов, узнать их характеристики. При КТ, УЗД и МРТ подобный анализ провести невозможно.
Главные причины ошибок
В основе ошибок ПЭТ КТ лежат следующие причины:
 параллельное существование еще одной патологии с аналогичными проявлениями;
параллельное существование еще одной патологии с аналогичными проявлениями;- низкое разрешение аппарата ПЭТ КТ;
- заболевание находится на ранней стадии развития;
- телодвижения пациента во время процедуры;
- неправильная подготовка к диагностике;
- присутствие на теле или одежде обследуемого предметов из металла;
- повышенный сахар в крови;
- передвижения пациента в момент распределения РПФ в организме;
- неправильное толкование срезов специалистами.
Как избежать постановки неправильного диагноза?
Для того, чтобы в результате обследования получить правильный диагноз, необходимо:
- правильно подготовиться к предстоящему процессу;
- заранее снять все предметы, в состав которых входит металл;
- не совершать никакой активности во время распределения контраста по организму и в период исследования;
- проинформировать врача о наличии серьезных заболеваний (например, сахарный диабет);
- проходить процедуру в специализированных центрах с высококвалифицированным персоналом и качественным оборудованием.
Поделитесь с друьями!
ПЭТ-КТ — это современный метод обследования, совмещающий позитронно-эмиссионную томографию (ПЭТ) и компьютерную томографию (КТ). Иногда метод называется просто ПЭТ. В его основе лежит регистрация гамма-излучения от введенного в организм радиофармпрепарата.
КАК ЧАСТО ОШИБАЕТСЯ ПЭТ-КТ, БЫВАЮТ ЛИ ОШИБКИ ПЭТ-КТ?
Вопрос важный, ведь это обследование проходят те, кому очень нужен точный диагноз!
Увы, ошибки диагностики при ПЭТ-КТ встречаются в определенном проценте случаев. Это обусловлено двумя факторами.
1. Объективный фактор, заключающийся в самой методике. В любом диагностическом методе, будь то КТ, МРТ или ПЭТ, изначально заложен определенный процент ошибок. Если мы возьмем какую-нибудь болезнь — например, рак молочной железы, то не все случаи рака молочной железы могут быть выявлены с помощью ПЭТ (это называется ложноотрицательный результат). Кроме того, иногда при отсутствии рака на снимках ПЭТ-КТ могут выявляться ее признаки (это называется ложноположительный результат). Есть несколько причин этого феномена: несовершенство аппаратуры, наличие сопутствующих болезней, имеющих сходную симптоматику, плохая выявляемость болезни на ранней стадии. Нужно отметить, что с каждым годом аппаратура ПЭТ-КТ становится все точнее, и поэтому процент ложных результатов постепенно уменьшается.
2. Субъективный фактор — более важный. Он обусловлен неверной трактовкой результатов ПЭТ-КТ. Врач, анализирующий снимки ПЭТ-КТ, может совершить ошибку и неправильно описать имеющиеся изменения! Нужно понимать, что любая аппаратура, даже самая современная — это всего лишь «железо» для получения изображений. А расшифровка изображений ПЭТ-КТ — это дело врача-радиолога, и от его опыта и знаний напрямую зависит достоверность диагностики.
Диагностические ошибки ПЭТ-КТ, обусловленные неправильной расшифровкой снимков, встречаются не так уж редко. В России этот метод только начинает развиваться. Количество квалифицированных специалистов по ПЭТ пока ограничено, и почти все они работают в нескольких профильных центрах в крупных городах (например, Институт мозга человека РАН). Встречается ситуация, когда в лечебное учреждение поставили новое оборудование ПЭТ, а опытного специалиста для работы на нем не найти. Это касается как государственных, так и частных центров ПЭТ.
В этих случаях не нужно отчаиваться. Если у вас или ваших лечащих врачей после проведения ПЭТ-КТ остаются вопросы по диагнозу, снимки можно проконсультировать у более опытного специалиста. Сегодняшняя ситуация такова, что такой специалист не обязательно должен жить в том же городе — результаты можно переслать ему по сети интернет.
ПЭТ-КТ В ДИАГНОСТИКЕ РАКА — КАК ИЗБЕЖАТЬ ОШИБОК?
Второе мнение по ПЭТ-КТ — распространенная услуга во всем мире. Для онкологических пациентов крайне важно не ошибиться с диагнозом — например, знать точную стадию рака, количество пораженных лимфатических узлов, достоверно исключить метастазы в печень, кости и другие органы. Пересмотр ПЭТ-КТ опытным врачом-диагностом — это способ свести риск ошибки к минимуму.
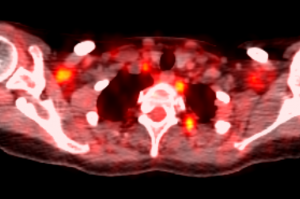
Может ли ПЭТ-КТ дать ошибку по метастазам? На примере — очаги накопления радиофармпрепарата [18F]-дезоксиглюкозы в подмышечной области и вдоль позвоночника, которые первоначально были расценены как метастазы в лимфатические узлы. Более внимательный анализ в ходе второго мнения показал, что эти очаги не являются злокачественной опухолью, а представляют собой участки бурого жира, отличающиеся повышенной метаболической активностью. На этом примере мы видим, как пересмотр результатов ПЭТ-КТ помог сделать диагноз менее опасным.
Заказать второе мнение по ПЭТ-КТ можно из любого города России, не выходя из дома. Врачи-радиологи Санкт-Петербургского Института мозга человека обладают огромным опытом в расшифровке ПЭТ-КТ головного мозга с метионином, ПЭТ-КТ всего тела с глюкозой, и других видов ПЭТ. Достаточно отправить им снимки через систему Национальной телерадиологической сети, и получить в течение суток подробное и квалифицированное заключение. Пересмотр результатов ПЭТ осуществляется под руководством З. Л. Бродской — корифея отечественной радиологии, многолетнего соратника знаменитой Н. П. Бехтеревой.
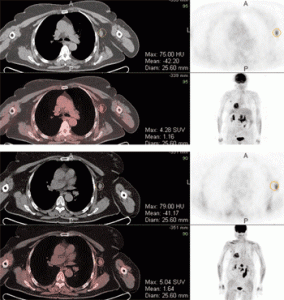
ПЭТ-КТ при раке молочной железы. Тщательный анализ характеристик накопления РФП (SUV) в подмышечных лимфатических узлах помогают различить метастазы и доброкачественное увеличение узлов.
Читать подробнее о Втором мнении
Читать подробнее о телемедицине

Кандидат медицинских наук, член Европейского общества радиологов
- Case report
- Open Access
- Published: 05 March 2020
BMC Medical Imaging
volume 20, Article number: 26 (2020)
Cite this article
-
4941 Accesses
-
2 Citations
-
1 Altmetric
-
Metrics details
Abstract
Background
The F-18 fluorodeoxyglucose positron emission/computed tomography (FDG PET/CT) has become an established diagnostic imaging for malignancy. However, there are other diseases that can also be identified with FDG, some of them are infections such as tuberculosis.
Case presentation
In this case report, two patients showed multiple hypermetabolic tuberculosis lesions on FDG PET/CT, with one of the patients having history of malignancy. The objective of the present case report is to emphasize the need to use other differential diagnosis techniques for tuberculosis especially in tuberculosis-endemic countries when interpreting FDG PET/CT.
Conclusion
By analyzing diagnostic imaging alone, there is a high chance of misinterpreting asymptomatic tuberculosis patient as having malignancy. Therefore, there is need for correlation with clinical data as well as other imaging modalities and PET/CT with more specific tracer in order to differentiate malignancy from benign disease such as tuberculosis.
Peer Review reports
Background
The bacteria responsible for tuberculosis is Mycobacterium tuberculosis, which is a serious contagious pathogen in many countries. Based on the data released by the World Health Organization in 2009, one-third of the world’s population, almost 2 billion people, are infected with M. tuberculosis [1, 2].
Tuberculosis is a major health problem in most developing countries including Indonesia. The incidence rate of tuberculosis in Indonesia was 391 per 100,000 population in 2015 and was marked as the ninth most common country with Tuberculosis [3].
M. Tuberculosis usually affects the lung but to some extent may also involve other susceptible extra-pulmonary organs. Also, there is a challenge with the identifying the infection at the extra-pulmonary site as it is often difficult to obtain specimen for definitive diagnosis of tuberculosis [4, 5].
FDG PET/CT is a diagnostic imaging procedure which provides a unique information of cellular glucose metabolism. By using the anomalous hallmark of cancer cell in reprogramming glucose metabolism and upregulating glucose transporter, the uptake of FDG is markedly increased in cancer cells [6]. However, there are some limitations with respect to the specificity of FDG PET/CT in that it sometimes gives false negative or positive results. The false positive findings are majorly associated with high FDG uptake in infectious or inflammatory tissue [7]. Granulocytes and mononuclear cells use glucose as an energy source during their metabolic burst [8], consequently, high FDG uptake could be seen in tuberculosis. Two cases of malignancy-like lesions in tuberculosis patients were reported which resulted in false positive findings with FDG PET/CT (Table 1).
Full size table
Case presentation
The FDG PET/CT images were acquired on a PET/CT scanner (Gemini, Phillips Healthcare, USA). All patients were subjected to fasting for over 6 h with blood sugar level below 150 mg/dL before the intravenous injection of FDG with a dose of 0.10 mCi/kgBW. The images were then acquired between 45 to 90 min after the injection. The acquisition was carried out from head to feet with arms above the head position using 700-mm field of view (FOV) and slice thickness of 10 mm. Also, three-dimensional data acquisition was performed for 3 min per bed position, followed by image reconstruction with the 3D-ordered-subsets expectation maximization method. Segmented attenuation was corrected by X-ray CT (140 kV, 120–240 mAs) to produce 128 × 128 matrix image. CT images were reconstructed using a conventional filtered back projection method.
Case 1
A 47-year old male with nasopharyngeal cancer for 2 years complained of a stuffed nose and hearing derivation in the right ear for about 2 weeks before being subjected to FDG PET/CT. He had no history of exposure to tuberculosis patient, weight loss, cough, low-grade fever, decreased appetite, or night sweat.
The results from laboratory tests showed normal blood count and serum carcinoma embryonic antigen (CEA) level. Contrast enhanced head and neck CT scan showed no sign of relapse in the nasopharyngeal wall with multiple metastases neck lymphadenopathies.
However, FDG PET/CT showed high FDG uptake by these multiple neck lymphadenopathies and the right nasopharyngeal wall (Fig. 1). The highest SUVmax of multiple neck lymphadenopathies was 11.05 that located in the right jugular superior, meanwhile SUVmax of the right nasopharyngeal wall was 4.51. Mild FDG-avid ground glass opacities with thick cavitation and calcification were also found at the apex of the left lung. Based on these FDG PET/CT findings, the biopsy was performed in the right nasopharyngeal that positive for tuberculous infection.
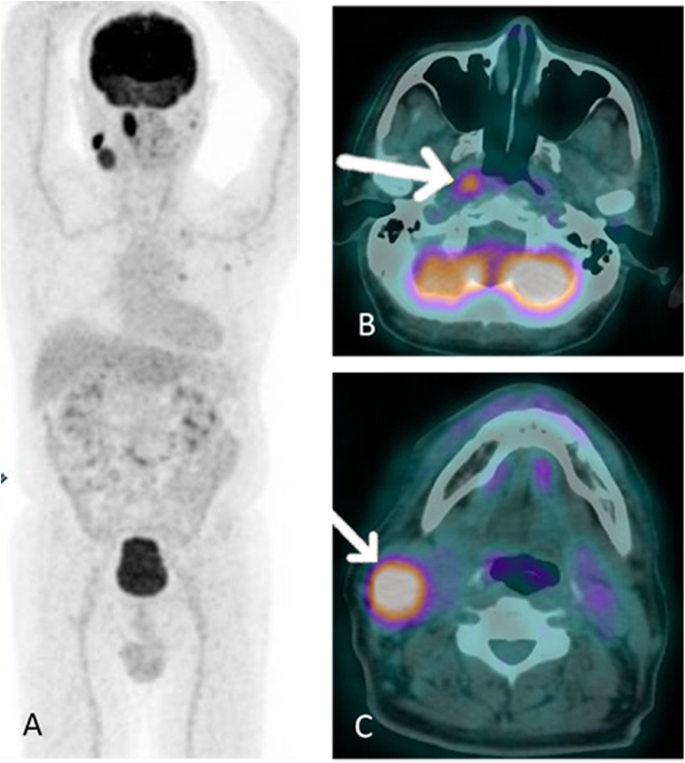
FDG PET/CT of patient number 1. Hypermetabolic lesions in several parts of head and neck. a MIP. b hypermetabolic lesion at right nasopharyngeal wall. c hypermetabolic enlarge lymph node at neck region
Full size image
Case 2
A 58-year old female presented with occasional dizziness for almost 4 months. She had history of smoking but none for tuberculosis exposure.
The CT scan on the brain showed multiple metastatic nodules (Fig. 2b). Also, the FDG PET/CT showed high FDG uptake at the left superior bronchial wall (Fig. 2c) and mild FDG uptake of bronchial thickening at posterior region of the left superior lung lobe. There were also multiple high FDG uptakes at the neck, mediastinal, abdominal, and pelvic lymphadenopathies with the highest SUVmax was 4.05 that located at left hilar. High FDG uptake of lytic lesion at fourth lumbar and right parieto-occipital nodule were also seen. All these findings were interpreted as metastatic lung cancer to the lymph nodes, brain, and bone. Based on these FDG PET/CT findings, the biopsy was performed at the left hilar lymph node and positive for tuberculous infection.
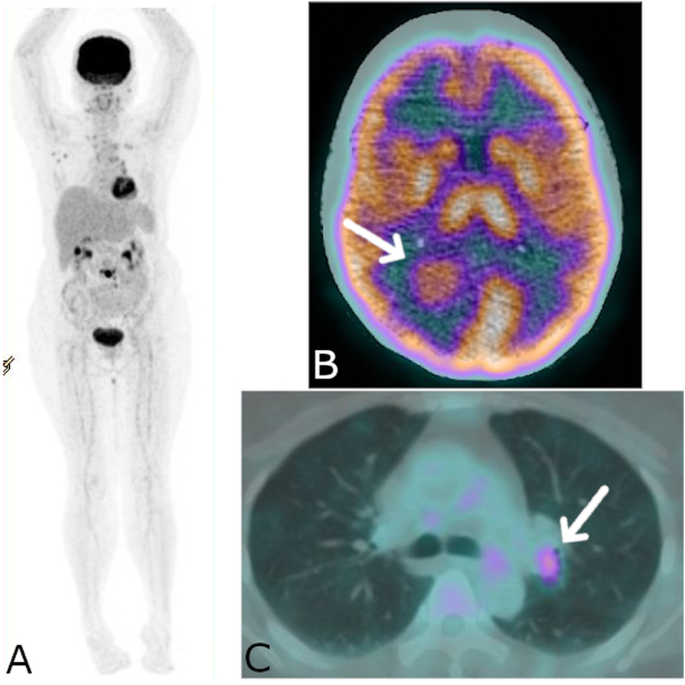
FDG PET/CT of patient number 2. a MIP showed multiple hypermetabolic lesions. b hypermetabolic nodule at brain highly suspicious for metastasis. c hypermetabolic lesion at left hilar region
Full size image
All patients underwent lymph nodes biopsy and were reported as tuberculosis infections. Consequently, anti-tuberculosis drugs such as rifampicin, pyrazinamide, isoniazid, and streptomycin were administered according to the histopathology results. Also, all the patients underwent contrast enhanced CT scan three to 5 months after the initial anti-tuberculosis treatment for response evaluation. All cases showed good response to the treatment and were all considered as complete remission.
Discussion and conclusion
There were two reported cases of malignancy-like lesions in tuberculosis patients that resulted in false positive findings with FDG PET/CT. All the lesions showed high FDG malignant-like lesions uptake and the FDG PET/CT findings misinterpreted as malignancy. However, tuberculosis was confirmed as final diagnosis by the histopathology studies.
In all these cases, the initial CT scan did not show typical characteristics finding for extrapulmonary tuberculosis, however, the FDG PET/CT showed high FDG lesions uptake which is generally viewed as malignant lesions. The extrapulmonary tuberculosis commonly develop from the pulmonary tuberculosis which subsequently spread outside the lungs through the lymphatic system. However, there are conditions whereby extrapulmonary tuberculosis develops without any evidence of pulmonary lesions [9, 10]. These two cases were found with mild FDG uptake of pulmonary lesions without any typical radiological findings for tuberculosis.
The case number one showed marked hypermetabolic lesion at right nasopharyngeal wall, suggesting nasopharyngeal cancer recurrence. This case was misinterpreted as malignancy because of the patients’ history, lesions sites, and atypical pulmonary radiologic finding lesions for tuberculosis. However, subject in case number two had no history of malignancy but showed typical metastatic distribution with hypermetabolic lesion at bronchial wall which is a suspicious sign for malignancy.
According to WHO criteria for classification, extrapulmonary tuberculosis is defined as an infection caused by M. Tuberculosis which affects tissues and organs outside the pulmonary parenchyma. The incidence rate of extrapulmonary tuberculosis is between 20 and 25% of all tuberculosis cases [11]. One of the most common extrapulmonary tuberculosis form is lymphadenopathy tuberculosis that counts for 30–40% of all extrapulmonary tuberculosis. The most common predilection site for lymphadenopathy tuberculosis is neck region (63–77%), however, it can also be found in other regions [12]. Fever and other typical systemic symptoms may not always present until the late stage of extrapulmonary tuberculosis [13].
The PET/CT study using F-18 FDG as a glucose analogue is a rapidly producing functional imaging modality which has been very beneficial in the detection of primary, recurrent, and metastatic tumour, planning, and therapy monitoring. The growth of cancer cell is an energy-related process which is supported by increased glucose metabolism. It is widely known that glucose transporter (GLUT) proteins, a membrane protein, are responsible for the transport of glucose across cellular membranes. Consequently, cancer cells have higher rates of GLUT expressions compared to normal cells. Together with this mechanism, some types of tumour is also associated with a higher rate of phosphorylation, lower rate of dephosphorylation of intracellular phosphorylated glucose, and higher activity of hexokinase.
These characteristics of cancer cell make the FDG accumulation much higher than normal cell. FDG PET/CT is known as superior but less specific for diagnostic imaging in malignancy. Through glucose transporters that are overexpressed both in cancer and inflammatory cells hence result in FDG accumulation, is not only visible in cancer cells but also in inflammatory cells such as activated macrophages, lymphocytes, and neutrophils at the site of inflammation or infection [14].
There is a similarity between the FDG uptake mechanism of both cancer and inflammatory cells. Both cells need high glucose consumption to fulfill the high energy demands. Glucose enter the cells through energy-dependent transporters. There are seven types of glucose transporter, known as GLUT-1 to GLUT-7 [11]. It was discovered in a study that a relative higher FDG uptake was observed in some of the inflammatory lesions, in which the expression level of GLUT-3 was much higher compared to GLUT-1. Also, Fu et all found that mRNA analysis in inflammatory cells showed GLUT-1 expression increased to 3.5 times, whereas GLUT-3 increased to 6 times, following the activation of inflammatory factors [9, 12]. The expressions of GLUT-1 and GLUT-3 in the inflammatory lesions are related to the type, quantity, and degree of activation of the inflammatory cells. Another study reported the important roles played by cytokines and growth factors in promoting the affinity of glucose transporter. Therefore, FDG uptake mechanism in inflammatory cells is almost similar compared to tumour setting though different situations [9].
Many studies have been conducted in attempting to differentiate between malignancy and inflammation in FDG PET study, including variation of protocols, characteristic, and parameter. Traditionally, a threshold for single time point using SUV max has been proposed to differentiate the two processes, however this method was proven not effective with false positive rate above 60%. Other widely accepted method is using dual-time imaging, based on varying levels of glucose-6-phosphatase activity among different tumour cell types, inflammatory and normal cells. However, this method is not dependable for several reasons including histologic type of tumours, the combination or the coexisting of chronic and acute inflammation, necrosis, hypoxia, and degree of angiogenesis. Most recent proposed method is using influx rate constant (Ki). It is reported in lung inflammatory lesions that this parameter is closely related to neutrophil activation. However, it is not applicable in daily practice and therefore requires further study in various type of tumours.
Familiarity with oncologic pattern and correlation with other modalities such as tumour marker and anatomical imaging are important in FDG PET/CT interpretation to produce more accurate assessment in clinical setting. Also, it is important to understand the pitfall of tumour markers and other clinical assessments commonly used in diagnosing malignancy. Several studies showed CEA level which might also increase in inflammatory process in the lung [15, 16]. New specific radiopharmaceutical for tuberculosis, such as Tc-99 m-ethambutol might also be helpful in these setting [17, 18].
Conclusively, two cases of malignancy-like lesions in tuberculosis patients were reported but resulted in false positive findings in FDG PET/CT. By analyzing only diagnostic imaging, asymptomatic tuberculosis patient can be easily misinterpreted as having malignancy. There is need for correlation with clinical data, as well as other imaging modalities and PET/CT with more specific tracer, in order to be able to differentiate malignancy from benign disease such as tuberculosis.
Availability of data and materials
The datasets generated and/or analysed during the current study are de-identified and not publicly available considering the fact that not all the patients consented to it for publication but are available from the corresponding author on reasonable request.
Abbreviations
- CEA:
-
Carcinoma Embryonic Antigen
- CT:
-
Computed tomography
- FDG:
-
18F-fluorodeoxyglucose
- GLUT:
-
Glucose transporter
- PET:
-
Positron emission tomography
References
-
Polley P, Dunn R. Noncontiguous spinal tuberculosis: incidence and management. Eur Spine J. 2009;18(8):1096–101..
Article
Google Scholar
-
Khue PM, Truffot-Pernot C, Texier-Maugein J, Jarlier V, Robert J. A 10-year prospective surveillance of mycobacterium tuberculosis drug resistance in France 1995–2004. Eur Respir J. 2007;30(5):937–44.
Article
CASGoogle Scholar
-
Who report 2009. Global Tuberculosis control: epidemiología, strategy, financing. Geneva: World Health; 2009.
Google Scholar
-
Kanga I, Taylor JA, Jacobs C, Outerbridge G. Tuberculosis of the neuromusculoskeletal system: a review of two cases presenting as chiropractic patients. J Can Chiropr Assoc. 2015;59(1):13.
PubMed
PubMed CentralGoogle Scholar
-
Lee JY. Diagnosis and treatment of extra pulmonary tuberculosis. Tuberc Respir Dis. 2015;78:47–55.
Article
Google Scholar
-
Fletcher JW, Djulbegovic B, Soares HP, Siegel BA, Lowe VJ, Lyman GH, Coleman RE, Wahl R, Paschold JC, Avril N, Einhorn LH, Suh WW, Samson D, Delbeke D, Gorman M, Shields AF. Recommendation on the use of 18F-FDG PET in oncology. J Nucl Med. 2008;49:480–508.
Article
Google Scholar
-
Bakheet SM, Powe J, Kandil A, Ezzat A, Rostom A, Amartey J. F-18 FDG uptake in breast infection and inflammation. Clin Nucl Med. 2000;25:100–3.
Article
CASGoogle Scholar
-
Weisdorf DJ, Craddock PR, Jacob HS. Glycogenolysis versus glucose transport in human granulocytes: differential activation in phagocytosis and chemotaxis. Blood. 1982;60:888–93.
Article
CASGoogle Scholar
-
Fisher D, Elwood K. Nonrespiratory tuberculosis. In: Canadian thoracic society, Canadian Lung Association, and the Public Health Agency of Canada, editor. Canadian tuberculosis standards. 7th ed. Ottawa: Canadian Thoracic Society; 2013.
Google Scholar
-
Zuang H, Pourdehnad M, Lambright ES, Yamamoto AJ, Lanuti M, Li P, Mozley PD, Rossman MD, Albelda SM, Alavi A. Dual time point 18F-FDG PET imaging for differentiating malignant from inflammatory process. J Nucl Med. 2001;42:1412–7.
Google Scholar
-
Metser U, Even-Sapir E. Increased 18 F-fluorodeoxyglucose uptake in benign, nonphysiologic lesions found on whole-body positron emission tomography/computed tomography (PET/CT): accumulated data from four years of experience with PET/CT. In: Seminars in nuclear medicine. Philadelphia: Elsevier; 2007. p. 206–22.
Google Scholar
-
Wang ZG, Yu MM, Han Y, Wu FY, Yang GJ, Li DC, Liu SM. Correlation of Glut-2 and Glut-3 expression with F-18 FDG uptake in pulmonary inflammatory lesion. Medicine. 2016;95:48.
Google Scholar
-
Hammoudeh M, Khanjar I. Skeletal tuberculosis mimicking seronegative spondyloarthropathy. Rheumatol Int. 2004;24(1):50–2.
Article
Google Scholar
-
Kim IJ, Lee JS, Kim SJ, Kim YK, Jeong YJ, Jun S, Nam HY, Kim JS. Double-phase 18F-FDG PET-CT for determina- tion of pulmonary tuberculoma activity. Eur J Nucl Med Mol Imaging. 2008;35:808–14.
Article
Google Scholar
-
Quist J, Hill AR. Serum lactate dehydrogenase (LDH) in Pneumocystis carinii pneumonia, tuberculosis and bacterial pneumonia. Chest. 1995;108(2):415–8.
Article
CASGoogle Scholar
-
No JI, Yang JY, Hyun HJ, Yeon CS, Choi HJ. Factors associated with serum levels of carcinoembryonic antigen in healthy non-smokers. Korean J Fam Med. 2013;34(6):413–9. https://doi.org/10.4082/kjfm.2013.34.6.413.
Article
PubMed
PubMed CentralGoogle Scholar
-
Houshmand S, Salavati A, Basu S, et al. The role of dual and multiple time point imaging of FDG uptake in both normal and disease states. Clin Transl Imaging. 2014;2:281. https://doi.org/10.1007/s40336-014-0075-x.
Article
Google Scholar
-
Kartamihardja AHS, Kurniawati Y, Gunawan R. Diagnostic value of 99mTc-ethambutol scintigraphy in tuberculosis: compared to microbiological and histopathological tests. Ann Nucl Med. 2018;32(1):60–8.
Article
CASGoogle Scholar
Download references
Acknowledgements
Not Applicable.
Funding
There was no funding received for this study.
Author information
Authors and Affiliations
-
Department of Nuclear Medicine, Mochtar Riady Comprehensive Cancer Centre Siloam Hospital, Jakarta, Indonesia
Febby Hutomo, Ryan Yudistiro, Ivana Dewi Mulyanto & Hendra Budiawan
-
Department of Nuclear Medicine, School of Medicine of Pelita Harapan University, Tangerang, Indonesia
Ryan Yudistiro & Ivana Dewi Mulyanto
-
Department of Nuclear Medicine and Molecular Imaging, School of Medicine of Padjadjaran University, Dr Hasan Sadikin Hospital, Bandung, Indonesia
Hendra Budiawan
Authors
- Febby Hutomo
You can also search for this author in
PubMed Google Scholar - Ryan Yudistiro
You can also search for this author in
PubMed Google Scholar - Ivana Dewi Mulyanto
You can also search for this author in
PubMed Google Scholar - Hendra Budiawan
You can also search for this author in
PubMed Google Scholar
Contributions
FH collected patient data and drafted the manuscript. FH, RY, and IDM designed and organized this report and participated in writing the manuscript. HB reviewed and approved the final manuscript. All authors read and approved the final manuscript.
Corresponding author
Correspondence to
Ryan Yudistiro.
Ethics declarations
Ethics approval and consent to participate
Not Applicable.
Consent for publication
Not Applıcable.
Competing interests
The authors declare that they have no competing interests.
Additional information
Publisher’s Note
Springer Nature remains neutral with regard to jurisdictional claims in published maps and institutional affiliations.
Rights and permissions
Open Access This article is licensed under a Creative Commons Attribution 4.0 International License, which permits use, sharing, adaptation, distribution and reproduction in any medium or format, as long as you give appropriate credit to the original author(s) and the source, provide a link to the Creative Commons licence, and indicate if changes were made. The images or other third party material in this article are included in the article’s Creative Commons licence, unless indicated otherwise in a credit line to the material. If material is not included in the article’s Creative Commons licence and your intended use is not permitted by statutory regulation or exceeds the permitted use, you will need to obtain permission directly from the copyright holder. To view a copy of this licence, visit http://creativecommons.org/licenses/by/4.0/. The Creative Commons Public Domain Dedication waiver (http://creativecommons.org/publicdomain/zero/1.0/) applies to the data made available in this article, unless otherwise stated in a credit line to the data.
Reprints and Permissions
About this article
Cite this article
Hutomo, F., Yudistiro, R., Mulyanto, I.D. et al. False positive finding from malignancy-like lesions on FDG PET/CT: case report of tuberculosis patients.
BMC Med Imaging 20, 26 (2020). https://doi.org/10.1186/s12880-020-00427-w
Download citation
-
Received: 04 June 2019
-
Accepted: 21 February 2020
-
Published: 05 March 2020
-
DOI: https://doi.org/10.1186/s12880-020-00427-w
Keywords
- Tuberculosis
- Malignancy
- FDG
- PET/CT
- Case report
- Open Access
- Published: 05 March 2020
BMC Medical Imaging
volume 20, Article number: 26 (2020)
Cite this article
-
4941 Accesses
-
2 Citations
-
1 Altmetric
-
Metrics details
Abstract
Background
The F-18 fluorodeoxyglucose positron emission/computed tomography (FDG PET/CT) has become an established diagnostic imaging for malignancy. However, there are other diseases that can also be identified with FDG, some of them are infections such as tuberculosis.
Case presentation
In this case report, two patients showed multiple hypermetabolic tuberculosis lesions on FDG PET/CT, with one of the patients having history of malignancy. The objective of the present case report is to emphasize the need to use other differential diagnosis techniques for tuberculosis especially in tuberculosis-endemic countries when interpreting FDG PET/CT.
Conclusion
By analyzing diagnostic imaging alone, there is a high chance of misinterpreting asymptomatic tuberculosis patient as having malignancy. Therefore, there is need for correlation with clinical data as well as other imaging modalities and PET/CT with more specific tracer in order to differentiate malignancy from benign disease such as tuberculosis.
Peer Review reports
Background
The bacteria responsible for tuberculosis is Mycobacterium tuberculosis, which is a serious contagious pathogen in many countries. Based on the data released by the World Health Organization in 2009, one-third of the world’s population, almost 2 billion people, are infected with M. tuberculosis [1, 2].
Tuberculosis is a major health problem in most developing countries including Indonesia. The incidence rate of tuberculosis in Indonesia was 391 per 100,000 population in 2015 and was marked as the ninth most common country with Tuberculosis [3].
M. Tuberculosis usually affects the lung but to some extent may also involve other susceptible extra-pulmonary organs. Also, there is a challenge with the identifying the infection at the extra-pulmonary site as it is often difficult to obtain specimen for definitive diagnosis of tuberculosis [4, 5].
FDG PET/CT is a diagnostic imaging procedure which provides a unique information of cellular glucose metabolism. By using the anomalous hallmark of cancer cell in reprogramming glucose metabolism and upregulating glucose transporter, the uptake of FDG is markedly increased in cancer cells [6]. However, there are some limitations with respect to the specificity of FDG PET/CT in that it sometimes gives false negative or positive results. The false positive findings are majorly associated with high FDG uptake in infectious or inflammatory tissue [7]. Granulocytes and mononuclear cells use glucose as an energy source during their metabolic burst [8], consequently, high FDG uptake could be seen in tuberculosis. Two cases of malignancy-like lesions in tuberculosis patients were reported which resulted in false positive findings with FDG PET/CT (Table 1).
Full size table
Case presentation
The FDG PET/CT images were acquired on a PET/CT scanner (Gemini, Phillips Healthcare, USA). All patients were subjected to fasting for over 6 h with blood sugar level below 150 mg/dL before the intravenous injection of FDG with a dose of 0.10 mCi/kgBW. The images were then acquired between 45 to 90 min after the injection. The acquisition was carried out from head to feet with arms above the head position using 700-mm field of view (FOV) and slice thickness of 10 mm. Also, three-dimensional data acquisition was performed for 3 min per bed position, followed by image reconstruction with the 3D-ordered-subsets expectation maximization method. Segmented attenuation was corrected by X-ray CT (140 kV, 120–240 mAs) to produce 128 × 128 matrix image. CT images were reconstructed using a conventional filtered back projection method.
Case 1
A 47-year old male with nasopharyngeal cancer for 2 years complained of a stuffed nose and hearing derivation in the right ear for about 2 weeks before being subjected to FDG PET/CT. He had no history of exposure to tuberculosis patient, weight loss, cough, low-grade fever, decreased appetite, or night sweat.
The results from laboratory tests showed normal blood count and serum carcinoma embryonic antigen (CEA) level. Contrast enhanced head and neck CT scan showed no sign of relapse in the nasopharyngeal wall with multiple metastases neck lymphadenopathies.
However, FDG PET/CT showed high FDG uptake by these multiple neck lymphadenopathies and the right nasopharyngeal wall (Fig. 1). The highest SUVmax of multiple neck lymphadenopathies was 11.05 that located in the right jugular superior, meanwhile SUVmax of the right nasopharyngeal wall was 4.51. Mild FDG-avid ground glass opacities with thick cavitation and calcification were also found at the apex of the left lung. Based on these FDG PET/CT findings, the biopsy was performed in the right nasopharyngeal that positive for tuberculous infection.

FDG PET/CT of patient number 1. Hypermetabolic lesions in several parts of head and neck. a MIP. b hypermetabolic lesion at right nasopharyngeal wall. c hypermetabolic enlarge lymph node at neck region
Full size image
Case 2
A 58-year old female presented with occasional dizziness for almost 4 months. She had history of smoking but none for tuberculosis exposure.
The CT scan on the brain showed multiple metastatic nodules (Fig. 2b). Also, the FDG PET/CT showed high FDG uptake at the left superior bronchial wall (Fig. 2c) and mild FDG uptake of bronchial thickening at posterior region of the left superior lung lobe. There were also multiple high FDG uptakes at the neck, mediastinal, abdominal, and pelvic lymphadenopathies with the highest SUVmax was 4.05 that located at left hilar. High FDG uptake of lytic lesion at fourth lumbar and right parieto-occipital nodule were also seen. All these findings were interpreted as metastatic lung cancer to the lymph nodes, brain, and bone. Based on these FDG PET/CT findings, the biopsy was performed at the left hilar lymph node and positive for tuberculous infection.

FDG PET/CT of patient number 2. a MIP showed multiple hypermetabolic lesions. b hypermetabolic nodule at brain highly suspicious for metastasis. c hypermetabolic lesion at left hilar region
Full size image
All patients underwent lymph nodes biopsy and were reported as tuberculosis infections. Consequently, anti-tuberculosis drugs such as rifampicin, pyrazinamide, isoniazid, and streptomycin were administered according to the histopathology results. Also, all the patients underwent contrast enhanced CT scan three to 5 months after the initial anti-tuberculosis treatment for response evaluation. All cases showed good response to the treatment and were all considered as complete remission.
Discussion and conclusion
There were two reported cases of malignancy-like lesions in tuberculosis patients that resulted in false positive findings with FDG PET/CT. All the lesions showed high FDG malignant-like lesions uptake and the FDG PET/CT findings misinterpreted as malignancy. However, tuberculosis was confirmed as final diagnosis by the histopathology studies.
In all these cases, the initial CT scan did not show typical characteristics finding for extrapulmonary tuberculosis, however, the FDG PET/CT showed high FDG lesions uptake which is generally viewed as malignant lesions. The extrapulmonary tuberculosis commonly develop from the pulmonary tuberculosis which subsequently spread outside the lungs through the lymphatic system. However, there are conditions whereby extrapulmonary tuberculosis develops without any evidence of pulmonary lesions [9, 10]. These two cases were found with mild FDG uptake of pulmonary lesions without any typical radiological findings for tuberculosis.
The case number one showed marked hypermetabolic lesion at right nasopharyngeal wall, suggesting nasopharyngeal cancer recurrence. This case was misinterpreted as malignancy because of the patients’ history, lesions sites, and atypical pulmonary radiologic finding lesions for tuberculosis. However, subject in case number two had no history of malignancy but showed typical metastatic distribution with hypermetabolic lesion at bronchial wall which is a suspicious sign for malignancy.
According to WHO criteria for classification, extrapulmonary tuberculosis is defined as an infection caused by M. Tuberculosis which affects tissues and organs outside the pulmonary parenchyma. The incidence rate of extrapulmonary tuberculosis is between 20 and 25% of all tuberculosis cases [11]. One of the most common extrapulmonary tuberculosis form is lymphadenopathy tuberculosis that counts for 30–40% of all extrapulmonary tuberculosis. The most common predilection site for lymphadenopathy tuberculosis is neck region (63–77%), however, it can also be found in other regions [12]. Fever and other typical systemic symptoms may not always present until the late stage of extrapulmonary tuberculosis [13].
The PET/CT study using F-18 FDG as a glucose analogue is a rapidly producing functional imaging modality which has been very beneficial in the detection of primary, recurrent, and metastatic tumour, planning, and therapy monitoring. The growth of cancer cell is an energy-related process which is supported by increased glucose metabolism. It is widely known that glucose transporter (GLUT) proteins, a membrane protein, are responsible for the transport of glucose across cellular membranes. Consequently, cancer cells have higher rates of GLUT expressions compared to normal cells. Together with this mechanism, some types of tumour is also associated with a higher rate of phosphorylation, lower rate of dephosphorylation of intracellular phosphorylated glucose, and higher activity of hexokinase.
These characteristics of cancer cell make the FDG accumulation much higher than normal cell. FDG PET/CT is known as superior but less specific for diagnostic imaging in malignancy. Through glucose transporters that are overexpressed both in cancer and inflammatory cells hence result in FDG accumulation, is not only visible in cancer cells but also in inflammatory cells such as activated macrophages, lymphocytes, and neutrophils at the site of inflammation or infection [14].
There is a similarity between the FDG uptake mechanism of both cancer and inflammatory cells. Both cells need high glucose consumption to fulfill the high energy demands. Glucose enter the cells through energy-dependent transporters. There are seven types of glucose transporter, known as GLUT-1 to GLUT-7 [11]. It was discovered in a study that a relative higher FDG uptake was observed in some of the inflammatory lesions, in which the expression level of GLUT-3 was much higher compared to GLUT-1. Also, Fu et all found that mRNA analysis in inflammatory cells showed GLUT-1 expression increased to 3.5 times, whereas GLUT-3 increased to 6 times, following the activation of inflammatory factors [9, 12]. The expressions of GLUT-1 and GLUT-3 in the inflammatory lesions are related to the type, quantity, and degree of activation of the inflammatory cells. Another study reported the important roles played by cytokines and growth factors in promoting the affinity of glucose transporter. Therefore, FDG uptake mechanism in inflammatory cells is almost similar compared to tumour setting though different situations [9].
Many studies have been conducted in attempting to differentiate between malignancy and inflammation in FDG PET study, including variation of protocols, characteristic, and parameter. Traditionally, a threshold for single time point using SUV max has been proposed to differentiate the two processes, however this method was proven not effective with false positive rate above 60%. Other widely accepted method is using dual-time imaging, based on varying levels of glucose-6-phosphatase activity among different tumour cell types, inflammatory and normal cells. However, this method is not dependable for several reasons including histologic type of tumours, the combination or the coexisting of chronic and acute inflammation, necrosis, hypoxia, and degree of angiogenesis. Most recent proposed method is using influx rate constant (Ki). It is reported in lung inflammatory lesions that this parameter is closely related to neutrophil activation. However, it is not applicable in daily practice and therefore requires further study in various type of tumours.
Familiarity with oncologic pattern and correlation with other modalities such as tumour marker and anatomical imaging are important in FDG PET/CT interpretation to produce more accurate assessment in clinical setting. Also, it is important to understand the pitfall of tumour markers and other clinical assessments commonly used in diagnosing malignancy. Several studies showed CEA level which might also increase in inflammatory process in the lung [15, 16]. New specific radiopharmaceutical for tuberculosis, such as Tc-99 m-ethambutol might also be helpful in these setting [17, 18].
Conclusively, two cases of malignancy-like lesions in tuberculosis patients were reported but resulted in false positive findings in FDG PET/CT. By analyzing only diagnostic imaging, asymptomatic tuberculosis patient can be easily misinterpreted as having malignancy. There is need for correlation with clinical data, as well as other imaging modalities and PET/CT with more specific tracer, in order to be able to differentiate malignancy from benign disease such as tuberculosis.
Availability of data and materials
The datasets generated and/or analysed during the current study are de-identified and not publicly available considering the fact that not all the patients consented to it for publication but are available from the corresponding author on reasonable request.
Abbreviations
- CEA:
-
Carcinoma Embryonic Antigen
- CT:
-
Computed tomography
- FDG:
-
18F-fluorodeoxyglucose
- GLUT:
-
Glucose transporter
- PET:
-
Positron emission tomography
References
-
Polley P, Dunn R. Noncontiguous spinal tuberculosis: incidence and management. Eur Spine J. 2009;18(8):1096–101..
Article
Google Scholar
-
Khue PM, Truffot-Pernot C, Texier-Maugein J, Jarlier V, Robert J. A 10-year prospective surveillance of mycobacterium tuberculosis drug resistance in France 1995–2004. Eur Respir J. 2007;30(5):937–44.
Article
CASGoogle Scholar
-
Who report 2009. Global Tuberculosis control: epidemiología, strategy, financing. Geneva: World Health; 2009.
Google Scholar
-
Kanga I, Taylor JA, Jacobs C, Outerbridge G. Tuberculosis of the neuromusculoskeletal system: a review of two cases presenting as chiropractic patients. J Can Chiropr Assoc. 2015;59(1):13.
PubMed
PubMed CentralGoogle Scholar
-
Lee JY. Diagnosis and treatment of extra pulmonary tuberculosis. Tuberc Respir Dis. 2015;78:47–55.
Article
Google Scholar
-
Fletcher JW, Djulbegovic B, Soares HP, Siegel BA, Lowe VJ, Lyman GH, Coleman RE, Wahl R, Paschold JC, Avril N, Einhorn LH, Suh WW, Samson D, Delbeke D, Gorman M, Shields AF. Recommendation on the use of 18F-FDG PET in oncology. J Nucl Med. 2008;49:480–508.
Article
Google Scholar
-
Bakheet SM, Powe J, Kandil A, Ezzat A, Rostom A, Amartey J. F-18 FDG uptake in breast infection and inflammation. Clin Nucl Med. 2000;25:100–3.
Article
CASGoogle Scholar
-
Weisdorf DJ, Craddock PR, Jacob HS. Glycogenolysis versus glucose transport in human granulocytes: differential activation in phagocytosis and chemotaxis. Blood. 1982;60:888–93.
Article
CASGoogle Scholar
-
Fisher D, Elwood K. Nonrespiratory tuberculosis. In: Canadian thoracic society, Canadian Lung Association, and the Public Health Agency of Canada, editor. Canadian tuberculosis standards. 7th ed. Ottawa: Canadian Thoracic Society; 2013.
Google Scholar
-
Zuang H, Pourdehnad M, Lambright ES, Yamamoto AJ, Lanuti M, Li P, Mozley PD, Rossman MD, Albelda SM, Alavi A. Dual time point 18F-FDG PET imaging for differentiating malignant from inflammatory process. J Nucl Med. 2001;42:1412–7.
Google Scholar
-
Metser U, Even-Sapir E. Increased 18 F-fluorodeoxyglucose uptake in benign, nonphysiologic lesions found on whole-body positron emission tomography/computed tomography (PET/CT): accumulated data from four years of experience with PET/CT. In: Seminars in nuclear medicine. Philadelphia: Elsevier; 2007. p. 206–22.
Google Scholar
-
Wang ZG, Yu MM, Han Y, Wu FY, Yang GJ, Li DC, Liu SM. Correlation of Glut-2 and Glut-3 expression with F-18 FDG uptake in pulmonary inflammatory lesion. Medicine. 2016;95:48.
Google Scholar
-
Hammoudeh M, Khanjar I. Skeletal tuberculosis mimicking seronegative spondyloarthropathy. Rheumatol Int. 2004;24(1):50–2.
Article
Google Scholar
-
Kim IJ, Lee JS, Kim SJ, Kim YK, Jeong YJ, Jun S, Nam HY, Kim JS. Double-phase 18F-FDG PET-CT for determina- tion of pulmonary tuberculoma activity. Eur J Nucl Med Mol Imaging. 2008;35:808–14.
Article
Google Scholar
-
Quist J, Hill AR. Serum lactate dehydrogenase (LDH) in Pneumocystis carinii pneumonia, tuberculosis and bacterial pneumonia. Chest. 1995;108(2):415–8.
Article
CASGoogle Scholar
-
No JI, Yang JY, Hyun HJ, Yeon CS, Choi HJ. Factors associated with serum levels of carcinoembryonic antigen in healthy non-smokers. Korean J Fam Med. 2013;34(6):413–9. https://doi.org/10.4082/kjfm.2013.34.6.413.
Article
PubMed
PubMed CentralGoogle Scholar
-
Houshmand S, Salavati A, Basu S, et al. The role of dual and multiple time point imaging of FDG uptake in both normal and disease states. Clin Transl Imaging. 2014;2:281. https://doi.org/10.1007/s40336-014-0075-x.
Article
Google Scholar
-
Kartamihardja AHS, Kurniawati Y, Gunawan R. Diagnostic value of 99mTc-ethambutol scintigraphy in tuberculosis: compared to microbiological and histopathological tests. Ann Nucl Med. 2018;32(1):60–8.
Article
CASGoogle Scholar
Download references
Acknowledgements
Not Applicable.
Funding
There was no funding received for this study.
Author information
Authors and Affiliations
-
Department of Nuclear Medicine, Mochtar Riady Comprehensive Cancer Centre Siloam Hospital, Jakarta, Indonesia
Febby Hutomo, Ryan Yudistiro, Ivana Dewi Mulyanto & Hendra Budiawan
-
Department of Nuclear Medicine, School of Medicine of Pelita Harapan University, Tangerang, Indonesia
Ryan Yudistiro & Ivana Dewi Mulyanto
-
Department of Nuclear Medicine and Molecular Imaging, School of Medicine of Padjadjaran University, Dr Hasan Sadikin Hospital, Bandung, Indonesia
Hendra Budiawan
Authors
- Febby Hutomo
You can also search for this author in
PubMed Google Scholar - Ryan Yudistiro
You can also search for this author in
PubMed Google Scholar - Ivana Dewi Mulyanto
You can also search for this author in
PubMed Google Scholar - Hendra Budiawan
You can also search for this author in
PubMed Google Scholar
Contributions
FH collected patient data and drafted the manuscript. FH, RY, and IDM designed and organized this report and participated in writing the manuscript. HB reviewed and approved the final manuscript. All authors read and approved the final manuscript.
Corresponding author
Correspondence to
Ryan Yudistiro.
Ethics declarations
Ethics approval and consent to participate
Not Applicable.
Consent for publication
Not Applıcable.
Competing interests
The authors declare that they have no competing interests.
Additional information
Publisher’s Note
Springer Nature remains neutral with regard to jurisdictional claims in published maps and institutional affiliations.
Rights and permissions
Open Access This article is licensed under a Creative Commons Attribution 4.0 International License, which permits use, sharing, adaptation, distribution and reproduction in any medium or format, as long as you give appropriate credit to the original author(s) and the source, provide a link to the Creative Commons licence, and indicate if changes were made. The images or other third party material in this article are included in the article’s Creative Commons licence, unless indicated otherwise in a credit line to the material. If material is not included in the article’s Creative Commons licence and your intended use is not permitted by statutory regulation or exceeds the permitted use, you will need to obtain permission directly from the copyright holder. To view a copy of this licence, visit http://creativecommons.org/licenses/by/4.0/. The Creative Commons Public Domain Dedication waiver (http://creativecommons.org/publicdomain/zero/1.0/) applies to the data made available in this article, unless otherwise stated in a credit line to the data.
Reprints and Permissions
About this article
Cite this article
Hutomo, F., Yudistiro, R., Mulyanto, I.D. et al. False positive finding from malignancy-like lesions on FDG PET/CT: case report of tuberculosis patients.
BMC Med Imaging 20, 26 (2020). https://doi.org/10.1186/s12880-020-00427-w
Download citation
-
Received: 04 June 2019
-
Accepted: 21 February 2020
-
Published: 05 March 2020
-
DOI: https://doi.org/10.1186/s12880-020-00427-w
Keywords
- Tuberculosis
- Malignancy
- FDG
- PET/CT
Новости онкологии
17.02.2020
К дискуссии о роли ПЭТ-КТ в лечении рака молочной железы

Строяковский Даниил Львович
Руководитель химиотерапевтического отделения Городской онкологической больницы №62, член правления RUSSCO, кандидат медицинских наук, Москва
Выражаю исключительно свое собственное мнение, основанное на каждодневной работе и постоянном просмотре дисков КТ, ПЭТ-КТ, МРТ и других рентгенологических исследований, во время консультаций пациентов.
1. Качество ПЭТ-КТ исследования
На мой взгляд, сегодня независимо от нозологии выполнение ПЭТ-КТ исследования без введения внутривенного (в/в) контрастирования делает это исследование неполноценным. Без в/в контрастирования зачастую сложно оценить размер патологических образований и, самое главное, это исследование невозможно использовать в дальнейшем для оценки динамики процесса при сравнении с КТ исследованием. Если сделано ПЭТ-КТ без в/в контраста, то пациенту необходимо делать еще одно исследование – КТ с в/в контрастированием 3 зон (грудная клетка, брюшная полость и малый таз), чтобы дальше можно было оценивать эффективность лечения с помощью КТ. Если сделано сразу ПЭТ-КТ исследование с в/в контрастированием, то КТ-часть этого исследования с в/в контрастированием отлично подходит для оценки эффективности при дальнейшем использовании КТ. На мой взгляд, ПЭТ-КТ без в/в контраста должно быть очень редким исследованием и проводиться только при наличии жестких противопоказаний для введения в/в контраста (например, аллергическая реакция на йод или тяжелая почечная недостаточность). Не должно быть так, что ПЭТ-КТ исследование делают без в/в контраста из-за того, что тариф ОМС при добавлении стоимости контрастного вещества делает исследование менее прибыльным (к сожалению, сегодня это распространенная практика). Как результат – скупой платит дважды: пациенту приходится делать еще одно исследование – КТ с в/в контрастом.
2. Собственно ПЭТ-КТ и рак молочной железы
Для чего нужно делать более углубленные методы исследований при онкологических заболеваниях, такие как КТ, МРТ, ПЭТ-КТ? Углубленное исследование практически может привести к повышению стадии заболевания или, крайне маловероятно, к снижению стадии. Всегда ли это необходимо? Это необходимо делать в том случае, если дополнительные знания о наличии метастатических очагов (регионарных или метастатических), которые не были видны при рутинном обследовании, приведут к изменению тактики лечения. Данное изменение тактики лечения должно быть более благоприятно для лечения пациента, как с точки зрения прогноза и выбора метода, так и последовательности лечения. Если углубленное исследование не приводит к изменению тактики лечения или может создать дополнительные сложности в принятии решения, за которыми не стоит реальное излечение или увеличение продолжительности жизни пациента, то проведение подобного исследования может носить негативный характер.
Локальный рак молочной железы (операбельный). Независимо от биологического подтипа опухоли не требуется проведение ПЭТ-КТ исследования, так как шансы, что будут найдены клинически значимые отдаленные метастазы, очень невелики. Случайно выявленные бессимптомные находки могут затянуть начало лечения, и у некоторых пациенток опухоль может стать местнораспространенной (особенно при агрессивных подтипах, таких как Her2 позитивный, базальный, трижды негативный, или люминальный В с высоким уровнем пролиферативной активности). Ранние локальные стадии рака молочной железы нуждаются в эффективном и безопасном локальном лечении без проведения КТ, ПЭТ-КТ и т.д. и затем в эффективной адъювантной терапии, в зависимости от подтипа опухоли. Например, у больной локальный рак молочной железы, мы делаем ПЭТ-КТ исследование и видим несколько очагов в легочной ткани малых размеров, которые глубоко расположены от плевры и немного накапливают радиофармпрепарат. Данные очаги могут быть как неспецифическими (воспалительными), так и метастатическими. Начинается «пляска» вокруг этих очагов: метастазы, значит IV стадия? значит паллиативное лечение? взять биопсию? торакоскопически? открыто? один очаг возьмем – окажется не метастаз, значит остальные очаги не метастазы? и т.д. Бесконечное количество вопросов…. Действие клинициста или консилиума: берем на себя ответственность, волевое решение – не метастазы. Лечим как раннюю стадию. Но в голове у всех червь сомнений, а вдруг ошибка. Пациентка жить спокойно не может. Врач ёрзает, потому что нет истины в последней инстанции. Начинаем каждые 3-6 месяцев проверять. Увеличивает ли данная информация шансы пациентки на излечение или продолжительность жизни? Обследование затягивается, лечение затягивается, сомнения в правильности, отслеживания и т.д., а всего лишь хотели углубленно посмотреть и обрадоваться, что все прекрасно.
Местнораспространенный рак молочной железы: IIB-III стадии. Более сложная проблема. Здесь очень много факторов влияют на выбор тактики лечения. Основные: биологический тип опухоли, возраст и сопутствующая патология.
Если у больной Her2 позитивный вариант рака молочной железы, то предоперационная химиотаргетная терапия с очень высокой вероятностью перекрывает отсутствие информации о возможных клинически незначимых метастазах, пропущенных при рутинном обследовании. На мой взгляд, лучше лечить пациентку как с III стадией, проводить интенсивное лечение, т.к. это подразумевает куративный (а не паллиативный) подход. Получается, что у ПЭТ-КТ задача: перевести пациентку с III стадией в IV стадию, т.к. будут визуализированы субклинические очаги! А надо ли это? При использовании химиотерапии, с двойной таргетной блокадой, у больной имеются высокие шансы (50-75%) достичь полного лечебного патоморфоза первичной опухоли и л/у (pCR), как суррогат элиминации микрометастазов. При этом понятно, что дистанция между микрометастазами, которые мы еще не видим, и мелкими видимыми метастазами, которые начинаем видеть, очень эфемерная. Соответственно, маленькие, подозрительные или слегка видимые метастазы будут также уничтожены эффективным системным лечением. Лучше для больной и для врачей не знать об их наличии и не сомневаться в необходимости использования эффективной программы для IIB-III стадии. Если мы по какой-то причине решим, что выявленные изменения по КТ или ПЭТ-КТ являются отдаленными метастазами (неважно, так это на самом деле или нет), то терапия будет деэскалирована, хирургический компонент может быть отменен, лучевая терапия отменена, таргетная терапия будет проводиться до прогрессирования или токсичности (а она практически нетоксична) и лечение с паллиативным настроем будет проводиться бесконечно (или очень долго). Причем никто не знает, как долго ее проводить!
Но у больных преклонного возраста с выраженной сопутствующей патологией имеет смысл уточнить стадию процесса, так как данная категория больных с трудом может перенести всю программу радикального лечения, и риск осложнений может превышать потенциальную пользу. В этом случае ПЭТ-КТ может помочь избежать ненужной агрессии, если мы сразу поймем, что имеем дело с IV стадией болезни, и далее безопасно, но при этом достаточно эффективно, длительно лечить пациентку с помощью лекарственной терапии. Но если с помощью ПЭТ-КТ (или КТ) подтвердилась III стадия, то тогда у врачей имеется четкое обоснование для радикального подхода к лечению больной.
Если у пациентки агрессивный вариант трижды-негативного рака. Базальный подтип ~85% от всех трижды-негативных вариантов. Прогноз в данной биологической подгруппе в настоящее время существенно хуже, чем при Her2 позитивном варианте. При локальных, малых опухолях, которые чаще всего являются случайной находкой: хирургия на первом этапе и затем химиотерапия (на мой взгляд, включая карбоплатин) являются основными. Риск выявления отдаленных метастазов незначительный, значит, углубленное обследование не обосновано. Лучше не затягивать начало лечение (чтобы «за время пути собачка не могла подрасти»). При местнораспространенном потенциально операбельном раке IIB-IIIA(B?) лечение должно начаться с неоадъювантной интенсивной химиотерапии, и в данной группе имеются 30-50% шансы на полный патоморфологический ответ, что опять-таки является хорошим предсказательным маркером. В недалеком будущем к неоадъювантной химиотерапии в этой группе будет добавлена иммунотерапия, что еще повысит на 14-15% шансы на pCR и, самое главное, позволит снизить риск раннего прогрессирования (что при трижды-негативном раке бывает очень часто). Отдельная группа трижды-негативного рака – больные с явно неоперабельными IIIB-IIIC стадиями. В этом случае, конечно, очень вероятна конверсия III стадии в IV стадию при проведении ПЭТ-КТ исследования (или просто КТ). И тут стоит задуматься индивидуально, стоит ли это делать. Это индивидуальное решение. IV стадия трижды-негативного рака пока не может быть излечена. Надо ли сразу иметь паллиативную направленность лечения? Или попробовать идти по радикальному пути? Тем более что пациентки (первоначально) очень хорошо отвечают на химиотерапию в большинстве случаев, особенно если химиотерапия дозоинтенсивная и с добавлением платины? Нет однозначного ответа на этот вопрос… Или пожилые пациентки с трижды-негативным вариантом (такие тоже встречаются). В этом случае, на мой взгляд, лучше знать истинную стадию и не откладывать информацию о ней в долгий ящик, так как переносимость интенсивной химиотерапии в этой группе неудовлетворительная, и конверсия стадии, если таковая произойдет (благодаря ПЭТ-КТ), послужит обоснованному паллиативному подходу.
Еще одна, самая многочисленная группа – гормонопозитивный, Her2 негативный вариант. Очень гетерогенная группа.
Пациентки с ранними формами, их много, не нуждаются в углубленном дообследовании. Шансы найти отдаленные метастазы и повысить стадию малы. У больных с местнораспространенным раком шансы найти отдаленные метастазы довольно большие – примерно 20-25%. У молодых и/или у пациентов без существенной сопутствующей патологии нет смысла усугублять стадию с помощью ПЭТ-КТ. Это лишает пациенток радикального подхода к лечению. Конечно, у значительной доли больных с течением времени реализуются отдаленные метастазы. Но это может быть через 3-5-10 лет. Зачем об этом знать с самого начала? Это вопрос спорный. С одной стороны, ранняя информация о наличии бессимптомной метастатической болезни не увеличивает продолжительность жизни (сегодня пока так), просто пациентка живет с информацией о неизлечимости болезни и о том, что лечение (гормонотерапия, химиотерапия и т.д.) будут проводиться всю оставшуюся жизнь, а это многие-многие годы. С другой стороны, если у пациентки изначально 4 стадия, то 1 год жизни (неоадъювантная химиотерапия, операция, лучевое лечение) она потратит на агрессивное лечение, которое не приведет к увеличению общей выживаемости, при этом снизит качество жизни (удаление молочной железы, полгода токсичной химиотерапии, лучевое лечение). Не все пациентки этого бы хотели, и эти обсуждения, безусловно, должны приниматься совместно с пациенткой и, в том числе, в зависимости от ее настроя. Надо объяснить, что мы ждем от ПЭТ-КТ и какие изменения тактики могут быть.
Опять стоит задуматься о больных преклонного возраста и/или с сопутствующей патологией. В этом случае конверсия стадии из III в IV позволяет избежать избыточного химиотерапевтического и локального лечения, которое входит в программу лечения местнораспространенных стадий. В этом случае мы основной упор делаем на гормонотерапию +/- ингибиторы CDK 4/6. И лечение может быть очень эффективным. Долгие годы метастатический процесс контролируется с помощью минимально токсичного лечения. В этой группе знание – сила.
При этом стоит также сказать о «пользе» КТ/ПЭТ-КТ в подходе к диагностике местнораспространенных раков молочной железы. Такой метод исследования дает нам более точное представление об N-cтадировании, в частности, о вовлечении над-подключичных лимфатических узлов или парастернальных, и диктует подход к хирургической агрессии, а также лучевой терапии.
Также стоит отметить, что такие спорные обсуждения и индивидуальные решения не могут быть масштабированы или применяться рутинно вне экспертных центров.
Теперь о метастатическом раке молочной железы. Надо ли делать ПЭТ-КТ и отслеживать эффективность по ПЭТ-КТ? Возникает вопрос: а что такого может дополнительно дать ПЭТ-КТ в сравнении с КТ с контрастом? КТ хорош тем (сейчас практически все КТ мультиспиральные), что воспроизводим, не очень дорог, видит очевидную патологию, удобен для динамического контроля, много аппаратов. Может ли информация о каком-либо дополнительным очаге или группе очагов, которые пропущены на КТ трех зон, поменять тактику лечения? Мой ответ – в небольшом проценте случаев может, так как ПЭТ-КТ делается всего тела (а не только 3-х зон). На ПЭТ-КТ видна голова, проксимальная часть рук и ноги: можно увидеть там какие-либо изменения. Например, увидеть подозрительный бессимптомный очаг в головном мозге, врач направит на МРТ, и если окажется метастаз, то будет проведен гамма-нож (например). Но много ли таких случаев в рутинной клинической практике? Мой опыт говорит, что не более 3-5%, это я сужу по своим ощущениям. Статистику не делал. Может быть, раз в месяц или два вижу подобные находки благодаря ПЭТ-КТ, которые меняют мой подход к выбору лечения. Может ли накопление радиофармпрепарата (SUV) диктовать мне необходимость каких-либо действий, если нет явного очага? КТ тем и хорош, что видит явный очаг (плюс ткань), пропускает клинически незначимые малые очаги (которые практически всегда бессимптомные). Врачу-клиницисту не нужна избыточная и бессмысленная информация, это мешает, создает информационный шум, мешает увидеть главное. Те врачи-клиницисты, кто регулярно смотрит КТ и ПЭТ-КТ, все время видят, что нет совершенного метода, который может со 100% вероятностью отличить онкопатологию от воспаления или неспецифики.
Терапия метастатического рака молочной железы требует видения проблемы болезни и пациентки в целом, и очень редко детализации. На продолжительность и качество жизни практически не влияет, на 1-2 мм больше метастаз или меньше, стал ли немного больше SUV или чуть уменьшился. Для оценки эффективности химиотерапии метастатического рака молочной железы отлично подходит КТ с контрастом. ПЭТ-КТ с контрастом может быть на старте (обезопасить себя, что не прозевали метастаз в мозг или диафиз бедренной кости, например), а затем отслеживать динамику стоит на основании КТ трех зон с в/в контрастом. Некоторые формы метастатического рака молочной железы, например, дольковый рак, вообще плохо видны на ПЭТ-КТ с точки зрения SUV. На фоне гормонотерапии изменения в костных метастазах происходят небыстро, и может быть симптом вспышки (как при сканировании костей), когда на фоне эффективной гормонотерапии сначала SUV может вырасти. При этом структура метастазов начинает меняться в сторону склерозирования, что отражает положительную динамику на фоне лечения (я очень много видел формальных заключений ПЭТ-КТ о прогрессировании на основании роста SUV, тогда как по КТ части исследования и клинически была явная положительная динамика, и вынужден брать на себя ответственность, успокаивать пациентку и продолжать лечение без изменений). Проведение ПЭТ-КТ исследования может быть оправданно, если у больной мы видим олигометастатическую болезнь и задумали какое-то локальное лечение (например, удалить единственный метастаз), тут ПЭТ-КТ очевидный помощник в принятии решения.
В целом, при метастатическом раке молочной железы ПЭТ-КТ практически не имеет преимуществ в сравнении с качественным КТ. Может быть, оправдан на старте терапии. Но не в оценке динамики. Лишь в отдельных случаях, на усмотрение клинициста, ПЭТ-КТ может дать дополнительную ценную информацию.
3. Надо ли делать ПЭТ-КТ при динамическом наблюдении после радикального лечения?
Категорически нет!!! Также как и КТ, МРТ, УЗИ, маркеры, анализы крови и т.д. Раннее выявление бессимптомных метастазов не приводит к увеличению продолжительности жизни. Это не то же самое, что рано выявить первичную опухоль. Это – рано выявить фактически IV и неизлечимую стадию. При отсутствии симптоматики не нужно искать метастазы – это несет вред в большинстве случаев. Иногда, правда, можно случайно выявить другую опухоль ранней стадии (например, рак толстой кишки) и тогда вовремя прооперируют, но это все как случайный выстрел, который попал в десятку (в жизни все бывает). Не стоит заниматься скринингом с помощью ПЭТ-КТ. А что делать? Только маммографию неудаленной железы или обеих, если была органосохранная операция. Почему? Потому что у больных, перенесших рак молочной железы, повышается риск повторного первичного рака молочной железы. И лучше его выявить раньше. Повторная радикальная терапия локальной стадии имеет практически такой же шанс на успех, как и предыдущая.
Заключение
У ПЭТ-КТ есть ограниченная роль в лечении рака молочной железы. Назначение ПЭТ-КТ должно быть инициировано врачом-клиницистом, который реально разбирается во всех тонкостях болезни и понимает, для чего ему будет нужна потенциально новая информация. Ни в коем случае нельзя делать ПЭТ-КТ по требованию пациентки или ее родственников (сегодня медицина зачастую работает по принципу: чего изволите-с). ПЭТ-КТ не должно быть заменой КТ только потому, что проще направить и быстрее сделают, так как на КТ очередь, а ПЭТ-КТ оплачивает ОМС.
Вместе с тем, я благодарен системе, что ПЭТ-КТ была включена в ОМС почти 5 лет назад и так распространилась. Это значительно добавило мне знаний и понимания биологии разных болезней, в том числе рака молочной железы. Без этого я не смог бы сегодня поделиться своими мыслями (их бы просто не было). И еще (для врачей клиницистов, которые решают, как лечить): чтобы легко просматривать диски (КТ, МРТ, ПЭТ-КТ) скачайте из инета RADIANT для Windows. Это бесплатная программа. «Жует» практически все диски и виды DICOM программ. Последняя версия позволяет создать собственный архив, что очень важно при повторном визите пациента. Относительно быстро грузит (зависит от диска). Позволяет выводить фронтальную и сагитальную проекции, если сделаны тонкие срезы. Кнопочка F (фьюжен) позволяет сделать отличную картину ПЭТ-КТ со свечением. Нажатием на колесико мыши можно регулировать яркость ПЭТ изображения (спасибо Максиму Смолярчуку). Рекомендую, всегда смотреть imaging своих пациентов и не принимать решения на основании формальных заключений.
ПЭТ-КТ — это комплексное исследование тканей организма в рамках онкологического поиска. Методика основана на применении двух отдельных составляющих:
- ПЭТ или позитронно-эмиссионной томографии. Представляет собой способ визуализации измененных, чаще всего раковых тканей, основываясь на контрастировании наиболее «прожорливых» клеток препаратами на основе глюкозы и специального радиоактивного компонента.
- КТ — классическая компьютерная томография, которая позволяет визуализировать здоровые ткани.
Более чем в 90% случаев ПЭТ-КТ проводится для диагностики рака, уточнения характера и особенностей патологического процесса.

- В каких случаях назначают ПЭТ-КТ
- Противопоказания к исследованию
- Суть диагностики методом ПЭТ-КТ
- Всегда ли этот метод на сто процентов информативен
- Нужна ли специальная подготовка
- Преимущества методики
- Недостатки методики
- Как часто следует проводить исследование
В каких случаях назначают ПЭТ-КТ
ПЭТ-КТ — методика визуализации преимущественно раковых опухолей. Поскольку они отличаются повышенной потребностью в питании. Если говорить о показаниях более подробно, методика требуется в рамках:
- Дифференциальной диагностики злокачественных и доброкачественных опухолей. Первые копят специальный контрастирующий препарат. Вторые — нет или в минимальной, ничтожной степени.
- Оценка стадии злокачественного процесса. Определение фазы онкологического заболевания.
- Изучение характера опухоли, степени ее агрессивности по скорости обмена веществ.
- Планирование биопсии. В рамках позитронно-эмиссионной томографии врачи ищут наиболее активную область опухоли, где клетки претерпели наибольшее изменение, и их плотность физически выше.
- Мониторинг состояния после пройденного лечения. ПЭТ-КТ могут проходить раз в год или реже. В зависимости от того, какой был рак, насколько агрессивный, радикальное ли лечение получил пациент. ПЭТ нужен чтобы на ранних стадиях обнаружить рецидив онкологического процесса.
- Планирование хирургического лечение или лучевой терапии. Чтобы определить агрессивность неоплазии и проработать грамотную тактику борьбы с образованием. ПЭТ не помогает понять тип опухоли. Потому помимо требуется еще и гистологическое исследование образца.
- Поиск первичного очага при наличии метастазов.
ПЭТ-КТ универсальная методика диагностики и изучения деталей онкологических процессов. Но при низкой интенсивности обменных процессов в опухоли возможны опасные с точки зрения информативности погрешности и ошибки.

Противопоказания к исследованию
ПЭТ-КТ – исследование безопасное. Но ряд противопоказаний у него все же есть:
- Острые воспалительные процессы асептического характера. То есть не связанные с инфекционными агентами: поражениями грибками, вирусами или бактериями.
- Инфекционно-воспалительные процессы в острой и подострой фазах. Пока не наступило полного выздоровления. До тех пор, пока состояние полностью не нормализуется.
- Беременность, независимо от фазы. Исключая случаи, когда провести диагностику жизненно необходимо и других вариантов не остается.
- Психические расстройства в декомпенсированной фазе. Тяжелые психозы, алкогольный делирий, бредовый состояния. Пока человек не придет в себя.
- Период грудного вскармливания. Если пройти КТ жизненно необходимо, после процедуры мать отказываться от естественного вскармливания и переходит на специальные смеси.
- Общее тяжелое состояние человека.
- Диабет, как 1-го, так и 2-го типа.
- Тяжелые поражения печени или почек. Поскольку препарат будет выводиться непозволительно медленными темпами. Отсюда повышенный риск интоксикации всего организма.
Перед проведением ПЭТ-КТ следует проконсультироваться с врачом. На случай, если имеются противопоказания. Он взвесит все «за» и «против». Решит, стоит ли проводить позитронно-эмиссионную томографию несмотря на формальные основания этого не делать.

Суть диагностики методом ПЭТ-КТ
В основе ПЭТ-КТ лежат две технологии.
Первая, на которой зиждется ПЭТ — это качественная оценка метаболизма тканей. Раковый опухоли отличаются крайней «прожорливостью». Для роста и развития им требуется много веществ. Настолько много, что остальной организм остается в состоянии дефицита. Для определения таких ненасытных тканей используется вещество, которое универсально и нужно всем клеткам – глюкоза.
Чтобы зафиксировать интенсивность и степень накопления глюкозы в измененных клетках, ее маркируют специальным радиоактивным веществом. В значительной части случаев используются препараты радиоактивного фтора. Они отличаются большим периодом полураспада, без проблем транспортируются и хранятся. А с другой стороны, не вызывают токсического и радиоактивного поражения организма пациентов.
Препарат с такой маркировкой накапливается в измененных тканях, окрашивая наиболее агрессивные области. Врачи получают визуальное подтверждение, картинку. Результаты исследования дают возможность сделать выводы, какая опухоль имеет место.
Минус технологии — ПЭТ показывает только измененные ткани. Чтобы посмотреть, как опухоль соотносится с тканями здоровыми, применяют КТ. Картину компьютерной томографии накладывают на картину ПЭТ, получая единый снимок высокого качества.

Всегда ли этот метод на сто процентов информативен
К несчастью, даже такой высокочувствительный способ диагностики как ПЭТ-КТ не может быть на все сто информативным. Некоторые неоплазии обладают малой скоростью метаболизма:
- Раковые неоплазии щитовидки.
- Опухоли печени.
- Неоплазии почек.
- Раковые образования предстательной железы.
- Раковые опухоли костной ткани.
- Некоторые саркомы и лимфомы.
Недостаточная визуализация не означает, что проблемы нет. Требуются другие методы диагностики.
Ровно так же и окрашивание тканей не говорит о наличии рака. Старые поколения препаратов для контрастирования могут копиться и в здоровых тканях. Поэтому при расшифровке специалисты ориентируются на комплексную картину.

Нужна ли специальная подготовка
Подготовка простая:
- За сутки до исследования нужно снизить углеводную нагрузку. Углеводы исключают из рациона. Жевательная резинка также запрещена. В том числе с сахарозаменителем.
- За 8-10 часов нужно отказаться от пищи. Исследования проходят натощак. Воду пить разрешается.
- За сутки до процедуры стоит избегать интенсивной физической нагрузки.
Важно взять с собой заключения врачей и результаты иных диагностических мероприятий.
Преимущества методики
ПЭТ-КТ обладает несколькими весомыми плюсами:
- Комплексный характер, универсальность. Позитронно-эмиссионная и компьютерная томография позволяют исследовать любые органы.
- Высокая точность и информативность исследования.
- Возможность диагностики рака на ранних стадиях.
- Отсутствие боли и дискомфорта.
- Отсутствие необходимости госпитализации. Все проходит амбулаторно.
Есть и минусы.

Недостатки методики
Самый главный недостаток – это необходимость применения радиоактивных препаратов. Но при должном подходе есть возможность снизить лучевую нагрузку на организм.
Как часто следует проводить исследование
Частоту проведения исследования определяет врач, отталкиваясь от клинического случая. ПЭТ-КТ может проводиться как методика первичной диагностики, а также в рамках мониторинга патологического, онкологического процесса.
ПЭТ/КТ-исследование — что это?
Расшифровка аббревиатуры звучит как позитронно-эмиссионная томография – компьютерная томография. Данный метод диагностики совмещает исследование структуры и функциональных характеристик тканей. Особенно широко технологию применяют в онкологии для выявления и определения степени развития злокачественных опухолей.
Почему?
Сегодня в мире до 90% ПЭТ/КТ-исследований проводят у людей, которые страдают раковыми заболеваниями. Исследование важно с точки зрения ряда аспектов:
- Исследование важно с точки зрения определения степени развития и распространения опухолевого процесса, обнаружения метастазов, как региональных, так и отдаленных.
- В медицинской практике случаются ситуации, когда врачам неясен характер процесса, проистекающего в том или ином органе. Исследование позволяет дифференцировать процесс, различить доброкачественный либо злокачественный.
- Исследование помогает понять, эффективно ли проводимое лечение.
- Исследование может применяться как диагностика рецидива заболевания.
Если говорить о диагнозе, то многие раковые опухоли имеют способность активно накапливать фтордезоксиглюкозу. Это вещество применяют в ходе исследования. Однако некоторые виды раковых опухолей обладают низким метаболизмом.
К таким видам относятся:
- Высокодифференцированные раковые новообразования щитовидной железы;
Доброкачественные опухоли любых локализаций; - Часть опухолей почек;
- Некоторые опухоли костной ткани;
- Опухоли печени;
- Опухоли предстательной железы;
- Некоторые виды сарком, лимфом.
Имея низкий уровень метаболизма, они плохо визуализируются по данным ПЭТ/КТ. А это означает, что требуются иные диагностические методы.
Описание технологии исследования
Основу технологии исследования составляет изучение особенностей тканей, структурных и функциональных. Функциональные особенности можно оценить благодаря обмену веществ. Приведем следующий пример. Выбираем вещество, которое необходимо всем клеткам организма. Маркируем его радиоактивной меткой, вводим в организм и наблюдаем места его максимального накопления.
Глюкоза – универсальное вещество в организме человека. С помощью глюкозы происходит питание практически всех тканей и клеток. В злокачественных опухолях происходит наибольшее ее потребление, так как рост и размножение опухолевых клеток требует много энергии.
В ходе ПЭТ/КТ-исследования глюкоза маркируется радиоактивными атомами с коротким периодом полураспада. Попав в организм глюкоза в активно накапливается в тканях с наиболее интенсивным метаболизмом, т. е. в раковых опухолях.
Метка распадается, излучая при этом энергию в виде гамма-лучей. Специальный прибор регистрирует данный процесс. Данные, которые получает врач, складываются визуальную модель, показывающую место расположения новообразования, его размеры и метастазы.
Радиоактивные метки скапливаются только в месте локации атипичных клеток, здоровые ткани не визуализируются.
Когда врачу необходимо рассмотреть и здоровые, и измененные структуры, на помощь приходит КТ, позволяющая получить детальную картинку с точностью до миллиметра.
После того как данные от обеих сканирующих систем получены, их накладывают друг на друга, добиваясь тем самым изображения, дающее четкое представление о локации опухолевых очаги.
Преимущества
Перечисленные ниже преимущества метода относятся к неоспоримым:
- Высокая точность вследствие совмещения в одном исследовании нескольких видов диагностики;
- Безболезненность;
- Возможность диагностики онкологии рака на стадии, когда еще симптомы не выражены;
- Возможность исследования одновременно всех органов;
- Амбулаторное проведение без госпитализации.
Недостатки
Главный недостаток – необходимость применения препаратов радиоактивных. Однако в общем ценная информация полученная в ходе исследования, перекрывает побочные эффекты.
Необходимо придерживаться трех главных правил:
- Обоснованность исследования;
- Оптимизация лучевой нагрузки;
- Соблюдение норм и правил радиационной безопасности.
Виды используемых препаратов
Потенциал исследования зависит от арсенала радиофармпрепаратов, которые используются в нем. Эти препараты маркированы нестабильными изотопами, которые делают их радиоактивными.
Сегодня для процедуры исследования широко используют изотопы таких элементов, как:
- Азот-13;
- Кислород-15;
- Углерод-11;
- Фтор-18.
В онкологии наиболее распространен фтор, так как у него наибольший период полураспада и при этом наименьшая энергия излучения.
Эти преимущества фтора делает возможным получить высококачественные изображения с высоким пространственным разрешением. Кроме того, относительно длительный период полураспада делает возможным транспортировать препарат от места производства до клиники.
Самый распространенный применяемый препарат – фтордезоксиглюкоза. Она представляет собой аналог глюкозы. Атипичные клетки поглощают его быстрее, он активно скапливается, а это для сканирования идеально.
Недостаток фтордезоксиглюкозаэтого – накапливание его в тканях мозга и нефронах, что, в свою очередь, может стать причиной подсвечивания этих органов, даже когда они здоровы.
Данный недостаток стимулировал поиск иных, более совершенных препаратов, и сейчас таковые созданы.
Примером современного препарата может служить 18F-FET. Предназначен он для головного мозга и содержит аминокислоту тирозин, меченую изотопом фтора-18. У тирозина избирательная накопительность в ткани мозга очень высокая, это важно для визуализации нейроопухолей.
Препарат используют также в целях диагностики новообразований ротоглотки, для обнаружения метастазов и диагностики поражения шейных лимфатических узлов.
Показания к исследованию
- Поиск первичного очага опухоли при обнаружении метастазов;
- Определение стадии онкологического процесса;
- Дифференцированная диагностика рецидива и изменений послелечебных;
- Мониторинг течения заболевания, выявление рецидива;
- Планирование радиотерапии и хирургической манипуляции;
- Планирование биопсии и нахождение наиболее агрессивной зоны опухоли.
Противопоказания
- Период беременности;
- Период вскармливание грудью;
- Диабет;
- Тяжелое состояние больного;
- Невозможность пройти процедуры вследствие, например, психического заболевания;
- Острая инфекция;
- Острое хроническое воспаление.
Подготовка
При подготовке к обследованию необходимо придерживаться ряду правил:
- За сутки до назначенной процедуры соблюдать безуглеводную диету.
- Придти на исследование натощак.
- Накануне исследования избегать больших физических нагрузок.
- В день проведения процедуры пить обычную воду.
- Отказаться от жевательной резинки.
- На процедуру явиться в удобной комфортной и желательно теплой одежде.
Рекомендуется принести на процедуру исследования информацию о заболевании, диагнозы, выписки из других стационаров, результаты иных исследований и т.д.
Проведение
Самой процедура укладывается в час, однако необходимо иметь в виду подготовку, оформление необходимых бумаг и послепроцедурный отдых.
Процедуру проходят в комфортной одежде, необходимо снять все металлосодержащее.
Необходимо сообщить врачу о болезненных ощущениях, которые могут возникнуть от долгой неподвижности. Учитывая это, он сможет подобрать индивидуальный режим проведения процедуры.
После инъекции необходимо лежать молча, неподвижно и расслабленно. Неподвижность благотворно влияет на правильное распределение введенного препарата. Это важно для качества изображения.
Первый этап обследования – введение препарата. Длится он примерно час. Вводят препарат внутривенно. Иногда пациент может ощущать жар, не более того. Распределение препарата по клеткам длится примерно час.
Второй этап – сканирование. Пациент в томографе. Первой выполняют КТ, затем – ПЭТ. Если требуется, вводят дополнительно вещество контрастное. Длительность этого этапа варьируется от двадцати до сорока минут.
По окончании происходит наложение снимков КТ и ПЭТ.
Что после?
После в течение суток не рекомендуется находиться в местах скопления людей, тем более контактировать с беременными женщинами и с детьми. В семье необходимо соблюдать социальную дистанцию 1 -1,5 друг от друга.
Необходимо потреблять много жидкости, два с половиной литра и более. Это необходимо, чтобы быстрее и безопаснее вывести контраст и радиофармпрепарат.

Пить можно любые бескофеиновые напитки, а не только воду
Осложнения
Осложнения при проведении процедуры обследования главным образом связаны с введением контраста.
Это может быть:
- Аллергия, вызванная пунктированием вены;
- Повреждение сосудов;
- Возникновение гематомы;
- Неврит
Очень редкое осложнение – нарушение работы почек.
Пероральное введение контраста может вызвать тошноты, рвоту, диарея.
После проведения процедуры может возникнуть головокружение, слабость из-за того, что желудок пустой.
Лучевая нагрузка на пациента при обследовании
На выбор лучевой нагрузки влияет используемый радиофармпрепарат и объем исследования. Так сканирование головы требует меньше облучения, чем сканирование всего тела. Минимизация вреда от применения метода достигается, если следовать следующие требования:
- Применять изотопы, у которых время полураспада несколько минут или часов;
- Рассчитывать дозу индивидуально для каждого пациента, учитывая его возраст, рост, вес;
- Использовать на сканерах специальные фильтры, а также программы, снижающие дозы излучения;
- Потреблять необходимое количество жидкости, это позволит быстрее вывести радиофармпрепарат из организма
Обратившись в клинику интегративной онкологии Onco.Rehab, Вы узнаете, где лучше пройти исследование, о котором мы Вам рассказали в этой статье.
Позитронно-эмиссионная томография (ПЭТ) представляет собой метод исследования, при котором оборудование регистрирует попадание на детекторы пары гамма-фотонов, испущенных в результате аннигиляции позитрона и электрона.
Для доставки позитронов к тканям и органам в организм вводят специальное вещество, в состав которого входит радионуклид. Последний в организме распадется с образованием позитрона, который и аннигилирует с расположенным поблизости электроном. При этом испущенные гамма-кванты имеют одинаковую энергию и двигаются строго по прямой в противоположных направлениях.
Когда пара детекторов, расположенных друг против друга, регистрируют получение квантов одинаковой мощности, компьютер вносит данные об этом событии в модель, формируя таким образом трехмерное изображение.
На сегодняшний день наиболее широко используются радиофармпрепараты на основе изотопа фтор-18 (18F-фтордезоксиглюкоза или 18-ФДГ). У этого изотопа есть важное преимущество: его период полураспада составляет почти 109,8 минуты, по сравнению с 2-20 минут у других изотопов. Это позволяет успеть доставить препарат в клинику и провести процедуру без лишней спешки. Кроме того, 18F-фтордезоксиглюкоза в организме ведет себя как обычная глюкоза, легко проникая в клетки тканей, позволяя получить наиболее полную картину.
Современные ПЭТ-КТ аппараты позволяют обнаружить новообразования с размерами от 4-5 мм.
В каких случаях назначается ПЭТ
ПЭТ диагностика применяется для выявления широкого спектразлокачественных опухолей костей, мягких тканей и различных органов, а также для того, чтобы оценить результативность промежуточного лечения. Метод также позволяет с большой долей вероятности отличить злокачественные опухоли от доброкачественных без проведения биопсии.
ПЭТ-КТ применяется при:
- Опухолях, расположение которых не выявлено;
- Опухолях головы, шеи и головного мозга;
- Раке щитовидной железы;
- Меланоме;
- Опухоли легкого;
- Ракемолочной железы;
- Раке пищевода, желудка и толстой кишки;
- Лимфоме;
- Болезни Ходжкина;
- Раке шейки матки, яичников, тимуса и яичек;
- Саркоме мягких тканей;
- Неходжкинскихлимфомах;
- Опухолях костей.
Стоит сказать, что, хотя ПЭТ и относится к неинвазивным обследованиям, пациент получает значительную дозу облучения от 14мЭв до 26мЭв (при ПЭТ-КТ всего тела). Кроме того, вводимый препарат в организме ведёт себя как глюкоза, вследствие чего обследование не назначают беременным, больным туберкулезом, а также имеющим повышенный уровень сахара в крови.Обследование с осторожностью назначают больным сахарным диабетом, имеющим почечную недостаточность, и женщинам в период лактации.
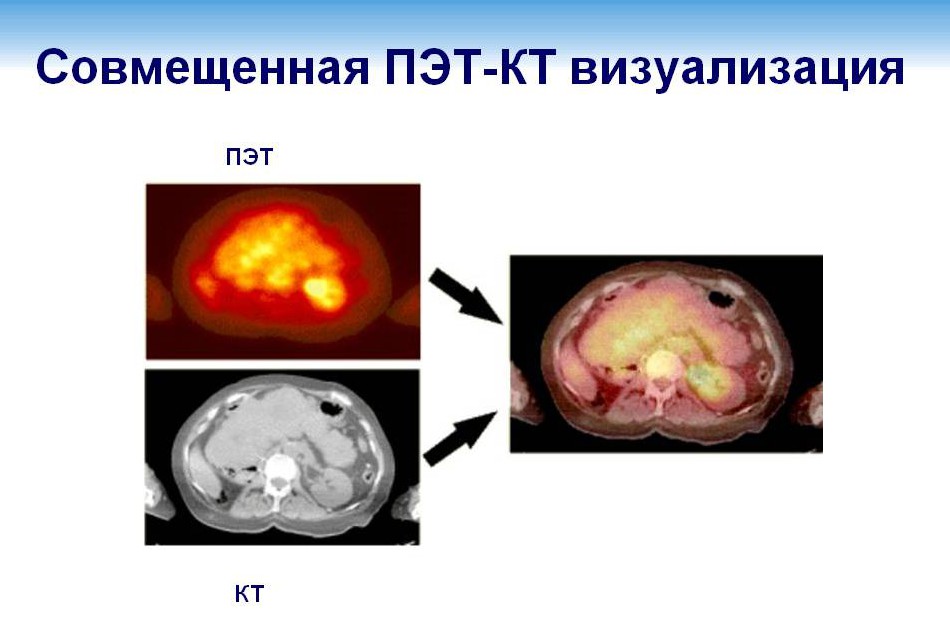
Возможны ли ошибки при ПЭТ-диагностике
К сожалению, как и при большинстве обследований, вполне возможно возникновение ошибок, которые могут иметь объективные и субъективные причины. Методы ПЭТ и ПЭТ-КТ не являются абсолютно точными. Отчасти это происходит потому, что точность применяемой аппаратуры не идеальна и, хотя она постоянно улучшается, все еще остается вероятность получить ошибочный результат. Кроме того, за злокачественные опухоли могут быть приняты совершенно другие болезни, дающие на ПЭТ очень сходную картинку. В этом случае пациенту будет поставлен диагноз рак, который впоследствии не будет подтвержден по результатам биопсии и гистологии.
Второй источник ошибок ПЭТ-КТ диагностики – неправильная интерпретация. Аппарат ПЭТ-КТ просто фиксирует полученные фотоны и складывает их в общую картину, а ее анализом занимается врач-радиолог. Учитывая, что метод появился относительно недавно, большого количества специалистов в стране еще нет, а у имеющихся часто недостаточно личного опыта, что и порождает неточности в постановке диагноза или составлении плана лечения.
Второе мнение
Учитывая риск ошибки при анализе результатов сканирования, чрезвычайно важной является возможность получения альтернативного или, лучше сказать, второго мнения. Возможно, это и не поможет снизить ошибки, связанные с неточностью аппаратной части, но наверняка позволит в несколько раз уменьшить влияние человеческого фактора.
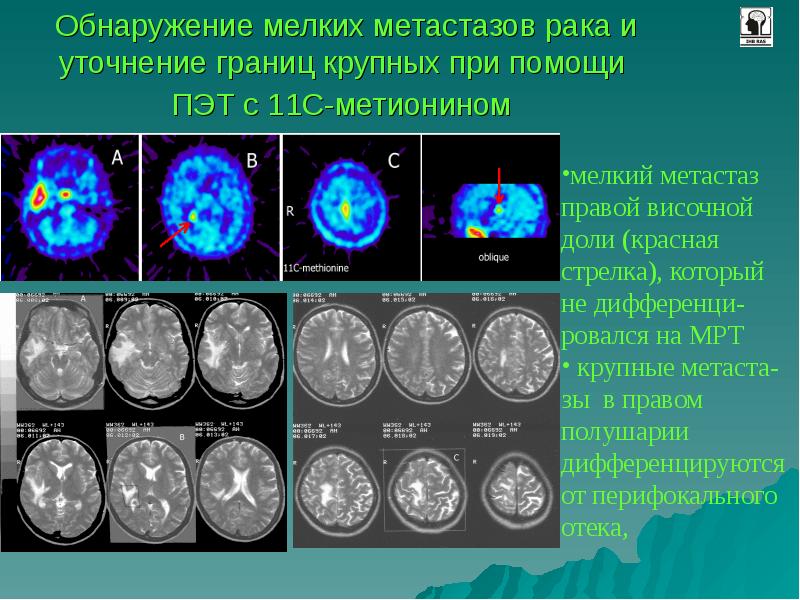
К сожалению, сегодня далеко не всегда в городе можно найти двух врачей, имеющих высокую квалификацию в ПЭТ-КТ. С другой стороны, результаты сканирования можно передать по интернету в любую точку планеты. В России для этого вы можете воспользоваться услугами Национальной телерадиологической сети. Загрузив данные, вы уже через сутки получите второе заключение, составленное врачами-радиологами, работающими в Санкт-Петербургском институте мозга человека и других ведущих учреждениях.
Второе мнение не только даст возможность минимизировать риск ошибки, но и позволит правильно подобрать лечение и спланировать оперативное вмешательство.
ПОЛУЧИТЬ ВТОРОЕ МНЕНИЕ ПО ПЭТ-КТ
ПЭТ-КТ – это гибридный метод обследования. Он объединяет:
ПЭТ – это метод ядерной медицины, который показывает уровень обмена веществ (метаболизм) в различных участках тела. Для этого в организм пациента вводят небольшие количества радиоактивных веществ, которые называют радиотрейсерами или радиофармпрепаратами. Они накапливаются в опухолях, местах воспаления или связываются с определенными белками в организме. С помощью ПЭТ можно увидеть интенсивность накопления радиотрейсера и диагностировать заболевание на ранних стадиях.
КТ — метод получения поперечных изображений (срезов) костей, кровеносных сосудов и мягких тканей тела. Во время КТ серию рентгеновских снимков, сделанных под разными углами, объединяют с помощью компьютерной обработки. В результате можно получить детальное послойное изображение органов и тканей, установить местоположение опухоли и ее границы.
При объединении ПЭТ с КТ, врач может получить детальную информацию об изменениях в строении и метаболизме еще на клеточном уровне. В результате, после ПЭТ-КТ пациент раньше получает правильное лечение, что увеличивает шансы на выздоровление.
Когда используют ПЭТ-КТ?
ПЭТ-КТ никогда не назначают полностью здоровым людям. Чаще всего исследование необходимо при уже установленном диагнозе рака. ПЭТ-КТ в онкологии позволяет:
- определить стадию рака (степень распространения злокачественного процесса по организму);
- подобрать наиболее подходящее лечение;
- оценить ответ на лечение, например эффективность химио- или лучевой терапии;
- диагностировать рецидив рака до появления симптомов.
ПЭТ-КТ используют не только при раке. Метод позволяет максимально точно оценить строение и работу мозга и сердца, что помогает:
- оценить метаболизм и жизнеспособность тканей;
- определить последствия перенесенного инфаркта миокарда;
- предсказать возможную пользу от ангиопластики или коронарного шунтирования;
- выявить и изучить аномалии головного мозга — опухоли, нарушения памяти, судороги и другие заболевания центральной нервной системы.
Противопоказания и риски при ПЭТ-КТ
ПЭТ-КТ — это безболезненный и безопасный метод диагностики. Все же возможны редкие нежелательные явления связанные с:
- реакцией или аллергией на радиофармпрепарат;
- пребыванием в закрытом тоннеле аппарата, что может быть неприятным для людей с клаустрофобией.
Для того чтобы сделать процедуру максимально комфортной, в некоторых медицинских центрах, например турецкой клинике Медиполь, аппараты для ПЭТ-КТ способны создавать декорацию небосвода.
Из-за возможного негативного влияния рентгеновских лучей и радиотрейсера на плод, не желательно делать ПЭТ-КТ при беременности. Все же это противопоказание не абсолютное, поэтому в редких ситуациях ПЭТ-КТ проводят и беременным. Анализ подобных случаев не выявил плохого влияния на плод.
Мифы, связанные с ПЭТ-КТ
В интернете и на многих пациентских форумах можно найти много неправдивой информации о ПЭТ-КТ. Часто, это умозаключения людей, не связанных с медициной, которые не подтверждены результатами исследований.
ПЭТ-КТ — лишняя трата денег, можно обойтись обычной КТ или МРТ
Ряд клинических исследований сравнивали ПЭТ-КТ с другими методами визуализации. Было установлено, что у трети пациентов технология ПЭТ/КТ выявляет изменения, которых не было найдено на обычной ПЭТ или КТ. Это позволяет сразу подобрать правильное лечение и увеличить шанс на выздоровление.
Для примера, у одного из реальных пациентов с раком легкого, ПЭТ/КТ выявило не только первичную опухоль в легком, которую ранее обнаружили на КТ, но и дополнительную опухоль, которую на КТ видно не было.
Если бы врач руководствовался только результатами КТ, он бы рекомендовал операцию. Дополнительная опухоль, обнаруженная с помощью ПЭТ/КТ, показала, что рак распространился и был неоперабельным. Основываясь на этой информации, врач приступил к лучевой терапии, что дало пациенту больше шансов на выживание.
Доза радиации при ПЭТ-КТ большая и может вызвать прогрессирование рака
Мир вокруг нас постоянно излучает радиацию. Так, жители России и США ежегодно получают дозу фонового радиационного излучения около 3 миллизиверта (мЗв). В Рамсаре и Иране ежегодное фоновое облучение в разы выше и составляет до 260 мзВ. Радиационный фон формируют многие источники, включая:
- космическое излучение;
- радиоактивность окружающей среды от естественных радиоактивных материалов, например, радона и радия;
- излучение в результате испытаний ядерного оружия и радиационных аварий.
При этом не все люди вокруг болеют раком. Дело в том, что человеческое тело оснащено механизмами восстановления для борьбы с повреждениями, вызванными низкими дозами радиации. Таким образом, люди могут переносить низкие дозы радиации без риска развития рака. Средняя доза облучения при ПЭТ-КТ составляет всего 25 мЗв, а значит организм может легко с ней справиться.
Я буду излучать радиацию много дней после процедуры
Некоторые люди думают, что радиоактивный изотоп долго не выводиться. На самом деле, через 12 часов после ПЭТ-КТ доза выделяемой радиации будет настолько низкой, что можно безопасно кормить ребенка грудью. Через сутки после процедуры в вашем организме совсем не останется радиотрейсера.
Как подготовиться к ПЭТ-КТ?
Для того чтобы результаты ПЭТ-КТ были максимально точными, следует придерживаться нескольких простых правил.
- За сутки до обследования нужно воздержаться от интенсивных физических нагрузок.
- Последний прием пищи должен быть не позже, чем за 4-6 часов перед процедурой.
- Следует пить достаточно жидкости, чтобы избежать обезвоживания.
- Нельзя жевать жевательную резинку или рассасывать любые карамельки или леденцы, в том числе и от кашля;
- Кольца, серьги и другие украшения перед обследованием нужно будет снять, поэтому лучше изначально оставить их дома.
- Желательно одевать удобную свободную одежду, хотя, перед процедурой на вас наденут одноразовую медицинскую робу.
Радиофармпрепараты, которые используют при ПЭТ-КТ, содержат глюкозу, поэтому, пациентам с сахарным диабетом нужна более тщательная подготовка к процедуре. Иногда нужно отменить сахаропонижающие лекарства за несколько дней до обследования. При использовании инсулина, последнюю дозу следует вводить не позже, чем за 4 часа до процедуры.
Обязательно сообщите врачу если вы:
- имеете хронические заболевания;
- принимаете какие-либо лекарства, включая витамины и растительные препараты;
- подозреваете беременность или беременны;
- когда-либо имели аллергию.
Чего ожидать во время ПЭТ-КТ?
Обследование включает в себя два этапа — поглощения и сканирования.
І — Этап поглощения
На этапе поглощения пациенту вводят радиотрейсер, чаще внутривенно, и ждут, пока он распределится по организму. Во время введения индикатора и 45-60 минут после, пациенту:
- нужно сидеть или лежать неподвижно;
- нельзя разговаривать и не жевать, чтобы избежать усиленного накопления радиофармпрепарата в мышцах гортани и шеи и искажения результатов ПЭТ-КТ;
- следует находиться в тепле.
Последнее нужно не только для комфорта пациента. Во время процедуры важно не мерзнуть, так как это может привести к накоплению препарата в жировой ткани. В идеале, обследуемого следует укрыть за 30–60 минут до введения радиотрейсера и согревать в течение всей ПЭТ-КТ.
ІІ — Этап сканирования и получения изображений
- Пациента помещают в специальный аппарат для ПЭТ-КТ.
- Через тонкие слои его тела в разных направлениях пропускают рентгеновские лучи.
- Электронные рентгеновские детекторы фиксируют излучение с разных участков тела и передают его на компьютер.
- Параллельно, специальные датчики гамма-излучения фиксируют излучение от введенного внутривенно радиотрейсера.
- Полученное изображение активности обмена веществ “накладывают” на послойное изображения тела.
В результате врач получает информацию о строении и обмене веществ различных органов в высоком разрешении. Процедура непосредственного сканирования длится около 30 минут.
Как вести себя после ПЭТ-КТ?
ПЭТ-КТ – это амбулаторная процедура. Для ее проведения не нужно ложиться в больницу. Покинуть клинику можно сразу после окончания сканирования.
В течение некоторого времени после обследования человек излучает небольшую дозу радиации. Для того чтобы обезопасить себя и окружающих, в течение 12 часов после процедуры следует:
- Ограничить близкие контакты с маленькими детьми и беременными женщинами;
- Отказаться от грудного вскармливания. В течение 12 часов молоко следует просто сцеживать, после чего можно возобновить привычный режим кормления.
Для того чтобы ускорить выведение радиотрейсера с организма пейте много жидкости. Сразу после обследования можно вернуться к обычному режиму питания.
Зачем ехать на ПЭТ-КТ за границу?
ПЭТ-КТ является золотым стандартом диагностики большинства злокачественных заболеваний. В тоже самое время, во многих странах метод остается недоступным. Например, в Украине существует всего 4 аппарата ПЭТ-КТ. В результате, не так много отечественных специалистов знают, как расшифровать полученные результаты, а многие пациенты не попадают на диагностику из-за очередей.
Преимуществами проведения ПЭТ-КТ за рубежом является:
- современное материально-техническое оснащение;
- отсутствие многомесячных очередей;
- процедуру проводят и интерпретируют врачи с 30-летним стажем в ядерной медицине.
Где можно сделать ПЭТ-КТ за границей?
ПЭТ-КТ пациентам из-за рубежа успешно делают в клиниках Турции, Германии, Испании, Израиля. При выборе клиники следует учитывать множество факторов, включая:
- диагноз;
- сопутствующие заболевания;
- пожелания пациента.
Оставьте заявку и наши врачи-координаторы бесплатно подберут наиболее подходящий центр, с учетом ваших пожеланий и особенностей заболевания.
На каких аппаратах делают ПЭТ-КТ за границей?
Хотя ПЭТ-КТ и так является инновационным методом диагностики, в клиниках за рубежом ее проводят на самых совеременных аппаратах. Так, в медицинском госпитале Медиполь (Турция), для ПЭТ-КТ используют томограф премиум-класса Philips Gemini TF. Главными преимуществами аппарата являются:
- сниженная лучевая нагрузка;
- использование более низких доз радифармпрепарата, что уменьшает стоимость диагностики;
- меньшая длительность обследования;
- повышенная точность полученных изображений;
- возможность обследовать крупных пациентов;
- открытый дизайн, который обеспечивает повышенный комфорт для тревожных пациентов и пациентов с клаустрофобией.
Сколько стоит ПЭТ-КТ за рубежом?
Стоимость ПЭТ-КТ за рубежом стартует от $650, однако широко варьируется и зависит от многих факторов. На цену влияет:
- заболевание, из-за которого проводят обследование;
- тип радиофармпрепарата;
- страна и клиника.
Так, цена ПЭТ-КТ с Галлием, которая является золотым стандартом диагностики рака простаты, начинается уже от $2000. Воспользовавшись формой справа, можно оставить заявку и получить детальную консультацию от наших врачей-координаторов и узнать актуальную стоимость ПЭТ-КТ в каждой из клиник.
ПЭТ-КТ — это комплексное исследование тканей организма в рамках онкологического поиска. Методика основана на применении двух отдельных составляющих:
- ПЭТ или позитронно-эмиссионной томографии. Представляет собой способ визуализации измененных, чаще всего раковых тканей, основываясь на контрастировании наиболее «прожорливых» клеток препаратами на основе глюкозы и специального радиоактивного компонента.
- КТ — классическая компьютерная томография, которая позволяет визуализировать здоровые ткани.
Более чем в 90% случаев ПЭТ-КТ проводится для диагностики рака, уточнения характера и особенностей патологического процесса.

- В каких случаях назначают ПЭТ-КТ
- Противопоказания к исследованию
- Суть диагностики методом ПЭТ-КТ
- Всегда ли этот метод на сто процентов информативен
- Нужна ли специальная подготовка
- Преимущества методики
- Недостатки методики
- Как часто следует проводить исследование
В каких случаях назначают ПЭТ-КТ
ПЭТ-КТ — методика визуализации преимущественно раковых опухолей. Поскольку они отличаются повышенной потребностью в питании. Если говорить о показаниях более подробно, методика требуется в рамках:
- Дифференциальной диагностики злокачественных и доброкачественных опухолей. Первые копят специальный контрастирующий препарат. Вторые — нет или в минимальной, ничтожной степени.
- Оценка стадии злокачественного процесса. Определение фазы онкологического заболевания.
- Изучение характера опухоли, степени ее агрессивности по скорости обмена веществ.
- Планирование биопсии. В рамках позитронно-эмиссионной томографии врачи ищут наиболее активную область опухоли, где клетки претерпели наибольшее изменение, и их плотность физически выше.
- Мониторинг состояния после пройденного лечения. ПЭТ-КТ могут проходить раз в год или реже. В зависимости от того, какой был рак, насколько агрессивный, радикальное ли лечение получил пациент. ПЭТ нужен чтобы на ранних стадиях обнаружить рецидив онкологического процесса.
- Планирование хирургического лечение или лучевой терапии. Чтобы определить агрессивность неоплазии и проработать грамотную тактику борьбы с образованием. ПЭТ не помогает понять тип опухоли. Потому помимо требуется еще и гистологическое исследование образца.
- Поиск первичного очага при наличии метастазов.
ПЭТ-КТ универсальная методика диагностики и изучения деталей онкологических процессов. Но при низкой интенсивности обменных процессов в опухоли возможны опасные с точки зрения информативности погрешности и ошибки.

Противопоказания к исследованию
ПЭТ-КТ – исследование безопасное. Но ряд противопоказаний у него все же есть:
- Острые воспалительные процессы асептического характера. То есть не связанные с инфекционными агентами: поражениями грибками, вирусами или бактериями.
- Инфекционно-воспалительные процессы в острой и подострой фазах. Пока не наступило полного выздоровления. До тех пор, пока состояние полностью не нормализуется.
- Беременность, независимо от фазы. Исключая случаи, когда провести диагностику жизненно необходимо и других вариантов не остается.
- Психические расстройства в декомпенсированной фазе. Тяжелые психозы, алкогольный делирий, бредовый состояния. Пока человек не придет в себя.
- Период грудного вскармливания. Если пройти КТ жизненно необходимо, после процедуры мать отказываться от естественного вскармливания и переходит на специальные смеси.
- Общее тяжелое состояние человека.
- Диабет, как 1-го, так и 2-го типа.
- Тяжелые поражения печени или почек. Поскольку препарат будет выводиться непозволительно медленными темпами. Отсюда повышенный риск интоксикации всего организма.
Перед проведением ПЭТ-КТ следует проконсультироваться с врачом. На случай, если имеются противопоказания. Он взвесит все «за» и «против». Решит, стоит ли проводить позитронно-эмиссионную томографию несмотря на формальные основания этого не делать.

Суть диагностики методом ПЭТ-КТ
В основе ПЭТ-КТ лежат две технологии.
Первая, на которой зиждется ПЭТ — это качественная оценка метаболизма тканей. Раковый опухоли отличаются крайней «прожорливостью». Для роста и развития им требуется много веществ. Настолько много, что остальной организм остается в состоянии дефицита. Для определения таких ненасытных тканей используется вещество, которое универсально и нужно всем клеткам – глюкоза.
Чтобы зафиксировать интенсивность и степень накопления глюкозы в измененных клетках, ее маркируют специальным радиоактивным веществом. В значительной части случаев используются препараты радиоактивного фтора. Они отличаются большим периодом полураспада, без проблем транспортируются и хранятся. А с другой стороны, не вызывают токсического и радиоактивного поражения организма пациентов.
Препарат с такой маркировкой накапливается в измененных тканях, окрашивая наиболее агрессивные области. Врачи получают визуальное подтверждение, картинку. Результаты исследования дают возможность сделать выводы, какая опухоль имеет место.
Минус технологии — ПЭТ показывает только измененные ткани. Чтобы посмотреть, как опухоль соотносится с тканями здоровыми, применяют КТ. Картину компьютерной томографии накладывают на картину ПЭТ, получая единый снимок высокого качества.

Всегда ли этот метод на сто процентов информативен
К несчастью, даже такой высокочувствительный способ диагностики как ПЭТ-КТ не может быть на все сто информативным. Некоторые неоплазии обладают малой скоростью метаболизма:
- Раковые неоплазии щитовидки.
- Опухоли печени.
- Неоплазии почек.
- Раковые образования предстательной железы.
- Раковые опухоли костной ткани.
- Некоторые саркомы и лимфомы.
Недостаточная визуализация не означает, что проблемы нет. Требуются другие методы диагностики.
Ровно так же и окрашивание тканей не говорит о наличии рака. Старые поколения препаратов для контрастирования могут копиться и в здоровых тканях. Поэтому при расшифровке специалисты ориентируются на комплексную картину.

Нужна ли специальная подготовка
Подготовка простая:
- За сутки до исследования нужно снизить углеводную нагрузку. Углеводы исключают из рациона. Жевательная резинка также запрещена. В том числе с сахарозаменителем.
- За 8-10 часов нужно отказаться от пищи. Исследования проходят натощак. Воду пить разрешается.
- За сутки до процедуры стоит избегать интенсивной физической нагрузки.
Важно взять с собой заключения врачей и результаты иных диагностических мероприятий.
Преимущества методики
ПЭТ-КТ обладает несколькими весомыми плюсами:
- Комплексный характер, универсальность. Позитронно-эмиссионная и компьютерная томография позволяют исследовать любые органы.
- Высокая точность и информативность исследования.
- Возможность диагностики рака на ранних стадиях.
- Отсутствие боли и дискомфорта.
- Отсутствие необходимости госпитализации. Все проходит амбулаторно.
Есть и минусы.

Недостатки методики
Самый главный недостаток – это необходимость применения радиоактивных препаратов. Но при должном подходе есть возможность снизить лучевую нагрузку на организм.
Как часто следует проводить исследование
Частоту проведения исследования определяет врач, отталкиваясь от клинического случая. ПЭТ-КТ может проводиться как методика первичной диагностики, а также в рамках мониторинга патологического, онкологического процесса.
