1. Введение
Электроэнцефалографический мониторинг (ЭГГ-мониторинг) — сегодня это основной метод исследования, цель которого регистрация пароксизмального события с целью проведения дифференциального диагноза между эпилептическими и неэпилептическими состояниями, например, такими как парасомнии, синкопальные состояния, стереотипии и другие.
Широкое распространение метода ЭЭГ-мониторинга в первой половине 90-х гг. произвело буквально революционные изменения в диагностике эпилепсии, позволило распознавать сложные в клиническом отношении судорожные припадки. Стало ясно, что многие виды судорожных приступов не укладываются в классическую картину, описанную в медицинских учебниках, что привело к пересмотру взглядов на диагностику и тактику лечения пациентов.
Проведение ЭЭГ назначается для получения ответов на следующие вопросы:
- Какова природа судорожных приступов — эпилептическая или неэпилептическая? (какую болезнь лечить)
- Какая форма эпилепсии? (как правильно лечить, какие препараты)
- Какая локализация приступа? (постановка вопроса о целесообразности хирургического лечения при неэффективности медикаментозного)
- Как протекает лечение? (изменять, отменять препараты)
Прежде чем приступить к ответу на эти вопросы необходимо понять происхождение этого метода, а потом прийти к плодам, результатам многолетних исследований, которые в изобилии разрослись на этом мощном стволе.
2. Понятия, определяющие ВЭЭГ
2.1. ЭЭГ и эпилепсия
Основные понятия, которые можно выделить, разбирая понятие видео-ЭЭГ-мониторинг — ЭЭГ и эпилепсия.
Вспомним определение эпилепсии: эпилепсия является одним из распространенных хронических заболеваний головного мозга. Согласно определению, эпилепсия — это хроническое заболевание головного мозга, характеризующееся повторными непровоцируемыми приступами нарушения двигательных, чувствительных, вегетативных, мыслительных или психических функций, возникающих вследствие чрезмерных нейронных разрядов (ILAE, 1989).
Электроэнцефалография — метод исследования биоэлектрической активности головного мозга, основанный на определении разности электрических потенциалов, генерируемых нейронами в процессе их жизнедеятельности. Регистрирующие электроды располагают так чтобы на записи были представлены все основные отделы мозга. Получаемая запись — ЭЭГ — суммарная электрическая активность миллионов нейронов, представленной преимущественно потенциалами дендритов и тел нервных клеток: возбудительными и тормозными постсинаптическими потенциалами и частично — потенциалами дендритов и тел нервных клеток. То есть ЭЭГ — как бы визуализированный результат функциональной активности головного мозга.
Здесь наверное стоило бы уделить долю внимания анатомии нейрона и его физиологии.
Нейрон является главной клеткой центральной нервной системы. Формы нейронов чрезвычайно многообразны, но основные части неизменны у всех типов нейронов: тело и многочисленных разветвленных отростков. У каждого нейрона есть два типа отростков: аксон, по которому возбуждение передается от нейрона к другому нейрону, и многочисленные дендриты (от греч. дерево), на которых заканчиваются синапсами (от греч. контакт) аксоны от других нейронов. Нейрон проводит возбуждение только от дендрита к аксону.
Основным свойством нейрона является способность возбуждаться (генерировать электрический импульс) и передавать (проводить) это возбуждение к другим нейронам, мышечным, железистым и другим клеткам.
Нейроны разных отделов мозга выполняют очень разнообразную работу, и в соответствии с этим форма нейронов из разных частей головного мозга также многообразна.
Многолетние исследования в области нейрофизиологии привели к выводам, что следующие электрические события присущи нейронам и могут вносить в вклад в суммарную биоэлектрическую активность мозга (ЭЭГ): постсинаптические возбуждающие и тормозные потенциалы (ВПСП, ТПСП), и распространяющиеся потенциалы действия (ПД). ВПСП и ТПСП возникают либо в дендритах, либо на теле нейрона. ПД генерируются в зоне аксонного «холмика» и далее распространяются по аксону.
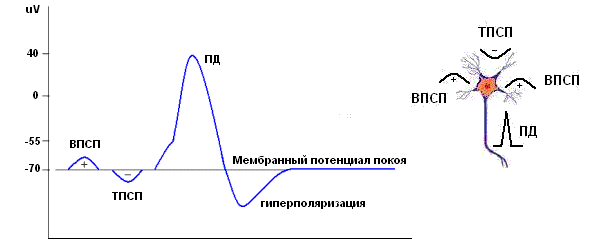
Нейрон. Возбуждающие и тормозные ПСП, потенциал действия.
Обычная спонтанная ЭЭГ, ее основные ритмы возникают в результате пространственной и временной суммации постсинаптических потенциалов (ПСП) большого количества корковых нейронов. Временные характеристики процесса суммации достаточны медленны по сравнению с длительностью ПД.
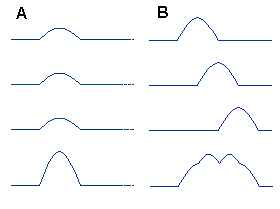 Определенная степень синхронизации задается различными подкорковыми структурами, которые выполняют роль «водителя ритма» или пейсмекера. Среди них наиболее значимую роль в генерации ритмов ЭЭГ играет таламус.
Определенная степень синхронизации задается различными подкорковыми структурами, которые выполняют роль «водителя ритма» или пейсмекера. Среди них наиболее значимую роль в генерации ритмов ЭЭГ играет таламус.
Потенциалы действия корковых нейронов не играют существенной роли в генерации основных ритмов ЭЭГ, поскольку являются очень короткими. Определяющая роль ПД в формировании паттернов ЭЭГ возникает в ситуациях, когда значительное количество нейронов синхронизируется и одновременно выдает пачки или «вспышки» ПД. Такой режим характерен для пароксизмальных событий, например, для эпилептических приступов и тогда морфология волн ЭЭГ в существенной степени определяется потенциалами действия. При этом острые компоненты ЭЭГ (спайки, острые волны) отражают не отдельные ПД, а скорее всю «пачку» потенциалов действия. Именно таким образом формируются многие эпилептиформные паттерны ЭЭГ, наиболее известным из которых является комплекс спайк-волна. Следует отметить, что подобная модель применима также в объяснении генеза физиологических острых компонентов ЭЭГ.
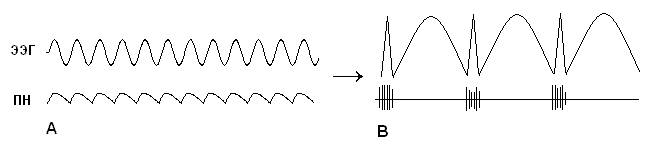
Таким образом, в генерации ЭЭГ принимают участие и постсинаптические потенциалы и потенциалы действия. Основная ритмика ЭЭГ определяется градуальными изменениями постсинаптических потенциалов благодаря пространственной и временной суммации отдельных ПСП в больших популяциях нейронов, которые относительно синхронизированы и находятся под воздействием подкоркового водителя ритма. Пароксизмальные же события, синхронизирующие значительное количество нейронов, которые продуцируют вспышки потенциалов действия, отвечают за формирование многих эпилептиформных феноменов ЭЭГ, в частности комплексов спайк-волна.
Собственно изучением всего этого процесса и занимается электроэнцефалография.
2.2. История изучения ЭЭГ
Начало изучению электрических процессов мозга было положено Д. Реймоном (Du Bois Reymond) в 1849 году, который показал, что мозг, также как нерв и мышца, обладает электрогенными свойствами.
Начало электроэнцефалографическим исследованиям положил В.В.Правдич-Неминский, опубликовав 1913 году первую электроэнцефалограмму записанную с мозга собаки. В своих исследованиях он использовал струнный гальванометр. Так же Правдич-Неминский вводит термин электроцереброграмма.
Первая запись ЭЭГ человека получена австрийским психиатром Гансом Бергером в 1928 году. Он же предложил запись биотоков мозга называть «электроэнцефалограмма».
По мере совершенствования компьютерной техники в 1996 году осуществлена методика амбулаторной полиграфической записи посредством 17-канального электроэнцефалографа (16 каналов ЭЭГ и 1 канал ЭКГ) с использованием переносного персонального компьютера (ноутбука) [Ebersole J. S. et al, 1996].
И наконец к концу 20 века у в арсенале эпилетологических и нейрофизиологических служб получается несколько видов методики ЭЭГ: рутинная ЭЭГ, холтеровское ЭЭГ и ВЭЭГ.
ЭЭГ стал «лезвием бритвы», наиболее качественным и информативным методом диагностики формы эпилепсии и позволяет регистрировать клинико-электроэнцефалографический коррелят эпилептического приступа, что дает возможность установить более точный диагноз и назначить рациональную схему антиэпилептической терапии.
3. Проведение ЭЭГ. Взгляд с 3 позиций
ЭЭГ мониторинг можно рассмотреть с 3 позиций: пациента, врача который проводит исследование в данный момент и со стороны врача, который расшифровывает видео-ЭЭГ-мониторинг постфактум.
Как предисловие стоит просто назвать показания и противопоказания к проведению этого исследования (Авакян)
Показания:
- Диагностика эпилепсий и эпилептических синдромов.
- Пароксизмальные состояния неясного генеза, вызывающие подозрение на наличие эпилепсии.
- Фармакорезистентные приступы (с целью выявления псевдоэпилептических пароксизмов или уточнения формы эпилепсии).
- Контроль эффективности лечения.
- Медикаментозная ремиссия (объективная констатация ремиссии).
- Подготовка к отмене антиконвульсантной терапии.
- Прехирургическое обследование.
- Субклиническая эпилептическая активность.
- Прогрессирующие когнитивные и поведенческие расстройства у детей.
- Первый судорожный приступ.
Противопоказания:
Противопоказаний к проведению ЭЭГ нет.
3.1. Устройство ВЭЭГ-лаборатории
Сутью метода ВЭЭГ является непрерывная запись ЭЭГ сигнала и видеоизображения пациента в течение длительного времени. Минимальная продолжительность исследования 15 минут, максимальная не лимитирована (до 7-14 суток). Обязательным условием является идеальная синхронизация видеоизображения и ЭЭГ во времени.
Основой системы ЭЭГ-мониторинга является многоканальный усилитель сигналов, имеющий возможность записи 19-32-64-128-канальной ЭЭГ, ЭКГ-канала, датчика дыхания, электромиографических и электроокулографических каналов.
К усилителю подключаются соответствующие регистрирующие датчики. Крепление ЭЭГ-электродов для длительной регистрации производится с помощью специальной шапочки или клеящей пасты. Конструкция электродной системы позволяет пациенту перемещаться по палате, не доставляет неудобств и делает проведение исследования комфортным.
Сигналы с усилителя посредством проводной или беспроводной связи направляются на рабочую компьютерную станцию.
Видеоизображение записывается посредством цифровых видеокамер, количество их может быть произвольным, в большинстве систем предусмотрена возможность использования 1-2 камер.
Обработка результатов производится изучением синхронного изображения ЭЭГ и видеоизображения, скорость прокрутки изображения выбирается произвольно. Программа обработки ЭЭГ включает возможности спектрального и когерентного анализа, программ трехмерной локализации диполя, и других вариантов компьютерного анализа.
Отделение видео-ЭЭГ-мониторинга должно включать в себя 3 основных звена:
- палата пациента, оборудованная видеокамерами, микрофоном, кнопкой пациента для регистрации событий;
- помещение для записывающих станций и персонала, осуществляющего слежение и контроль за пациентом.
- помещение для врачей (ординаторская), где располагаются станции просмотра и анализа записанных данных. Важным требованием к ВЭЭГ оборудованию является возможность просмотра и обработки ранее записанных исследований или текущего, не прерывая текущее исследование.
3.2. Схемы монтажа, подготовка пациента и начало исследования
Врач, проводящий исследование накладывает электроды либо встроенные в шапочку либо поочередно наклеивает каждый электрод соответственно своему месту. В обычной практике ЭЭГ-регистрирующие электроды располагают согласно международной системе «10-20».
В соответствии с системой «10–20» у испытуемого делают три измерения черепа:
- продольный размер черепа — измеряют расстояние по черепу между точкой перехода лобной кости в переносицу (назион) и затылочным бугром;
- поперечный размер черепа — измеряют расстояние по черепу через макушку (вертекс) между наружными слуховыми проходами обоих ушей;
- длину окружности головы, измеренной по этим же точкам.
Электроды, расположенные по средней линии, отмечаются индексом Z; отведения на левой половине головы имеют нечетные индексы, на правой — четные.
Отведения в системе «10–20»:
- фронтальные (F1, F2., F3 F4, Fz);
- лобные полюса (Fp1, Fp2);
- центральные (С1, С2, С3,С4, Сz);
- париетальные (Р1, Р2 Р3 Р4, Рz);
- темпоральные (T1, Т2, Т3, Т4, Т5, Тz);
- окципитальные (О1,О2, 0z).
Крепление и наложение электродов осуществляется в следующем порядке:
- Электроды подсоединяются к усилителю. Для этого штеккеры электродов вставляются в электродные гнезда усилителя.
- Ватным тампоном, смоченным в спирте обезжириваются места, предназначенные для постановки электродов.
- Непосредственно перед постановкой каждого электрода электродный гель наносится на контактирующую с кожным покровом поверхность. Необходимо помнить, что гель, применяемый в качестве проводника, должен быть предназначен для электродиагностики.
- На пациента надевается шлем/шапка со встроенными поверхностными электродами или каждый поврхностный электрод по отдельности с креплением его при помощи специального клея — коллодия. От практики игольчатых электродов ныне отходят согласно последним исследованиям ученых США и Великобритании. Места расположения электродов определяются соответственно системе расположения электродов. Необходимо помнить, что наложенные электроды не должны вызывать у пациента неприятные ощущения.
- Соответственно обозначениям, указанным на панели усилителя, устанавливаются электроды на предусмотренных системой местах, парные электроды располагаются симметрично.
После правильной установки и калибровки начинается само ВЭЭГ-исследование. В сегодняшней практике используются ВЭЭГ исследования длиной 4-5 часов (утренние/дневные/вечерние), длиной 9-10 часов (ночные), длиной 24 часа и более (холтеровские ВЭЭГ-мониторинги). Наиболее распространенными сегодня, являются короткие ВЭЭГ-исследования (60%), далее ночные — 36%, холтеровские — 4-5%
Премедикация перед исследованием, как правило, не проводится, поскольку введение препаратов, не входящих в схему лечения, может менять картину ЭЭГ, что не позволит оценить истинные параметры биоэлектрической активности мозга.
Не рекомендуется отмена или изменение схемы лечения в день исследования, что не позволит оценить эффекты терапии.
Принципиальное значение в диагностике эпилепсии имеет ЭЭГ сна. По мнению ведущих специалистов».. регистрация ЭЭГ в течение одной минуты поверхностного сна дает больше информации для диагностики эпилепсии, чем час исследования в состоянии бодрствования».
4. Понятия нормы и патологии в ВЭЭГ
4.1. Стандарты ВЭЭГ
Альфа ритм. Ритм частотой 8-13 Гц средней амплитуды 50 мкВ (15-100 мкВ), максимально выражен в задних (затылочных) отведениях при закрытых глазах. Возможно появление модуляций альфа ритма ( «веретен»), заключающихся в периодическом нарастании и снижении амплитуды волн. Выраженность альфа ритма зависит от многих условий, что необходимо учитывать при анализе ЭЭГ. Представленность альфа ритма на ЭЭГ и его регулярность уменьшаются при открывании глаз, записи в состоянии беспокойства, при активной умственной деятельности (решение задач), а также во время сна. У женщин во время менструации может быть увеличение его частоты. Установлено, что у здорового взрослого человека частота альфа ритма довольно стабильна и является генетически детерминированной.
Мю (роландический, аркообразный) ритм. Ритм аркообразной формы, частоты альфа (обычно, 8-10 Гц). По амплитуде не превышает альфа ритм (обычно, несколько ниже); регистрируется в центральных отделах у 20% здоровых взрослых. У детей данный ритм начинает хорошо определяться с 3-месячного возраста, лучше у девочек. Он не реагирует на открывание глаз, но блокируется с одной стороны при выполнении движений в контралатеральной конечности. Имеет малое диагностическое значение, даже при значительном его усилении или выраженной асимметрии.
Бета ритм. Ритм частотой более 13 Гц, средней амплитуды 10 мкВ; максимально выражен в передних отделах. Типичная частота бета ритма в норме составляет 18-25 Гц, менее распространен ритм частоты 14-17 Гц и крайне редко — свыше 30 Гц, У 70% здоровых людей амплитуда бета ритма не превышает 10 мкВ; и лишь у 3% — превышает 20мкВ. Бета ритм имеет максимальную выраженность в лобно-центральных отведениях. Бета активность несколько усиливается в период сонливости, при засыпании (I стадия сна), во время ФБС и иногда при пробуждении. В период глубокого сна (III, IV стадии фазы медленного сна) амплитуда и выраженность ее существенно снижаются.
Стойкое увеличение амплитуды бета активности свыше 25 мкВ, особенно с распространением её на задние отведения — признак патологии, однако, нозологически не специфичной. Традиционно усиление бета активности ( «excessive fast») связывалось с текущим эпилептическим процессом.
Тета ритм. Ритм частотой 4-7 Гц, по амплитуде, обычно превышающий основную активность фоновой записи. Встречается различной степени выраженности на ЭЭГ у всех здоровых детей. Тета активность начинает регистрироваться в центральных отделах уже с 3-недельного возраста, постепенно нарастая с возрастом и достигая максимума в 4-6 лет. В этом возрасте тета ритм является доминирующим на ЭЭГ у детей. Большинство исследователей считают, что у подростков и молодых взрослых при бодрствовании с закрытыми глазами низкоамплитудная тета активность (не превышающая амплитуды фона) частоты 6-7 Гц с бифронтальным преобладанием является нормальной, если она не превышает 35% фоновой записи.
4.2. Запись во сне
Сон является мощным активатором эпилептиформной активности. Неврологу, а тем более эпилептологу, важно уметь идентифицировать фазы и стадии сна. Известно, что эпилептиформная активность отмечается преимущественно в I и II стадии медленного сна, тогда как во время «дельта сна» и в периоде ФБС она чаще всего подавляется.
В настоящее время для дифференциации стадий сна применяется классификация Dement & Kleitman в модификаций Recbtshaffen & Kales (1968), Согласно этой классификации выделяются 2 фазы сна: фаза медленного сна (ФМС) и фаза быстрого сна (ФБС),
ФМС (в англоязычной литературе — non-REM sleep) развивается на фоне ослабления влияния активизирующей коры, восходящей ретикулярной формации и усиления активности синхронизирующих тормозящих структур.
В ФМС выделяют 4 стадии.
I стадия сна (дремота) характеризуется умеренным замедлением основной активности на ЭЭГ. Проявляется постепенным исчезновением альфа ритма и появлением ритмичной тета активности в центральной и лобно-центральной области, Может появляться периодическая ритмическая высокоамплитудная медленная активность частотой 4-6 Гц в лобных отведениях. Длительность I стадии сна у здорового человека составляет не более 10-15 минут.
II стадия сна (стадия «сонных веретен»). Наблюдаются следующие феномены. 1. Характерный признак II стадии сна — появление «сонных веретен» или сигма-ритма. Этот феномен представляет собой ритмические веретенообразно нарастающие и снижающиеся по амплитуде вспышки с частотой 12-16 Гц и амплитудой 20-40 мкВ, преимущественно в центрально-париетальных отделах. Длительность «сонных веретен» колеблется от 0 до 2 сек. Высокоамплитудные и продолжительные (около 3 сек) сонные веретена с преобладанием в лобных отведениях — обычно признак патологии.
III стадия сна характеризуется нарастанием амплитуды и количества медленных волн, преимущественно, дельта диапазона. Регистрируются К-комплексы и «сонные веретена». Дельта волны на эпохе анализа ЭЭГ занимают до 50% записи. Отмечается снижение индекса бета активности.
IV стадия сна характеризуется исчезновением «сонных веретен» и К-комплексов, появлением высокоамплитудных (не менее 50 мкВ} дельта волн, которые на эпохе анализа ЭЭГ составляют более 50% записи. III и IV стадии сна являются наиболее глубоким сном. Они объединены под общим названием «дельта сон».
В фазе быстрого сна (парадоксальный сон, REM-сон) отмечается ослабление влияния тормозящей ретикулярной формации и усиление десинхронизирующих активизирующих механизмов. При входе в ФБС нарастает бета активность. Данная фаза сна характеризуется появлением на ЭЭГ картины десинхронизации в виде нерегулярной активности с одиночными низкоамплитудными тета волнами, редкими группами замедленного альфа ритма и острыми «пилообразными» волнами. ФБС сопровождается быстрыми движениями глазных яблок и диффузным снижением мышечного тонуса. Именно в эту фазу сна у здоровых людей происходят сновидения. Начало сна с фазы быстрого сна или возникновение ее менее, чем через 15 минут после засыпания — признак патологии.
Нормальный сон взрослых и детей состоит из чередования серии циклов ФМС и ФБС. ФМС наиболее выражена в первую половину ночи и занимает 75% всего сна. Во второй половине ночи наиболее представлена ФБС (фаза сновидений), которая занимает около 25% ночного сна. Продолжительность одного цикла сна у детей младшего возраста составляет 45-55 минут; у взрослых 75-100 минут. За ночь у здорового человека возникает от 4 до 6 циклов сна.
4.3. Медленноволновая активность.
Медленноволновая активность. Этот термин включает в себя активность на ЭЭГ в форме замедления ритма по сравнению с возрастной нормой. Согласно международной классификации выделяют следующие варианты медленноволновой активности:
- замедление основной активности;
- периодическое замедление;
- продолженное замедление.
Замедление основной активности констатируется, когда основные ритмы имеют более медленные частотные характеристики по сравнению с возрастной нормой: в 1 год — частота менее 5Гц, в 4 года — менее 6 Гц, в 5 лет — менее 7Гц, в 8 лет и старше — менее 8 Гц.
Периодическое замедление. Периодическое замедление может быть нерегулярным и ритмическим, генерализованным и региональным. Выраженное периодическое ритмическое генерализованное замедление (обычно с преобладанием в лобных отведениях) иногда наблюдается при генерализованных формах эпилепсии. Нерегулярное региональное замедление (чаще в височных отведениях) может быть косвенным ЭЭГ признаком парциальной эпилепсии или локального органического поражения головного мозга.
Продолженное замедление констатируют в случае если данный паттерн занимает около 90% записи, и нет реакции на внешние стимулы. Всегда является патологическим признаком и свидетельствует об прогрессирующем очагово-деструктивном поражении мозга. В этом случае медленно-волновая активность отражает изменение коркового электрогенеза, вызванного анатомическим дефектом неирональных сетей. Она может сочетаться с нормальным или замедленным основным ритмом; возникает по одному из отведений (например, левому височному) или по всей гемисфере. Как правило, представлено тета (реже дельта) активностью низкой амплитуды, не реагирующей на экзогенные стимулы.
4.4. Провоцирующие пробы
Провоцирующие пробы. Фоновая запись биоэлектрической активности головного мозга осуществляется в состоянии пассивного бодрствования пациента с закрытыми глазами. С целью выявления нарушений ЭЭГ применяются провоцирующие пробы, Наиболее значимые из них следующие:
- Открывание-закрывание глаз.
- Гипервентиляция.
- Ритмическая фотостимуляция.
- Фоностимуляция.
- Депривация сна.
- Стимуляция умственной активности.
- Стимуляция мануальной активности.
Подробно остановимся на первых.
Проба на открывание-закрывание глаз служит для установления контакта с пациентом. При этом медицинский работник убеждается, что пациент находится в сознании и выполняет инструкции. Данная проба позволяет выявить реактивность альфа-ритма и других видов активности на открывание глаз. В норме при открывании глаза блокируется альфа ритм, нормальная и условно нормальная медленноволновая активность. Наоборот, отсугсгвие реакции паттернов на открывание глаз — как правило, признак патологической активности. Блокирование при открывании глаз затылочной пик-волновой активности у пациентов с доброкачественной затылочной эпилепсией Гасто является важным дифференциальным признаком с симптоматической затылочной эпилепсией. Следует помнить, что при некоторых формах фотосенситивной эпилепсии, эпилепти-формная активность на ЭЭГ возникает в момент закрывания глаз. Это может быть связано с исчезновением фиксации взора при закрытых глазах. Данный феномен был описан Panayiotopoulos (1998) и назван им «fixation off» или фотосенситивностью.
Гипервентиляция реально проводима у детей после 3-х лет. Продолжительность от 3 мин у детей до 5 мин у взрослых. Гипервентиляцию нельзя проводить в самом конце записи ЭЭГ, так как патологическая активность нередко появляется спустя некоторое время после окончания пробы. Основное назначение гипервентиляции — выявление генерализованной пик-волновой активности, а иногда и визуализация самого приступа (обычно абсанса). Реже появляется региональная эпилептиформная активность. Согласно наблюдениям Благо-склоновой Н.К. и Новиковой Л. А. (1994), появление пароксизмальных вспышек медленных волн при гипервентиляции свойственно здоровым детям и подросткам и является вариантом нормы. По мнению Daly & Pediey (1997), патологическая реакция на гипервентиляцию включает только появление на ЭЭГ пик-волновой активности или выраженной асимметрии паттернов. Принципиально важно, что любая другая реакция, в том числе и появление дельта активности, — индивидуальный вариант нормы. Таким образом, согласно современным воззрениям, оценка пароксизмальной генерализованной (нередко с бифронтальным преобладанием) ритмической тета-дельта активности при гипервентиляции как гипотетической «дисфункции мезо-диэнцефальных структур» несостоятельна. Подобная оценка нормальных, по своей сути, паттернов не имеет никакого значения для клиники, приводит к терминологической путанице и напрасному беспокойству, как врачей неврологов, так и самих пациентов.
Ритмическая фотостимуляция (РФС) является важнейшей пробой для выявления патологической активности при фотосенситивных формах эпилепсии. Используется классическая методика Jeavons & Harding (1975). Лампа стробоскопа должна находиться на расстоянии 30 см от закрытых глаз пациента. Необходимо использование широкого спектра частот, начиная от 1 вспышки в сек и, заканчивая частотой 50 Гц. Наиболее эффективна в выявлении эпилептиформной активности стандартная РФС с частотой 16 Гц. Возможны следующие реакции на РФС:
- Отсутствие очевидной реакции.
- Усвоение ритма: появление колебаний на ЭЭГ синхронно со вспышками при РФС.
- Фотомиоклонический ответ: при РФС возникает «трепетание» век и подергивание псриокулярной мускулатуры (миоклонический гиперкинез) синхронно со вспышками света. Это отражается на ЭЭГ отчетливым «ритмическим миографическим артефактом» в передних отведениях.
- Фотопароксизмалъный ответ: появление при РФС эпилептиформной активности, чаще возникают короткие разряды генерализованной быстрой (4 Гц и выше) полипик-волновой активности. По классификации фотосенситивных эпилепсии (Binnie и соавторы, 1992), выделяют форму фотосенситивной эпилепсии, при которой приступы возникают исключительно в лабораторных условиях во время РФС при ЭЭГ исследовании. Наиболее типично возникновение миоклонических пароксизмов, вовлекающих мышцы лица, плечевого пояса и рук, синхронно со вспышками света. В повседневной жизни приступы отсутствуют, даже при воздействии бытовых факторов РФС (мелькание света). Как правило, данная форма эпилепсии выявляется случайно при направлении больных на ЭЭГ исследование по причинам, не имеющим отношения к эпилепсии. Большинство авторов не рекомендуют назначение АЭП при этой форме, да и само отнесение таких случаев к эпилепсии вызывает сомнение. Фотопароксизмалъный ответ с высокой достоверностью коррелирует с наличием фотосенситивной эпилепсии.
4.5. Артефакты
Артефакты представляют собой любые графоэлементы на ЭЭГ, не являющиеся отражением электрической активности головного мозга. Подразделяются на механические и биоэлектрические. Механические артефакты бывают инструментальные, электродные и от электросети. Наиболее распространен артефакт вследствие «наводки» от сети переменного тока (отсутствие заземления, использование рядом различной медицинской аппаратуры) в виде появления синусоидальных колебаний частоты 50 Гц.
Биоэлектрические артефакты подразделяются на следующие:
- Миогенные артефакты. Наиболее частый вид артефактов. Регистрируются высокочастотные колебания миограммы, обычно преобладающие в височных отведениях. Они чаще вызваны напряжением жевательной мускулатуры, мимических мышц, мышц шеи. Артефакт от фасцикуляторного тремора напоминает аркообразный мю-ритм и наблюдается максимально в лобно-височных отведениях. Глоссокинетический артефакт возникает при ритмичных движениях языка, например, во время разговора или сосания (кормление младенцев во время ЭЭГ исследования).
- Сердечные и дыхательные артефакты. Электрод, находящийся на крупном сосуде, может вызывать артефакт, напоминающий графоэлемент реоэнцефалограммы. На ЭЭГ могут быть зарегистрированы электрокардиографические потенциалы, которые необходимо отличать от доброкачественных эпилептиформных нарушений детства. Данные потенциалы преобладают на электроэнцефалограмме при электроцеребральной инактивации (гибель мозга). Также встречаются артефакты, обусловленные экскурсией грудной клетки (часто во время проведения гипервентиляции).
- Окулографичесше артефакты. Связаны с активностью m. orbicularis oculi и регистрируются обычно в лобных отведениях. Возникают при ритмическом моргании (тикоидный гиперкинез), нистагме.
- Артефакты, вызванные изменением сопротивления кожи. Изменение сопротивления кожных покровов может быть обусловлено различными биохимическими процессами в организме. Наиболее часто данный тип артефактов возникает при волнении пациентов во время ЭЭГ исследования, что сопровождается выраженной потливостью.
При этом врач осуществляющий мониторинг должен уметь дифференцировать эти артефакты. Если, например, артефакт не уходит с течением времени, необходимо проверить электрод на полноценность соединения с усилителем, с пациентом и в случае необходимости заменить его/настроить.
5. Эпилептиформная активность
Эпилептиформная активность характеризуется появлением на ЭЭГ острых волн или пиков, которые резко отличаются от основной активности фона и возникают преимущественно у лиц, страдающих эпилепсией. Классификация нарушений ЭЭГ, принятая Американской ассоциацией нейрофизиологов [Daly & Pedley, 1997], придерживается строгой терминологии в обозначении патологических феноменов. В классификации общепринят термин «эпилептиформная активность», в связи с его исключительным применением к электроэнцефалографическим феноменам.
Согласно классификации нарушений ЭЭГ различают 9 межприступных (интериктальных) и два приступных (иктальных) эпилептиформных паттерна.
Межприступные эпилептиформные изменения:
- пики (спайки);
- острые волны;
- доброкачественные эпилептиформные нарушения детства (ДЭНД, «роландические» комплексы);
- комплексы пик-медленная волна;
- комплексы пик-медленная волна 3 Гц;
- медленные комплексы пик-медленная волна;
- множественные пики (полиспайки);
- гипсаритмия;
- фотопароксизмальный ответ (фотопароксизмальная реакция).
Иктальные эпилептиформные изменения:
- ЭЭГ приступа;
- ЭЭГ статуса.
Рассмотрим все указанные варианты эпилептиформных нарушений на ЭЭГ:
1. Пики (спайки) — эпилептиформный феномен, отличный от основной активности и имеющий пикообразную форму. Период пика составляет от 40 до 80 мсек. Это специфичный эпилептиформный паттерн, который наблюдается в рамках различных форм эпилепсии (генерализованных и парциальных). Одиночные пики встречаются исключительно редко; обычно они предшествуют появлению волн. Согласно базисным принципам электрофизиологии, появление спайков на ЭЭГ отражает процессы возбуждения корковых нейронов, а медленных волн — процессы торможения.
2. Острая волна — эпилептиформный феномен, отличный от основной активности, период которого составляет 80-200 мсек. Согласно данным ряда авторов [Eed-Oloffson, 1971; Gregori 1993], этот паттерн редко наблюдается у здоровых людей, и высоко специфичен в отношении эпилепсии. Острые волны, также как и пики, могут регистрироваться в виде региональных, мультирегиональных и генерализованных феноменов. Острая волна может встречаться, как изолированно (особенно, при парциальных формах эпилепсии), так и предшествуя медленной волне. Следует помнить, что острые волны, как и пики, могут представлять нормальные физиологические феномены: доброкачественные эпилептиформные транзиты сна (BETS), Wicket — потенциалы, 14 и 6 Гц позитивные спайки и некоторые другие.
3. Доброкачественные эпилептиформные нарушения детства (ДЭНД) — эпилептиформный феномен, который представлен в виде стереотипного электрического диполя, состоящего из острой волны, с последующей медленной волной. Амплитуда негативного полюса составляет 150-300 мкВ, — часто в 2 раза больше позитивного. Общий период комплекса составляет 80-120 мсек. Этот паттерн легко узнаваем, благодаря типичной морфологии, напоминающей зубцы QRST на ЭКГ [Мухин К. Ю. и соавт., 2001]. Для комплексов ДЭНД характерна тенденция к их группированию (дуплеты, триплеты и т.д.), а также усиление их представленности и амплитуды в фазу медленного сна. Доброкачественные эпилептиформные нарушения детства возникают, преимущественно, в возрасте от 3 до 14 лет и являются характерным паттерном при идиопатических парциальных формах эпилепсии. С наступлением пубертата их выраженность уменьшается, и они в большинстве случаев постепенно исчезают после 14-15 лет. Предполагается, что данный ЭЭГ паттерн является возраст-зависимым и генетически детерминированным с аутосомно-доминантным наследованием с низкой пенетрантностью и вариабельной экспрессивностью [Stephani, 2002].
4. Комплексы пик-медленная волна — представляют паттерн, состоящий из пика и следующей за ним медленной волны. Наиболее часто комплексы пик-медленная волна регистрируются в виде генерализованных разрядов, представленность и амплитуда которых усиливается в ФМС, при ГВ и РФС. Данная ЭЭГ картина высоко специфична для идиопатических генерализованных форм эпилепсии детского и юношеского возраста. Однако по данным Doose & Baier (1987), в 10-17% случаев генерализованные комплексы пик-медленная волна могут быть обнаружены у клинически здоровых лиц, в основном, у родственников пробандов с абсансными формами эпилепсии.
В виде единичных паттернов комплексы пик-медленная (или острая-медленная) волна встречаются при криптогенных и симптоматических формах парциальной эпилепсии.
5. Комплексы пик-медленная волна с частотой 3 Гц — представляют регулярный разряд генерализованных паттернов, состоящих из единичных спайков со следующей медленной волной с частотой от 2,5 до 3,5 Гц. Согласно классификации нарушений ЭЭГ, для отнесения паттернов в данную группу, продолжительность этих комплексов должна составлять более 3 секунд. Частота комплексов во время разряда непостоянна. В начале разряда она составляет 3-4 Гц, тогда как к финалу снижается до 2,5-2,25 Гц. Характерно амплитудное преобладание паттернов в лобных отведениях. Медленный сон вызывает активацию пик-волновых комплексов. При этом продолжительность разрядов во время сна укорачивается и одновременно возможно некоторое замедление частоты комплексов. Данный ЭЭГ паттерн характерен для абсансных форм эпилепсии, особенно — детской абсанс эпилепсии. Продолжительность разряда пик-волновых комплексов более 3 сек с высокой вероятностью является иктальным феноменом типичных абсансов.
6. Медленные комплексы пик-медленная волна — представляют собой нерегулярные разряды комплексов пик (а чаще — острая волна)-медленная волна, частотой менее 2,5 Гц. Согласно классификации нарушений ЭЭГ, продолжительность этих комплексов должна составлять более 3 секунд. Комплексы состоят из би- и трифазных негативных острых волн с периодом 150-200 мсек. и следующих за ними высокоамплитудных (300-400 мкВ) негативных медленных волн. Они билатерально-синхронны, однако, в ряде случаев возможна их амплитудная асимметрия и начальная асинхрония. Характерная особенность этого паттерна — тенденция к усилению выраженности изменений во время ФМС.
7. Полипики (множественные пики) — определяются как группа генерализованных билатерально-синхронных, следующих друг за другом 3-х и более пиков частоты от 10 Гц и выше. Каждая группа полипиков может завершаться медленной волной (полипик-волновые комплексы). Генерализованные полипики являются специфичным паттерном для миоклонических форм эпилепсии, таких как юношеская миоклоническая эпилепсия, доброкачественная миоклоническая эпилепсия младенчества. Однако этот паттерн может встречаться и при парциальных формах эпилепсии, у больных синдромом Леннокса-Гасто, а также в случаях прогрессирующих эпилепсии с миоклонусом (болезни Лафора, Унферрихта-Лундборга и др.).
8. Гипсаритмия — эпилептиформный паттерн, характеризующийся нерегулярной диффузной продолженной высокоамплитудной (>300 мкВ) медленноволновой активностью (1-3 Гц), на фоне которой регистрируются мультирегиональные пики и острые волны. В отдельных случаях возможно преходящее кратковременное уплощение этой активности (вплоть до биоэлектрического молчания). Данный вариант гипсаритмии Ohtahara (1978) назвал паттерном вспышка-угнетение. В некоторых случаях (симптоматический вариант синдрома Веста) гипсаритмия существенно доминирует в одной из гемисфер, сочетаясь со стойкими региональными спайками в этой зоне. Сон существенно модифицирует гипсаритмию: во время ФМС амплитуда и представленность эпилептиформных изменений увеличивается и становится периодической, тогда как в быстром сне она уменьшается или исчезает полностью.
9. Фотопароксизмальный ответ. Характеризуется появлением эпилептиформной активности, как генерализованного характера, так и регионального (преимущественно, в затылочных отделах коры головного мозга), которая появляется при предъявлении ритмической фотостимуляции различной частоты. Максимальный ответ наблюдается при частоте РФС около 16 Гц при закрытых глазах. Лучше выявляется при референтном монтаже. Фотопароксизмальный ответ может продолжаться и после окончания световой стимуляции, что характерно для фотосенситивных форм эпилепсии: первичная фотосенситивная эпилепсия, идиопатическая фотосенситивная затылочная эпилепсия, болезнь Унферрихта-Лундборга и некоторые другие.
10. Иктальные ЭЭГ паттерны. ЭЭГ приступа — внезапное изменение биоэлектрической активности, регионального или диффузного характера, ассоциированное с эпилептическим приступом. Во многих случаях для дифференциальной диагностики иктальных и межприступных эпилептиформных нарушений на ЭЭГ единственным методом является видео-ЭЭГ-мониторинг. Однако кратковременность возникновения некоторых паттернов (например, разрядов генерализованных пик-волновых комплексов, продолжительностью 1-2 сек) не всегда позволяет точно зафиксировать наличие приступа, синхронно с ним. В этих случаях ряд авторов рекомендует употреблять термин «субклинические эпилептиформные нарушения на ЭЭГ» [Binnie, 1993]. ЭЭГ паттерн приступа может возникать как генерализованно, так и регионально. Это высокоспецифичный феномен для эпилепсии, даже если он возникает без клинических симптомов. При наличии в клинике пароксизмов неясной этиологии этот паттерн доказывает эпилептическую их природу.
11. ЭЭГ статуса определяется в случае продолженных эпилептиформных паттернов ЭЭГ приступа или часто повторяющихся паттернов ЭЭГ приступа без восстановления нормального ритма фоновой записи между ними. Следует отметить, что ЭЭГ статуса может не коррелировать с клиническими симптомами эпилептического статуса. Классический тому пример — электрический эпилептический статус медленного сна; тяжелая форма эпилепсии с выраженными когнитивными нарушениями, при которой частота и выраженность эпилептических приступов может быть минимальна или приступы отсутствуют вовсе. Таким образом, даже высоко специфичные паттерны ЭЭГ приступа и ЭЭГ статуса, следует рассматривать только в контексте с клиническими данными. Особенности иктальной ЭЭГ при различных типах эпилептических приступов в рамках отдельных форм эпилепсии будут рассмотрены в следующих главах.
6. Расшифровка и заключение ЭЭГ
Таким образом мы подошли к интерпретации ЭЭГ-нарушений
Эти рекомендации не являются строгими правилами. Они относятся в первую очередь к стандартной ЭЭГ. При описании более специализированных записей (неонатальные записи, электроцеребральное молчание) представление технических деталей должно быть более полным — в соответствии со стандартами ACNS (1 — «Minimum Technical Requirements (MTR) for Performing Clinical EEG»; 2 — «Minimal Technical Standards for Pediatric Electroencephalography»; 3 — «Minimum Technical Standards for EEG Recording in Suspected Cerebral Death»).
Отчет ВЭЭГ должен состоять из 3 основных частей:
- введение,
- описание,
- интерпретация, включая
- впечатление (мнение) касательно нормальности или степени аномальности,
- корреляцию данных ЭЭГ с клинической картиной.
1. Введение.
Введение должно начинаться с описания специальной подготовки, если таковая предпринималась перед записью.
2. Описание.
Описание ЭЭГ должно включать все характеристики записи, включая нормальные и аномальные, представленные объективным способом, максимально избегая утверждений об их значимости.
Целью является полный и объективный отчет, который позволит другим ЭЭГ-специалистам придти к выводу касательно нормальности или степени аномальности записи по описанию — без необходимости просматривать исходную ЭЭГ. Этот вывод может отличаться от исходного вывода, поскольку в определенной мере субъективен.
Описание начинается с фоновой активности, доминирующей активности, ее частоты, количества (постоянная, преходящая), локализации, амплитуды, симметрии или асимметрии, является ли она ритмической или иррегулярной. Частота должна указывать в Гц или циклах в секунду. В целях стандартизации отчета рекомендуется определять амплитуду в отведениях, включающих смежные электроды по схеме 10-20. Желательно, но не обязательно, оценивать амплитуду в микровольтах. Это позволит избежать таких терминов, как «низкий», «средний» и «высокий». Недоминирующая активность — частота, количество, амплитуда, локализация, симметрия или асимметрия, ритмичность или ее недостаточность, должна описываться с использованием таких же единиц измерения, как и для доминантной активности.
Если проводились тесты — должны быть описаны реакции на открытие и закрытие глаз, а также произвольных, целенаправленных движений. Включается описание указания на симметрию или асимметрию, полноту или неполноту, устойчивость или неустойчивость.
Аномальные записи, неонатальные записи, или записи только во время сна, могут не содержать четкого доминирующего ритма. В таких случаях, должны быть описаны другие виды активности (амплитуда, частота, и пр.) в любом порядке. Если запись демонстрирует заметную межполушарную асимметрию, характеристики по каждому полушарию должны быть представлены по отдельности (доминантная, недоминантная активность).
Вслед за фоновой активностью должно идти описание нарушений, не относящихся к фоновой активности. В описание включаются: тип нарушения (спайки, острые волны, медленные волны), распространенность (диффузные, локальные), топография или локализация, симметрия, синхронность (внутри— и межполушарная), амплитуда, временные характеристики (непрерывная, периодическая, эпизодическая, или пароксизмальная) и количество аномальных паттернов. Количество нарушений описывается субъективным способом, поскольку в клинической ЭЭГ невозможно точно измерить количество или соотношение.
Если аномалия является эпизодической, необходимо обратить внимание на отсутствие или наличие периодичности между эпизодами, ритмичность или иррегулярность паттерна внутри каждого эпизода. Необходимо представить временной диапазон продолжительности эпизодов.
В описании процедур активации необходимо включать утверждение об их качестве (например, хорошая, удовлетворительная или плохая гипервентиляция, длительность сна, стадии сна, которые были достигнуты во время исследования). Надо указать тип (глиссандо, пошаговая) фотостимуляции и диапазон частот стимуляции. Описываются эффекты гипервентиляции и фотостимуляции, включая нормальные и аномальные ответы. Если гипервентиляция или фотостимуляция не проводились, необходимо указать причину. Поскольку направляющий врач предполагает, что эти процедуры используются по умолчанию, он может ожидать описания их результатов — даже в том случае, если необходимость их проведения не была указана явно в направлении.
Нет нужды указывать на отсутствие определенных характеристик, за исключением нормальных, — таких как низкоамплитудная быстрая активность, сонные веретена, и др. Такие фразы как «отсутствие фокальной патологии» или «нет эпилептиформных нарушений» могут использоваться только в разделе интерпретации — при наличии явного или предполагаемого запроса направляющего доктора. Они не должны использоваться в описательной части.
Артефакты должны описываться только в сомнительных случаях (например, сохраняется вероятность того, что они отражают церебральную активность) или, когда они носят необычный характер, мешают интерпретации записи, а также когда они обладают определенной диагностической ценностью (например, миокимии, нистагм, и др.).
3. Интерпретация.
(I) Впечатление — это субъективное мнение специалиста о степени нормальности записи. Описание записи предназначено, в первую очередь, для электроэнцефалографиста, который использует его для последующего вывода, или другого эксперта, и должно быть детальным и объективным. Впечатление, с другой стороны, пишется в первую очередь для направляющего врача, и, следовательно, должно быть по возможности сжатым. Большинство клиницистов из предшествующего опыта предполагают, что чтение детального описания не дает им существенно новой информации, и поэтому ограничиваются интерпретаций. Если оно слишком большое и выглядит иррелевантно клинической картине, клиницист может потерять интерес, что в итоге приводит в снижению пользы от всего ЭЭГ отчета. Если запись считается аномальной, желательно указывать ее степень — с целью облегчить сравнение между повторными исследованиями. Поскольку эта часть отчета носит довольно субъективный характер, степень нарушений может варьировать от лаборатории к лаборатории. Однако в каждой лаборатории следует четко определять критерии степени нарушения и строго следовать им.
После определения степени нарушений, необходимо указать причины, на основе которых строится вывод. Если присутствуют несколько видов нарушений, желательно ограничиться списком из двух или трех главных нарушений, которые наиболее характерны для данной записи. Если перечислять все нарушения, наиболее существенные «растворяются» в тексте и теряется значимость выводов. При наличии данных предыдущих ЭЭГ записей, необходимо включать их сравнение с результатами данного исследования.
(II) Клиническая корреляция — это попытка показать насколько данные ЭЭГ укладываются (или нет) в общую клиническую картину. Оно может варьировать — в зависимости от того, кому оно адресуется. Для адресата, далекого от неврологии или ЭЭГ, оно должно быть более тщательным и выверенным.
Если ЭЭГ аномальная — это указывает на церебральную дисфункцию, поскольку ЭЭГ является отражением церебральной функции. Тем не менее, фраза «церебральная дисфункция» может звучать излишне угрожающе и должна использоваться только когда нарушение квалифицируется как «более чем легкое» и когда имеется достаточно клинической информации, чтобы считать такой вывод реалистичным в данном клиническом контексте. В остальных случаях допустимы предложения типа «Запись указывает на легкую иррегулярность церебральной функции». Определенные паттерны ЭЭГ являются подтверждающими для более или менее специфических клинических ситуаций; дельта фокус может говорить о структурном поражении в соответствующем клиническом контексте; определенные типы спайков или острых волн подтверждают потенциальный эпилептогенез. Если нарушение ЭЭГ соответствует клинической информации, которая содержит диагноз или подозрение на наличие подобного состояния, можно указать, что данные ЭЭГ согласуются или подтверждают диагноз.
Цифровые способы записи, генерации и передачи отчета позволяют, при необходимости, включать в отчет короткие отрезки реальной записи, в том числе с примерами нарушений.
7. ВЭЭГ-мониторинг в оценке эффективности противосудорожной терапии
Одним из основных критериев объективизации действия противоэпилептических препаратов является изменение биоэлектрической активности мозга, регистрируемое с помощью ЭЭГ.
Эти изменения носят различный характер и зависят от формы эпилепсии и применяемой терапии.
Помимо воздействия антиконвульсантов на эпилептическую активность, они также оказывают влияние на характер фоновой ритмической активности. Хорошо описаны изменения фоновой ритмики, появляющиеся при длительном приеме бензодиазепинов и барбитуратов.
При прогрессирующем течении заболевания отмечается нарастание индекса эпилептической активности в очаге.
Другим маркером отрицательной динамики является появление дополнительных очагов эпилептической активности. Они могут быть зависимы от первичного очага или существовать независимо.
К характеристикам проградиентного течения заболевания относится появление феномена вторичной билатеральной синхронизации (ВБС).
К ЭЭГ-критериям, отражающим положительное влияние ПЭП, относятся: снижение индекса пароксизмальности в очаге, уменьшение количества эпилептических очагов и регресс эффекта ВБС.
Динамические ВЭЭГ-исследования в период отмены терапии с высокой точностью позволяют оценить риск возобновления приступов.
8. Эффективность ЭЭГ-мониторинга
Была проанализирована достоверность направляющего диагноза «Эпилепсия» у первичных пациентов, поступающих в эпилептологический стационар (НПЦ медицинской помощи детям, ДЗ Москвы).
Исследуемая группа составила 1154 пациента в возрасте от 0 до 18 лет. Всем пациентам проводились следующие методы обследования: оценка нервно-психического статуса, видео-ЭЭГ-мониторинг продолжительностью 6 и более часов, и, в большинстве случаев, МРТ головного мозга.
Результаты: Диагноз «эпилепсия» был достоверно подтвержден у 643 пациентов (56%); у 240 (20,8%) пациентов не было получено электроэнцефалографических паттернов эпилепсии, но диагноз оставлен в прежнем виде с учетом данных анамнеза и других методов обследования; у 133 пациентов (11,5%) диагноз «эпилепсия» был снят; у 46 (4%) пациентов диагностированы парасомнии; у 39 (3,4%) — псевдоэпилептические (психогенные) приступы; у 8 (0.7%) — тики; в группу пациентов из 45 (3,9%) человек вошли дети с аффект-респираторными пароксизмами, синдромом Туретта, синкопальными состояниями, хореоатетозом/дистонией, мигренью, аутизмом, синдромом Мюнхаузена, мастурбацией.
Таким образом, у 23,2% (267) пациентов диагноз «эпилепсия» был исключен. Наиболее частыми пароксизмальными состояниями, мимикрирующими эпилепсию являлись парасомнии и психогенные приступы. Нельзя также забывать о большой группе (11,5% — 133 пациента) абсолютно здоровых детей, ошибочная постановка диагноза «эпилепсия» у которых, в большинстве случаев, была связана с неверной трактовкой поведенческих реакций, характерных для того или иного возраста. В подавляющем большинстве этих случаев причины гипердиагностики эпилепсии заключались в недостаточно полном и точном сборе анамнеза, неправильной трактовке результатов ЭЭГ, а в ряде случаев в психологическом давлении родственников пациента на врача.
9. Заключение
Успешное лечение эпилепсии напрямую зависит от своевременно и правильно установленного диагноза. Использование неинформативных методов диагностики на стартовом этапе лечения эпилепсии приводит к трудностям в подборе адекватной терапии, прогрессированию заболевания. В ЭЭГ это проявляется в виде появления множественных вторичных очагов эпилептической активности, развитию феномена вторичной билатеральной синхронизации при фокальных формах и значительному нарастанию индекса генерализованных разрядов при генерализованных формах эпилепсии.
Нередко наличие у пациента эпилептических приступов, несмотря на их очевидную курабельность, побуждает врача необоснованно вводить социальные ограничения, применять полипрагмазию в лечении.
С другой стороны, необоснованная констатация ремиссии у пациентов с эпилепсией также имеет неблагоприятные для пациента последствия, поскольку сохраняются клинически «невидимые» виды приступов или эпилептиформная активность на ЭЭГ.
Отсутствие изменений в записанном фрагменте ЭЭГ бодрствования длительностью до 30 мин (рекомендации ILAE) может создать ложное впечатление о положительной динамике на фоне лечения. Опираясь на полученные данные, врач может ошибочно констатировать клинико-энцефалографическую ремиссию. С другой стороны, выявление эпилептической активности на контрольной динамической ЭЭГ на фоне подобранной терапии может содержать фрагмент эпилептической активности, которую врач ошибочно трактует как «отрицательную динамику». В некоторых случаях на коротких фрагментах записи ЭЭГ-характеристики могут выглядеть как «нормальные» при сохраняющихся приступах. При этом объективный анализ продолженной записи свидетельствует, что характер биоэлектрической активности у пациента значимо не менялся. Ошибки при интерпретации связаны с чередованием нормальных и патологических фрагментов ЭЭГ.
Можно утверждать, что объективная трактовка изменений ЭЭГ может проводиться только при проведении ВЭЭГ-мониторинга.
Введение в алгоритм диагностики и динамического обследования ВЭЭГ-мониторинга позволяет, используя объективные клинико-нейрофизиологические критерии, своевременно диагностировать заболевание, оценивать состояние больного на разных этапах лечения, оптимизировать терапевтическую тактику и избегать диагностических ошибок у пациентов с эпилепсиями и эпилептическими синдромами.
Анализ длительного катамнеза больных эпилепсией (взрослых и детей) позволил разработать и внедрить в специализированных отделениях и кабинетах высокодостоверный комплексный клинико-нейрофизиологический подход к дифференциальной диагностике эпилепсий и судорожных синдромов, значительно повысить качество проводимой терапии в этой сложной группе пациентов.
Врач-педиатр, врач высшей категории,
невролог Тамбиев И. Е..
Ковалев И. Г.
Около 30 % пациентов, поступающих в эпилептологические центры с диагнозом «эпилепсия», в реальности не болеют эпилепсией – эти данные получены в ведущих мировых клиниках. Формула, приводящая к диагностическим ошибкам, чаще всего выглядит так:
Неспецифические симптомы + нормальная ЭЭГ, расцененная, как патологическая = ошибочный диагноз «эпилепсия»
Последствием этого является ненужное и опасное лечение, которое пациент получает долгие годы, причем повторные нормальные ЭЭГ не отменяют диагноз. «ЭЭГ как биопсия, а диагноз эпилепсия как рак», — такие сравнения приводятся врачами: будучи однажды поставленными, подобные диагнозы уже не снимаются. Только повторный пересмотр первой ЭЭГ, по которой был выставлен диагноз, может выявить ошибку, а в остальных случаях пациент будет нести за собой диагноз «эпилепсия» всю жизнь, он будет долгие годы принимать препараты, имеющие значительные побочные эффекты, страдать от социальной стигмы и ограничений, которые накладывает диагноз эпилепсия. Человек не сможет водить машину, для него будут закрыты некоторые виды работ и должностей.
Врачи-эпилептологи всего мира сходятся в одном (и надо отметить, что это, пожалуй, единственное, в чем они действительно согласны!): лучше поставить диагноз эпилепсии позже, чем поставить его «профилактически».
В чем же причина подобной гипердиагностики, если, по данным большинства исследований, только 1-2 % ЭЭГ могут быть расценены как ложноположительные? По мнению специалистов, первая причина в «человеческом факторе»: в отсутствие должного уровня знаний и опыта. Зачастую неверный диагноз бывает поставлен по одной единственной ЭЭГ, на которой известные доброкачественные эпилептиформные паттерны и варианты нормальной ЭЭГ были расценены как патологические. К таким паттернам относятся: микроспайки, ритмическая тета-активность в височных отведениях, возникающая при дремоте, 14 и 6 Гц позитивные острые волны, 6 Гц фантомные спайк-волны, ритмическая дельта-активность при гипервентиляции и т.д. Большинство этих паттернов были описаны еще в пятидесятых годах XX века, и их выявление не представляет трудности для специалистов, работающих с ЭЭГ.
Однако, на практике данные паттерны встречаются достаточно редко, в подавляющем большинстве случаев ошибочно интерпретируются артефакты, брешь-ритм (breach-rhythm), или «безымянные варианты», которые являются вариациями нормальной ритмики, в результате чего возникают колебания заостренной конфигурации или фрагменты альфа-активности, которые не вписываются в легко узнаваемые ЭЭГ-феномены. Эти безымянные колебания нормального фона были описаны под разными названиями и их можно найти в большинстве ЭЭГ. Дифференцировать нормальные варианты из значимых спайков и острых волн иногда бывает сложно, но существуют определенные рекомендации, которым надо следовать. Избежать этих ошибок могут только обученные опытные врачи эпилептологи/нейрофизиологи, в противном случае пишутся расплывчатые трактовки и нормальная ЭЭГ описывается как патологическая. Здесь складывается ситуация, типичная для человеческой психики: чем меньше знания и опыт, тем с большим вниманием человек относится к незначительным изменениям на ЭЭГ (что в зарубежной литературе называется «Overriding EEG» и «Looking too hard syndrome»). «Снисходительность приходит с опытом», как и понимание того, насколько вариабельна норма на ЭЭГ. Точно так же, как терапевт найдет больше изменений на ЭКГ, чем кардиолог, так же и неопытный врач нейрофизиолог скорее опишет больше патологической активности на ЭЭГ, чем опытный эпилептолог.
Как мы можем исправить существующее положение вещей и уменьшить частоту ошибок, связанных с анализом ЭЭГ?
Здесь необходимо отметить, что в Америке и странах Европы чтением ЭЭГ занимаются неврологи, которые обучаются этому в рамках прохождения резидентуры (аналог российской ординатуры, только длительностью 4-7 лет). В связи с этим, за рубежом проблема неверного анализа ЭЭГ связывается с низким уровнем знаний врачей об ЭЭГ и умением ее интерпретировать. С учетом данной особенности, одно из предложений зарубежных коллег — оценка ЭЭГ не неврологом, а опытным нейрофизиологом. В России ЭЭГ в большинстве клиник описывается специалистами функциональной диагностики, которые в части случаев вообще имеют не медицинское образование, тогда как врач невролог зачастую не знаком даже с основами ЭЭГ. И, надо сказать, данный путь также порочен: процент диагностических ошибок в нашей стране не меньше, если не больше, так как в этом случае отсутствует интерпретация ЭЭГ в контексте клинических данных.
Неверный анализ ЭЭГ врачом-неврологом за рубежом и отсутствие анализа результатов ЭЭГ с позиции клиники — обе ситуации одинаково плохи.
Наверное, наиболее оптимальным вариантом является другое решение, которое также обсуждено в статье Benbadis S.R.:
так как в повседневной практике невролог и психиатр сталкивается с пароксизмальными состояниями и, в частности, с эпилепсией достаточно часто, то трудно представить, чтобы врач не умел читать ЭЭГ и не умел анализировать данные, с которыми работает. Но если мы считаем, что описание ЭЭГ — прерогатива врачей, то система обучения должна быть в корне изменена. ЭЭГ в рамках последипломной подготовки неврологов и психиатров должно уделяться больше времени и внимания. Нужен курс, обучающий врачей анализу ЭЭГ, затем должна быть практика под руководством опытных специалистов, а после — возможность в ходе самостоятельной работы обращаться к специалисту для разбора сложных случаев.
По мнению авторов, к описанию ЭЭГ должна быть применена система, используемая при описании ЭКГ или рентгенографии грудной клетки. Они могут быть оценены экстренно врачами скорой помощи, терапевтами, реаниматологами, но затем должны быть повторно проанализированы специалистами — кардиологами или рентгенологами, для того, чтобы избежать ошибок и неверных диагнозов.
Другой важный методологический прием — первичный анализ ЭЭГ «вслепую», то есть без клинических данных о пациенте (при этом, безусловно, клиническая трактовка в последующем дается с учетом всей информации о заболевании. Так предлагают описывать ЭЭГ многие ведущие эпилептологи мира, чтобы избежать синдрома «слишком тщательного анализа» (“looking too hard” syndrome).
Улучшить ситуацию может:
1. улучшение качества анализа ЭЭГ путем более высокого уровня обучения неврологов и психиатров а, главное, введением контроля уровня знаний
2. обучение «консервативному» чтению ЭЭГ, при котором должна быть описана только четкая эпилептиформная активность, а сомнительные вопросы должны решаться в пользу нормы или дообследования с изменением дизайна исследования
3. обязательная клиническая интерпретация ЭЭГ-данных в тех случаях, когда это возможно
4. создание более четких рекомендаций и руководств по описанию ЭЭГ
5. повторная оценка ЭЭГ специалистом-нейрофизиологом или эпилептологом.
Итак, вернемся к формуле:
Неспецифические симптомы + неверно интерпретированная нормальная ЭЭГ = ошибочный диагноз «эпилепсия»
Надо понимать, что четкая клиническая картина приступов при нормальной ЭЭГ скорее подтверждает диагноз эпилепсии, чем неспецифические симптомы и острые волны на ЭЭГ. Неспецифические симптомы и неубедительная патологическая активность на ЭЭГ (как например, «заостренные двухфазные потенциалы» или «ирритативные знаки») ни в коем случае не должны приводить к диагнозу «эпилепсия».
Материал подготовлен Фоминых В.В., Гриненко О.А., Троицким А.А. на основе следующих статей:
1. Benbadis SR. «Just like EKGs!» Should EEGs undergo a confirmatory interpretation by a clinical neurophysiologist? Neurology. 2013;80(1 Suppl 1):S47-51.
2. Benbadis SR. Errors in EEGs and the misdiagnosis of epilepsy: importance, causes, consequences, and proposed remedies. Epilepsy Behav. 2007;11(3):257-62.
3. Markand ON. Pearls, perils, and pitfalls in the use of the electroencephalogram. Semin Neurol. 2003;23(1):7-46.
Около 30 % пациентов, поступающих в эпилептологические центры с диагнозом «эпилепсия», в реальности не болеют эпилепсией – эти данные получены в ведущих мировых клиниках. Формула, приводящая к диагностическим ошибкам, чаще всего выглядит так:
Неспецифические симптомы + нормальная ЭЭГ, расцененная, как патологическая = ошибочный диагноз «эпилепсия»
Последствием этого является ненужное и опасное лечение, которое пациент получает долгие годы, причем повторные нормальные ЭЭГ не отменяют диагноз. «ЭЭГ как биопсия, а диагноз эпилепсия как рак», — такие сравнения приводятся врачами: будучи однажды поставленными, подобные диагнозы уже не снимаются. Только повторный пересмотр первой ЭЭГ, по которой был выставлен диагноз, может выявить ошибку, а в остальных случаях пациент будет нести за собой диагноз «эпилепсия» всю жизнь, он будет долгие годы принимать препараты, имеющие значительные побочные эффекты, страдать от социальной стигмы и ограничений, которые накладывает диагноз эпилепсия. Человек не сможет водить машину, для него будут закрыты некоторые виды работ и должностей.
Врачи-эпилептологи всего мира сходятся в одном (и надо отметить, что это, пожалуй, единственное, в чем они действительно согласны!): лучше поставить диагноз эпилепсии позже, чем поставить его «профилактически».
В чем же причина подобной гипердиагностики, если, по данным большинства исследований, только 1-2 % ЭЭГ могут быть расценены как ложноположительные? По мнению специалистов, первая причина в «человеческом факторе»: в отсутствие должного уровня знаний и опыта. Зачастую неверный диагноз бывает поставлен по одной единственной ЭЭГ, на которой известные доброкачественные эпилептиформные паттерны и варианты нормальной ЭЭГ были расценены как патологические. К таким паттернам относятся: микроспайки, ритмическая тета-активность в височных отведениях, возникающая при дремоте, 14 и 6 Гц позитивные острые волны, 6 Гц фантомные спайк-волны, ритмическая дельта-активность при гипервентиляции и т.д. Большинство этих паттернов были описаны еще в пятидесятых годах XX века, и их выявление не представляет трудности для специалистов, работающих с ЭЭГ.
Однако, на практике данные паттерны встречаются достаточно редко, в подавляющем большинстве случаев ошибочно интерпретируются артефакты, брешь-ритм (breach-rhythm), или «безымянные варианты», которые являются вариациями нормальной ритмики, в результате чего возникают колебания заостренной конфигурации или фрагменты альфа-активности, которые не вписываются в легко узнаваемые ЭЭГ-феномены. Эти безымянные колебания нормального фона были описаны под разными названиями и их можно найти в большинстве ЭЭГ. Дифференцировать нормальные варианты из значимых спайков и острых волн иногда бывает сложно, но существуют определенные рекомендации, которым надо следовать. Избежать этих ошибок могут только обученные опытные врачи эпилептологи/нейрофизиологи, в противном случае пишутся расплывчатые трактовки и нормальная ЭЭГ описывается как патологическая. Здесь складывается ситуация, типичная для человеческой психики: чем меньше знания и опыт, тем с большим вниманием человек относится к незначительным изменениям на ЭЭГ (что в зарубежной литературе называется «Overriding EEG» и «Looking too hard syndrome»). «Снисходительность приходит с опытом», как и понимание того, насколько вариабельна норма на ЭЭГ. Точно так же, как терапевт найдет больше изменений на ЭКГ, чем кардиолог, так же и неопытный врач нейрофизиолог скорее опишет больше патологической активности на ЭЭГ, чем опытный эпилептолог.
Как мы можем исправить существующее положение вещей и уменьшить частоту ошибок, связанных с анализом ЭЭГ?
Здесь необходимо отметить, что в Америке и странах Европы чтением ЭЭГ занимаются неврологи, которые обучаются этому в рамках прохождения резидентуры (аналог российской ординатуры, только длительностью 4-7 лет). В связи с этим, за рубежом проблема неверного анализа ЭЭГ связывается с низким уровнем знаний врачей об ЭЭГ и умением ее интерпретировать. С учетом данной особенности, одно из предложений зарубежных коллег — оценка ЭЭГ не неврологом, а опытным нейрофизиологом. В России ЭЭГ в большинстве клиник описывается специалистами функциональной диагностики, которые в части случаев вообще имеют не медицинское образование, тогда как врач невролог зачастую не знаком даже с основами ЭЭГ. И, надо сказать, данный путь также порочен: процент диагностических ошибок в нашей стране не меньше, если не больше, так как в этом случае отсутствует интерпретация ЭЭГ в контексте клинических данных.
Неверный анализ ЭЭГ врачом-неврологом за рубежом и отсутствие анализа результатов ЭЭГ с позиции клиники — обе ситуации одинаково плохи.
Наверное, наиболее оптимальным вариантом является другое решение, которое также обсуждено в статье Benbadis S.R.:
так как в повседневной практике невролог и психиатр сталкивается с пароксизмальными состояниями и, в частности, с эпилепсией достаточно часто, то трудно представить, чтобы врач не умел читать ЭЭГ и не умел анализировать данные, с которыми работает. Но если мы считаем, что описание ЭЭГ — прерогатива врачей, то система обучения должна быть в корне изменена. ЭЭГ в рамках последипломной подготовки неврологов и психиатров должно уделяться больше времени и внимания. Нужен курс, обучающий врачей анализу ЭЭГ, затем должна быть практика под руководством опытных специалистов, а после — возможность в ходе самостоятельной работы обращаться к специалисту для разбора сложных случаев.
По мнению авторов, к описанию ЭЭГ должна быть применена система, используемая при описании ЭКГ или рентгенографии грудной клетки. Они могут быть оценены экстренно врачами скорой помощи, терапевтами, реаниматологами, но затем должны быть повторно проанализированы специалистами — кардиологами или рентгенологами, для того, чтобы избежать ошибок и неверных диагнозов.
Другой важный методологический прием — первичный анализ ЭЭГ «вслепую», то есть без клинических данных о пациенте (при этом, безусловно, клиническая трактовка в последующем дается с учетом всей информации о заболевании. Так предлагают описывать ЭЭГ многие ведущие эпилептологи мира, чтобы избежать синдрома «слишком тщательного анализа» (“looking too hard” syndrome).
Улучшить ситуацию может:
1. улучшение качества анализа ЭЭГ путем более высокого уровня обучения неврологов и психиатров а, главное, введением контроля уровня знаний
2. обучение «консервативному» чтению ЭЭГ, при котором должна быть описана только четкая эпилептиформная активность, а сомнительные вопросы должны решаться в пользу нормы или дообследования с изменением дизайна исследования
3. обязательная клиническая интерпретация ЭЭГ-данных в тех случаях, когда это возможно
4. создание более четких рекомендаций и руководств по описанию ЭЭГ
5. повторная оценка ЭЭГ специалистом-нейрофизиологом или эпилептологом.
Итак, вернемся к формуле:
Неспецифические симптомы + неверно интерпретированная нормальная ЭЭГ = ошибочный диагноз «эпилепсия»
Надо понимать, что четкая клиническая картина приступов при нормальной ЭЭГ скорее подтверждает диагноз эпилепсии, чем неспецифические симптомы и острые волны на ЭЭГ. Неспецифические симптомы и неубедительная патологическая активность на ЭЭГ (как например, «заостренные двухфазные потенциалы» или «ирритативные знаки») ни в коем случае не должны приводить к диагнозу «эпилепсия».
Материал подготовлен Фоминых В.В., Гриненко О.А., Троицким А.А. на основе следующих статей:
1. Benbadis SR. «Just like EKGs!» Should EEGs undergo a confirmatory interpretation by a clinical neurophysiologist? Neurology. 2013;80(1 Suppl 1):S47-51.
2. Benbadis SR. Errors in EEGs and the misdiagnosis of epilepsy: importance, causes, consequences, and proposed remedies. Epilepsy Behav. 2007;11(3):257-62.
3. Markand ON. Pearls, perils, and pitfalls in the use of the electroencephalogram. Semin Neurol. 2003;23(1):7-46.
Актуальность проблемы
Электроэнцефалографическое исследование (ЭЭГ) позволяет врачу-неврологу контролировать функциональное состояние головного мозга при различных неврологических заболеваниях. Но в настоящее время в отечественной неврологической школе интерес к этому методу невелик. Одним из аспектов данной проблемы является тот факт, что анализ данных ЭЭГ-исследования нельзя уместить только в рамки изменений частотно-волновых гармонических характеристик. Большинство патогномонично значимых феноменов зачастую имеют асинхронный, случайный и псевдохаотический вариант представленности в записи. Также они обладают определенными индивидуальными особенностями, требующими описательных и нематематических характеристик, что не позволяет использовать методы «автоматического» формирования медицинского заключения на основе простых аналитических механизмов гармонических функций.
Электроэнцефалографическое исследование (ЭЭГ) позволяет врачу-неврологу контролировать функциональное состояние головного мозга при различных неврологических заболеваниях. Но в настоящее время в отечественной неврологической школе интерес к этому методу невелик. Одним из аспектов данной проблемы является тот факт, что анализ данных ЭЭГ-исследования нельзя уместить только в рамки изменений частотно-волновых гармонических характеристик. Большинство патогномонично значимых феноменов зачастую имеют асинхронный, случайный и псевдохаотический вариант представленности в записи. Также они обладают определенными индивидуальными особенностями, требующими описательных и нематематических характеристик, что не позволяет использовать методы «автоматического» формирования медицинского заключения на основе простых аналитических механизмов гармонических функций.
Особенную важность индивидуальный подход к анализу ЭЭГ приобретает при анализе различного вида артефактов. Современная ЭЭГ-аппаратура регистрирует чрезвычайно малые величины изменений биоэлектрических потенциалов, из-за этого истинная ЭЭГ-активность может сильно искажаться вследствие воздействия разнообразных физических (технических) и/или физиологических воздействий [2]. В части случаев подобные искажения можно убрать при помощи аналогово-цифрового преобразования и различных фильтров, но если артефактное воздействие совпадает по частотно-волновым характеристикам с реальной ЭЭГ-записью, эти способы становятся неэффективными [1]. Определенную помощь в выделении и нейтрализации подобных артефактов может оказать использование полиграфической записи с автоматическим устранением «типичного» графоэлемента, но такой подход тоже не всегда достаточно эффективен, и в результате основная работа по выявлению и устранению артефактов из ЭЭГ- записи ложится на врача-специалиста.
Особую важность дифференциальная диагностика приобретает при различных пароксизмальных состояниях, в частности эпилепсии. По данным Jeavons (1983), ошибки дифференциальной диагностики весьма существенны, ее гипердиагностика эпилепсии составляет до 20–25% всех случаев впервые диагностированной эпилепсии. Случаи гиподиагностики встречаются реже и составляют, по данным разных авторов, до 10% случаев [3]. В большинстве случаев подобные ошибки связаны не только с особенностями течения заболевания и трудностью верификации его клинической картины, но и с неправильной интерпретацией данных электрофизиологических исследований и, чаще всего, с восприятием артефактов в качестве истинной биоэлектрической активности головного мозга (БЭАГМ).
Цель данной работы состоит в демонстрации, предложении методик определения и классификации наиболее характерных ЭЭГ-артефактов, возникающих при проведении ЭЭГ-исследования.
Материалом для исследования послужил анализ ЭЭГ-записей пациентов различных возрастов, проходивших ЭЭГ-исследование для исключения различных патологических состояний (согласно рекомендациям H. Luders [5], W. Penfield [6]).
Результаты
По происхождению артефакты ЭЭГ-записи можно разделить на физические, возникновение которых связано с различными техническими (технологическими) погрешностями, и физиологические, в возникновении которых принимают участие различные физиологические процессы организма. Наиболее часто из физических артефактов встречаются: сетевая наводка, телефонный артефакт, обрыв проводника, плохой контакт электрода, артефакт высокого импеданса. Из физиологических артефактов часто регистрируются: ЭКГ-артефакт, сосудистый РЭГ-артефакт, кожно-гальванический артефакт (реакция КГР), глазодвигательный артефакт, электроокулограмма (ЭОГ), миографический артефакт – электромиограмма (ЭМГ).
Физические артефакты
Сетевая наводка от сети переменного тока частотой 50 Гц (рис.1) в современных ЭЭГ-регистраторах встречается редко. Причиной ее появления, помимо неисправности аппаратуры, является влияние мощных электромагнитных полей сетевого тока от медицинской аппаратуры (магнитно-резонансной, рентгенологической, физиотерапевтической). Для устранения сетевой наводки необходимо отрегулировать энцефалограф, проверить наличие заземления аппаратуры, нарушение контакта в электродных проводниках. В случае необходимости проведения исследования вблизи источников электромагнитных излучений можно на короткое время выключить все электроприборы, если это невозможно, например, в операционной или палате интенсивной терапии, то можно применить фильтр высокой частоты. Однако следует учитывать, что в этом случае из ЭЭГ исчезают соответствующие частоты биоэлектрической активности головного мозга обследуемого.
Телефонный артефакт. Сходным с сетевой наводкой по происхождению и форме является артефакт от телефонного звонка. Он возникает при расположении телефонного аппарата рядом с пациентом и плохом контакте проводников, что позволяет ЭЭГ-анализатору регистрировать электромагнитные волны, возникающие во время работы телефонного звонка. При последующем анализе при выявлении телефонного артефакта нужно проводить его дифференциальную диагностику со сходными физиологическими графоэлементами, такими как сонные веретена и группы заостренных βволн по типу «щеток» (феномена низкоамплитудной быстрой активности lafa) (рис. 2).
Полный обрыв проводника (потеря контакта с пациентом). Для этого артефакта характерны резкие скачки потенциала с «зашкаливанием» (рис. 3). Чаще всего они появляются при обрыве соединительного провода, плохой установке электрода, поляризации электрода или при накоплении электрических зарядов на теле обследуемого пациента. В таких случаях нужно проверить целостность проводов, соединяющих электроды с входной коробкой электроэнцефалографа.
При обрыве соединительного провода или появлении потенциала поляризации необходимо заменить электрод. По данным Л.Р. Зенкова [2], потенциалы поляризации чаще появляются при использовании дешевых медных и латунных электродов, подвергнутых некачественному золочению или серебрению; для устранения подобной ситуации электроды подвергают хлорированию.
Статический разряд. Данный артефакт чаще всего возникает в условиях низкой влажности, проявляясь в виде единичных электромагнитных всплесков (рис. 4). Для устранения электрических зарядов с тела можно переустановить электроды, подвергнуть кожу под электродом абразии специальной пастой (мелкой наждачной бумагой или стерильной инъекционной иглой) до легкого покраснения, не повреждая дермы, предложить пациенту снять синтетическую одежду.
Артефакт высокого импеданса. Возникает при неправильном наложении электрода на кожу пациента, высыхании контактного геля или отхождения электрода от кожной поверхности. Артефакт характеризуется выявляемой под одним электродом продолженной островолновой активностью, симулирующей электромиограмму. Устраняется при восстановлении контакта электрода с кожей пациента и проводящей средой (рис. 5).
Физиологические артефакты
Как правило, их возникновение обусловлено различными биологическими процессами, протекающими в организме пациента. Наиболее часто в ЭЭГ-записи встречаются электрокардиограмма (ЭКГ-артефакт), реограмма (РЭГ, РГ-артефакт), кожно-гальваническая реакция (КГР-артефакт), электромиограмма (ЭМ-артефакт) и др. Ниже представлены наиболее характерные изменения ЭЭГ-записи, вызываемые физиологическими артефактами.
ЭКГ-артефакт. Чаще всего возникает у обследуемых, страдающих повышением артериального давления, преимущественно в монополярных и поперечных биполярных отведениях. Его возникновение связывают с повышением активности симпатической нервной системы, что облегчает проведение ЭКГ-сигнала на периферийные ткани. ЭКГ-артефакт (рис. 6) представлен ритмичными острыми комплексами, имитирующими эпилептиформную активность – доброкачественный эпилептиформный паттерн детства (ДЭПД), но в отличие от нее лишен медленно-волнового компонента или в случае имитации ДЭПД – его частота устойчива и совпадает с частотой комплексов QRS на ЭКГ, поскольку для ДЭПД ритмичность и совпадение с QRS комплексами не характерны.
Сосудистый РЭГ-артефакт. Также у больных, страдающих повышением артериального давления, часто наблюдается РЭГ-артефакт, который появляется при установке электрода над поверхностью пульсирующего сосуда. Он имеет характерный для реограммы вид, включающий крутой подъем – анакроту и более пологий спуск – катакроту. Может симулировать дельта- активность (рис. 7). Выявление РЭГ-артефакта, как правило, не представляет большого труда, поскольку его основной графоэлемент имеет характерную форму и выявляется чаще всего под конкретным электродом. Устраняется РЭГ-артефакт небольшим смещением электрода в сторону (из зоны сосуда).
Кожно-гальванический артефакт (реакция КГР). Возникает вследствие активации парасимпатической нервной системы больного и повышения потоотделения, вследствие чего происходит общее цикличное изменение импеданса кожных покровов и системы кожа-электрод. На ЭЭГ регистрируются медленно-волновые «тренды», имитирующие смещение электродов. Подавить этот артефакт можно дополнительным обезжириванием кожных покровов пациента, а в случае неэффективности протирания кожи можно ограничить нижнюю полосу пропускания электроэнцефалографа до 0,1 с (рис. 8).
Глазодвигательный артефакт, электроокулограмма. Проявляется в виде медленно-волновых колебаний во фронтополярных отведениях частотой 0,3–2 Гц. Определенные сложности представляет его дифференциальная диагностика с медленно-волновой активностью глубинных отделов лобных долей головного мозга (рис. 9). Возникновение ЭОГ связано с изменением положения глазного яблока (сетчатки). Для ЭОГ характерно затухание амплитуды от лобных отведений по направлению к затылочным, а также симметричность и стереотипная форма потенциалов. Устранить ЭОГ можно, попросив пациента зафиксировать глазные яблоки, придерживая веки собственными пальцами.
Миографический артефакт, электромиограмма. ЭМГ выявляется при мышечном напряжении лобных, жевательных и затылочных мышц. Она может быть спровоцирована как спонтанным напряжением пациента, так и его непроизвольной реакцией на чрезмерно плотно одетую фиксирующую электроды систему.
Дифференцировать ЭМГ следует с β-ритмом, сонными веретенами и спайковой активностью на ЭЭГ (рис. 10). β-ритм отличается от ЭМГ меньшей амплитудой колебаний, неправильным и нерегулярным ритмом. Сонные веретена представляют собой модулированные, диффузные колебания частотой 11–15 Гц, амплитудой около 50 мкВ, продолжительностью от 0,5 до 3 с. Спайковая активность – это потенциалы с острой формой, длительностью 5–50 мс, их амплитуда может превышать фоновую активность в десятки и даже тысячи раз. Устранить ЭМГ можно, предложив обследуемому не сжимать зубы, приоткрыть рот, расслабить мышцы лба и шеи. Если после всех вышеизложенных мероприятий регистрация ЭМГ-артефакта сохраняется, то можно использовать фильтры высоких частот с ограничением полосы пропускания свыше 15 или 30 Гц.
Обсуждение и выводы
Многообразие проявлений артефактов ЭЭГ-записи, трудности в их устранении, а также их сходство с истинными ЭЭГ-паттернами часто заставляют начинающих специалистов отрицать диагностическую ценность метода ЭЭГ в клинической практике, направляя пациентов на другие, подчас дорогостоящие диагностические методы, основанные на иных физических принципах. Тем не менее, как показано выше, выявление, устранение и дифференциальная диагностика ЭЭГ-артефактов не представляет какую-либо сложную и неразрешимую для специалиста проблему.
ЭЭГ-артефакты имеют определенные характеристики, что позволяет отделить их от основной записи (табл. 1, 2), поэтому даже при проведении исследования на современной диагностической аппаратуре специалист должен распознавать и отмечать регистрируемые артефакты, прилагая максимальные усилия к их устранению из основной ЭЭГ-записи, но вместе с тем, полное устранение физиологических артефактов не всегда необходимо, т.к. именно их наличие может косвенно указывать на основную медицинскую патологию, по поводу которой пациент и обратился к врачу.
Возможно, подобные недостатки можно разрешить посредством изменения подготовки специалистов, проводящих нейрофизиологические исследования, с выделением в курсе обучения отдельных тем, посвященных диагностике ЭЭГ-артефактов.
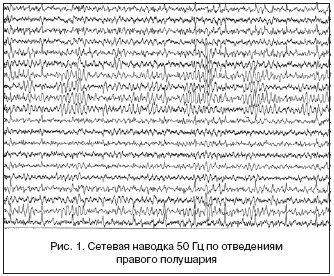

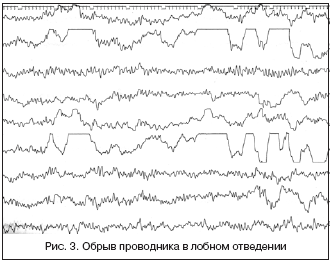
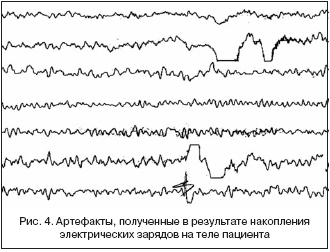
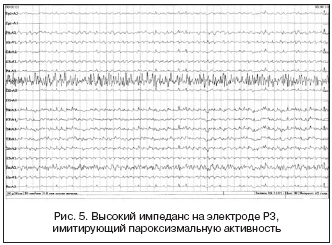
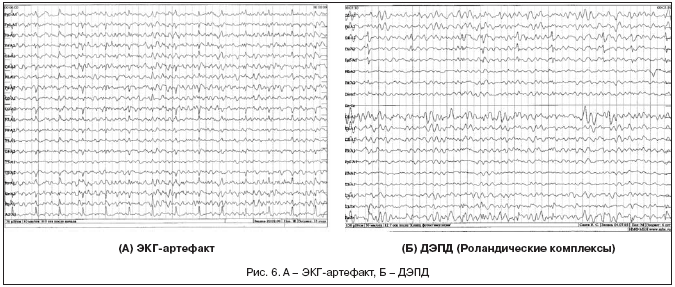
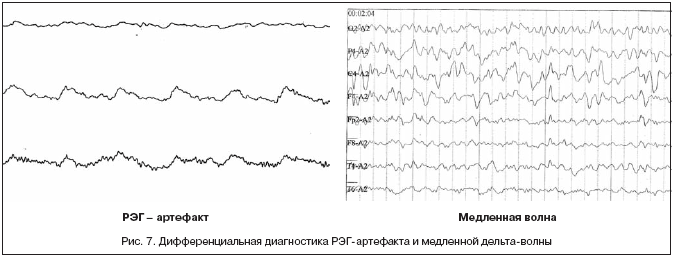
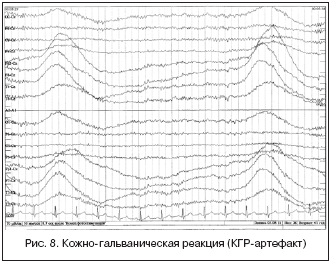
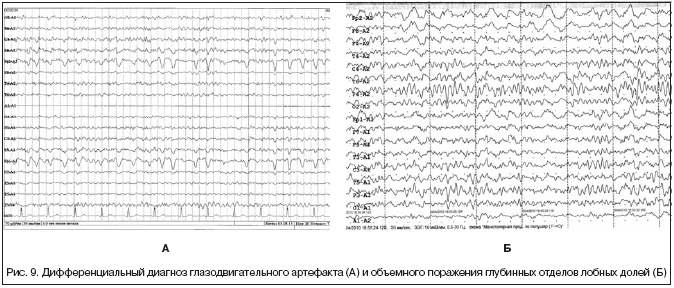



Литература
1. Гуляев С.А., Архипенко И.В. и др. Электроэнцефалография в диагностике заболеваний нервной системы. – Владивосток: изд-во ДВГУ, 2012. 200 с.
2. Зенков Л.Р. Электроэнцефалография с элементами эпилептологии. – Таганрог: Изд–во ТРТУ, 1996.
3. Мухин К.Ю., Петрухин А.С., Глухова Л.Ю. Эпилепсия: атлас электроклинической диагностики. – М.: Альварес Паблишинг, 2004. 440 с.
4. Петрухин А.С., Мухин К.Ю., Глухова Л.Ю. Принципы диагностики и лечения эпилепсии в педиатрической практике. – М., 2009. 43 с.
5. Luders H., Noachtar S. eds. Atlas and Classification of Electroencephalography. –Philadelphia: WB Saunders, 2000. 208 p.
6. Penfield W., Jasper H. Epilepsy and the Functional Anatomy of the Human Brain. – Boston: Little, Brown & Co, 1954. 469 p.
1. Введение
Электроэнцефалографический мониторинг (ЭГГ-мониторинг) — сегодня это основной метод исследования, цель которого регистрация пароксизмального события с целью проведения дифференциального диагноза между эпилептическими и неэпилептическими состояниями, например, такими как парасомнии, синкопальные состояния, стереотипии и другие.
Широкое распространение метода ЭЭГ-мониторинга в первой половине 90-х гг. произвело буквально революционные изменения в диагностике эпилепсии, позволило распознавать сложные в клиническом отношении судорожные припадки. Стало ясно, что многие виды судорожных приступов не укладываются в классическую картину, описанную в медицинских учебниках, что привело к пересмотру взглядов на диагностику и тактику лечения пациентов.
Проведение ЭЭГ назначается для получения ответов на следующие вопросы:
- Какова природа судорожных приступов — эпилептическая или неэпилептическая? (какую болезнь лечить)
- Какая форма эпилепсии? (как правильно лечить, какие препараты)
- Какая локализация приступа? (постановка вопроса о целесообразности хирургического лечения при неэффективности медикаментозного)
- Как протекает лечение? (изменять, отменять препараты)
Прежде чем приступить к ответу на эти вопросы необходимо понять происхождение этого метода, а потом прийти к плодам, результатам многолетних исследований, которые в изобилии разрослись на этом мощном стволе.
2. Понятия, определяющие ВЭЭГ
2.1. ЭЭГ и эпилепсия
Основные понятия, которые можно выделить, разбирая понятие видео-ЭЭГ-мониторинг — ЭЭГ и эпилепсия.
Вспомним определение эпилепсии: эпилепсия является одним из распространенных хронических заболеваний головного мозга. Согласно определению, эпилепсия — это хроническое заболевание головного мозга, характеризующееся повторными непровоцируемыми приступами нарушения двигательных, чувствительных, вегетативных, мыслительных или психических функций, возникающих вследствие чрезмерных нейронных разрядов (ILAE, 1989).
Электроэнцефалография — метод исследования биоэлектрической активности головного мозга, основанный на определении разности электрических потенциалов, генерируемых нейронами в процессе их жизнедеятельности. Регистрирующие электроды располагают так чтобы на записи были представлены все основные отделы мозга. Получаемая запись — ЭЭГ — суммарная электрическая активность миллионов нейронов, представленной преимущественно потенциалами дендритов и тел нервных клеток: возбудительными и тормозными постсинаптическими потенциалами и частично — потенциалами дендритов и тел нервных клеток. То есть ЭЭГ — как бы визуализированный результат функциональной активности головного мозга.
Здесь наверное стоило бы уделить долю внимания анатомии нейрона и его физиологии.
Нейрон является главной клеткой центральной нервной системы. Формы нейронов чрезвычайно многообразны, но основные части неизменны у всех типов нейронов: тело и многочисленных разветвленных отростков. У каждого нейрона есть два типа отростков: аксон, по которому возбуждение передается от нейрона к другому нейрону, и многочисленные дендриты (от греч. дерево), на которых заканчиваются синапсами (от греч. контакт) аксоны от других нейронов. Нейрон проводит возбуждение только от дендрита к аксону.
Основным свойством нейрона является способность возбуждаться (генерировать электрический импульс) и передавать (проводить) это возбуждение к другим нейронам, мышечным, железистым и другим клеткам.
Нейроны разных отделов мозга выполняют очень разнообразную работу, и в соответствии с этим форма нейронов из разных частей головного мозга также многообразна.
Многолетние исследования в области нейрофизиологии привели к выводам, что следующие электрические события присущи нейронам и могут вносить в вклад в суммарную биоэлектрическую активность мозга (ЭЭГ): постсинаптические возбуждающие и тормозные потенциалы (ВПСП, ТПСП), и распространяющиеся потенциалы действия (ПД). ВПСП и ТПСП возникают либо в дендритах, либо на теле нейрона. ПД генерируются в зоне аксонного «холмика» и далее распространяются по аксону.

Нейрон. Возбуждающие и тормозные ПСП, потенциал действия.
Обычная спонтанная ЭЭГ, ее основные ритмы возникают в результате пространственной и временной суммации постсинаптических потенциалов (ПСП) большого количества корковых нейронов. Временные характеристики процесса суммации достаточны медленны по сравнению с длительностью ПД.
 Определенная степень синхронизации задается различными подкорковыми структурами, которые выполняют роль «водителя ритма» или пейсмекера. Среди них наиболее значимую роль в генерации ритмов ЭЭГ играет таламус.
Определенная степень синхронизации задается различными подкорковыми структурами, которые выполняют роль «водителя ритма» или пейсмекера. Среди них наиболее значимую роль в генерации ритмов ЭЭГ играет таламус.
Потенциалы действия корковых нейронов не играют существенной роли в генерации основных ритмов ЭЭГ, поскольку являются очень короткими. Определяющая роль ПД в формировании паттернов ЭЭГ возникает в ситуациях, когда значительное количество нейронов синхронизируется и одновременно выдает пачки или «вспышки» ПД. Такой режим характерен для пароксизмальных событий, например, для эпилептических приступов и тогда морфология волн ЭЭГ в существенной степени определяется потенциалами действия. При этом острые компоненты ЭЭГ (спайки, острые волны) отражают не отдельные ПД, а скорее всю «пачку» потенциалов действия. Именно таким образом формируются многие эпилептиформные паттерны ЭЭГ, наиболее известным из которых является комплекс спайк-волна. Следует отметить, что подобная модель применима также в объяснении генеза физиологических острых компонентов ЭЭГ.

Таким образом, в генерации ЭЭГ принимают участие и постсинаптические потенциалы и потенциалы действия. Основная ритмика ЭЭГ определяется градуальными изменениями постсинаптических потенциалов благодаря пространственной и временной суммации отдельных ПСП в больших популяциях нейронов, которые относительно синхронизированы и находятся под воздействием подкоркового водителя ритма. Пароксизмальные же события, синхронизирующие значительное количество нейронов, которые продуцируют вспышки потенциалов действия, отвечают за формирование многих эпилептиформных феноменов ЭЭГ, в частности комплексов спайк-волна.
Собственно изучением всего этого процесса и занимается электроэнцефалография.
2.2. История изучения ЭЭГ
Начало изучению электрических процессов мозга было положено Д. Реймоном (Du Bois Reymond) в 1849 году, который показал, что мозг, также как нерв и мышца, обладает электрогенными свойствами.
Начало электроэнцефалографическим исследованиям положил В.В.Правдич-Неминский, опубликовав 1913 году первую электроэнцефалограмму записанную с мозга собаки. В своих исследованиях он использовал струнный гальванометр. Так же Правдич-Неминский вводит термин электроцереброграмма.
Первая запись ЭЭГ человека получена австрийским психиатром Гансом Бергером в 1928 году. Он же предложил запись биотоков мозга называть «электроэнцефалограмма».
По мере совершенствования компьютерной техники в 1996 году осуществлена методика амбулаторной полиграфической записи посредством 17-канального электроэнцефалографа (16 каналов ЭЭГ и 1 канал ЭКГ) с использованием переносного персонального компьютера (ноутбука) [Ebersole J. S. et al, 1996].
И наконец к концу 20 века у в арсенале эпилетологических и нейрофизиологических служб получается несколько видов методики ЭЭГ: рутинная ЭЭГ, холтеровское ЭЭГ и ВЭЭГ.
ЭЭГ стал «лезвием бритвы», наиболее качественным и информативным методом диагностики формы эпилепсии и позволяет регистрировать клинико-электроэнцефалографический коррелят эпилептического приступа, что дает возможность установить более точный диагноз и назначить рациональную схему антиэпилептической терапии.
3. Проведение ЭЭГ. Взгляд с 3 позиций
ЭЭГ мониторинг можно рассмотреть с 3 позиций: пациента, врача который проводит исследование в данный момент и со стороны врача, который расшифровывает видео-ЭЭГ-мониторинг постфактум.
Как предисловие стоит просто назвать показания и противопоказания к проведению этого исследования (Авакян)
Показания:
- Диагностика эпилепсий и эпилептических синдромов.
- Пароксизмальные состояния неясного генеза, вызывающие подозрение на наличие эпилепсии.
- Фармакорезистентные приступы (с целью выявления псевдоэпилептических пароксизмов или уточнения формы эпилепсии).
- Контроль эффективности лечения.
- Медикаментозная ремиссия (объективная констатация ремиссии).
- Подготовка к отмене антиконвульсантной терапии.
- Прехирургическое обследование.
- Субклиническая эпилептическая активность.
- Прогрессирующие когнитивные и поведенческие расстройства у детей.
- Первый судорожный приступ.
Противопоказания:
Противопоказаний к проведению ЭЭГ нет.
3.1. Устройство ВЭЭГ-лаборатории
Сутью метода ВЭЭГ является непрерывная запись ЭЭГ сигнала и видеоизображения пациента в течение длительного времени. Минимальная продолжительность исследования 15 минут, максимальная не лимитирована (до 7-14 суток). Обязательным условием является идеальная синхронизация видеоизображения и ЭЭГ во времени.
Основой системы ЭЭГ-мониторинга является многоканальный усилитель сигналов, имеющий возможность записи 19-32-64-128-канальной ЭЭГ, ЭКГ-канала, датчика дыхания, электромиографических и электроокулографических каналов.
К усилителю подключаются соответствующие регистрирующие датчики. Крепление ЭЭГ-электродов для длительной регистрации производится с помощью специальной шапочки или клеящей пасты. Конструкция электродной системы позволяет пациенту перемещаться по палате, не доставляет неудобств и делает проведение исследования комфортным.
Сигналы с усилителя посредством проводной или беспроводной связи направляются на рабочую компьютерную станцию.
Видеоизображение записывается посредством цифровых видеокамер, количество их может быть произвольным, в большинстве систем предусмотрена возможность использования 1-2 камер.
Обработка результатов производится изучением синхронного изображения ЭЭГ и видеоизображения, скорость прокрутки изображения выбирается произвольно. Программа обработки ЭЭГ включает возможности спектрального и когерентного анализа, программ трехмерной локализации диполя, и других вариантов компьютерного анализа.
Отделение видео-ЭЭГ-мониторинга должно включать в себя 3 основных звена:
- палата пациента, оборудованная видеокамерами, микрофоном, кнопкой пациента для регистрации событий;
- помещение для записывающих станций и персонала, осуществляющего слежение и контроль за пациентом.
- помещение для врачей (ординаторская), где располагаются станции просмотра и анализа записанных данных. Важным требованием к ВЭЭГ оборудованию является возможность просмотра и обработки ранее записанных исследований или текущего, не прерывая текущее исследование.
3.2. Схемы монтажа, подготовка пациента и начало исследования
Врач, проводящий исследование накладывает электроды либо встроенные в шапочку либо поочередно наклеивает каждый электрод соответственно своему месту. В обычной практике ЭЭГ-регистрирующие электроды располагают согласно международной системе «10-20».
В соответствии с системой «10–20» у испытуемого делают три измерения черепа:
- продольный размер черепа — измеряют расстояние по черепу между точкой перехода лобной кости в переносицу (назион) и затылочным бугром;
- поперечный размер черепа — измеряют расстояние по черепу через макушку (вертекс) между наружными слуховыми проходами обоих ушей;
- длину окружности головы, измеренной по этим же точкам.
Электроды, расположенные по средней линии, отмечаются индексом Z; отведения на левой половине головы имеют нечетные индексы, на правой — четные.
Отведения в системе «10–20»:
- фронтальные (F1, F2., F3 F4, Fz);
- лобные полюса (Fp1, Fp2);
- центральные (С1, С2, С3,С4, Сz);
- париетальные (Р1, Р2 Р3 Р4, Рz);
- темпоральные (T1, Т2, Т3, Т4, Т5, Тz);
- окципитальные (О1,О2, 0z).
Крепление и наложение электродов осуществляется в следующем порядке:
- Электроды подсоединяются к усилителю. Для этого штеккеры электродов вставляются в электродные гнезда усилителя.
- Ватным тампоном, смоченным в спирте обезжириваются места, предназначенные для постановки электродов.
- Непосредственно перед постановкой каждого электрода электродный гель наносится на контактирующую с кожным покровом поверхность. Необходимо помнить, что гель, применяемый в качестве проводника, должен быть предназначен для электродиагностики.
- На пациента надевается шлем/шапка со встроенными поверхностными электродами или каждый поврхностный электрод по отдельности с креплением его при помощи специального клея — коллодия. От практики игольчатых электродов ныне отходят согласно последним исследованиям ученых США и Великобритании. Места расположения электродов определяются соответственно системе расположения электродов. Необходимо помнить, что наложенные электроды не должны вызывать у пациента неприятные ощущения.
- Соответственно обозначениям, указанным на панели усилителя, устанавливаются электроды на предусмотренных системой местах, парные электроды располагаются симметрично.
После правильной установки и калибровки начинается само ВЭЭГ-исследование. В сегодняшней практике используются ВЭЭГ исследования длиной 4-5 часов (утренние/дневные/вечерние), длиной 9-10 часов (ночные), длиной 24 часа и более (холтеровские ВЭЭГ-мониторинги). Наиболее распространенными сегодня, являются короткие ВЭЭГ-исследования (60%), далее ночные — 36%, холтеровские — 4-5%
Премедикация перед исследованием, как правило, не проводится, поскольку введение препаратов, не входящих в схему лечения, может менять картину ЭЭГ, что не позволит оценить истинные параметры биоэлектрической активности мозга.
Не рекомендуется отмена или изменение схемы лечения в день исследования, что не позволит оценить эффекты терапии.
Принципиальное значение в диагностике эпилепсии имеет ЭЭГ сна. По мнению ведущих специалистов».. регистрация ЭЭГ в течение одной минуты поверхностного сна дает больше информации для диагностики эпилепсии, чем час исследования в состоянии бодрствования».
4. Понятия нормы и патологии в ВЭЭГ
4.1. Стандарты ВЭЭГ
Альфа ритм. Ритм частотой 8-13 Гц средней амплитуды 50 мкВ (15-100 мкВ), максимально выражен в задних (затылочных) отведениях при закрытых глазах. Возможно появление модуляций альфа ритма ( «веретен»), заключающихся в периодическом нарастании и снижении амплитуды волн. Выраженность альфа ритма зависит от многих условий, что необходимо учитывать при анализе ЭЭГ. Представленность альфа ритма на ЭЭГ и его регулярность уменьшаются при открывании глаз, записи в состоянии беспокойства, при активной умственной деятельности (решение задач), а также во время сна. У женщин во время менструации может быть увеличение его частоты. Установлено, что у здорового взрослого человека частота альфа ритма довольно стабильна и является генетически детерминированной.
Мю (роландический, аркообразный) ритм. Ритм аркообразной формы, частоты альфа (обычно, 8-10 Гц). По амплитуде не превышает альфа ритм (обычно, несколько ниже); регистрируется в центральных отделах у 20% здоровых взрослых. У детей данный ритм начинает хорошо определяться с 3-месячного возраста, лучше у девочек. Он не реагирует на открывание глаз, но блокируется с одной стороны при выполнении движений в контралатеральной конечности. Имеет малое диагностическое значение, даже при значительном его усилении или выраженной асимметрии.
Бета ритм. Ритм частотой более 13 Гц, средней амплитуды 10 мкВ; максимально выражен в передних отделах. Типичная частота бета ритма в норме составляет 18-25 Гц, менее распространен ритм частоты 14-17 Гц и крайне редко — свыше 30 Гц, У 70% здоровых людей амплитуда бета ритма не превышает 10 мкВ; и лишь у 3% — превышает 20мкВ. Бета ритм имеет максимальную выраженность в лобно-центральных отведениях. Бета активность несколько усиливается в период сонливости, при засыпании (I стадия сна), во время ФБС и иногда при пробуждении. В период глубокого сна (III, IV стадии фазы медленного сна) амплитуда и выраженность ее существенно снижаются.
Стойкое увеличение амплитуды бета активности свыше 25 мкВ, особенно с распространением её на задние отведения — признак патологии, однако, нозологически не специфичной. Традиционно усиление бета активности ( «excessive fast») связывалось с текущим эпилептическим процессом.
Тета ритм. Ритм частотой 4-7 Гц, по амплитуде, обычно превышающий основную активность фоновой записи. Встречается различной степени выраженности на ЭЭГ у всех здоровых детей. Тета активность начинает регистрироваться в центральных отделах уже с 3-недельного возраста, постепенно нарастая с возрастом и достигая максимума в 4-6 лет. В этом возрасте тета ритм является доминирующим на ЭЭГ у детей. Большинство исследователей считают, что у подростков и молодых взрослых при бодрствовании с закрытыми глазами низкоамплитудная тета активность (не превышающая амплитуды фона) частоты 6-7 Гц с бифронтальным преобладанием является нормальной, если она не превышает 35% фоновой записи.
4.2. Запись во сне
Сон является мощным активатором эпилептиформной активности. Неврологу, а тем более эпилептологу, важно уметь идентифицировать фазы и стадии сна. Известно, что эпилептиформная активность отмечается преимущественно в I и II стадии медленного сна, тогда как во время «дельта сна» и в периоде ФБС она чаще всего подавляется.
В настоящее время для дифференциации стадий сна применяется классификация Dement & Kleitman в модификаций Recbtshaffen & Kales (1968), Согласно этой классификации выделяются 2 фазы сна: фаза медленного сна (ФМС) и фаза быстрого сна (ФБС),
ФМС (в англоязычной литературе — non-REM sleep) развивается на фоне ослабления влияния активизирующей коры, восходящей ретикулярной формации и усиления активности синхронизирующих тормозящих структур.
В ФМС выделяют 4 стадии.
I стадия сна (дремота) характеризуется умеренным замедлением основной активности на ЭЭГ. Проявляется постепенным исчезновением альфа ритма и появлением ритмичной тета активности в центральной и лобно-центральной области, Может появляться периодическая ритмическая высокоамплитудная медленная активность частотой 4-6 Гц в лобных отведениях. Длительность I стадии сна у здорового человека составляет не более 10-15 минут.
II стадия сна (стадия «сонных веретен»). Наблюдаются следующие феномены. 1. Характерный признак II стадии сна — появление «сонных веретен» или сигма-ритма. Этот феномен представляет собой ритмические веретенообразно нарастающие и снижающиеся по амплитуде вспышки с частотой 12-16 Гц и амплитудой 20-40 мкВ, преимущественно в центрально-париетальных отделах. Длительность «сонных веретен» колеблется от 0 до 2 сек. Высокоамплитудные и продолжительные (около 3 сек) сонные веретена с преобладанием в лобных отведениях — обычно признак патологии.
III стадия сна характеризуется нарастанием амплитуды и количества медленных волн, преимущественно, дельта диапазона. Регистрируются К-комплексы и «сонные веретена». Дельта волны на эпохе анализа ЭЭГ занимают до 50% записи. Отмечается снижение индекса бета активности.
IV стадия сна характеризуется исчезновением «сонных веретен» и К-комплексов, появлением высокоамплитудных (не менее 50 мкВ} дельта волн, которые на эпохе анализа ЭЭГ составляют более 50% записи. III и IV стадии сна являются наиболее глубоким сном. Они объединены под общим названием «дельта сон».
В фазе быстрого сна (парадоксальный сон, REM-сон) отмечается ослабление влияния тормозящей ретикулярной формации и усиление десинхронизирующих активизирующих механизмов. При входе в ФБС нарастает бета активность. Данная фаза сна характеризуется появлением на ЭЭГ картины десинхронизации в виде нерегулярной активности с одиночными низкоамплитудными тета волнами, редкими группами замедленного альфа ритма и острыми «пилообразными» волнами. ФБС сопровождается быстрыми движениями глазных яблок и диффузным снижением мышечного тонуса. Именно в эту фазу сна у здоровых людей происходят сновидения. Начало сна с фазы быстрого сна или возникновение ее менее, чем через 15 минут после засыпания — признак патологии.
Нормальный сон взрослых и детей состоит из чередования серии циклов ФМС и ФБС. ФМС наиболее выражена в первую половину ночи и занимает 75% всего сна. Во второй половине ночи наиболее представлена ФБС (фаза сновидений), которая занимает около 25% ночного сна. Продолжительность одного цикла сна у детей младшего возраста составляет 45-55 минут; у взрослых 75-100 минут. За ночь у здорового человека возникает от 4 до 6 циклов сна.
4.3. Медленноволновая активность.
Медленноволновая активность. Этот термин включает в себя активность на ЭЭГ в форме замедления ритма по сравнению с возрастной нормой. Согласно международной классификации выделяют следующие варианты медленноволновой активности:
- замедление основной активности;
- периодическое замедление;
- продолженное замедление.
Замедление основной активности констатируется, когда основные ритмы имеют более медленные частотные характеристики по сравнению с возрастной нормой: в 1 год — частота менее 5Гц, в 4 года — менее 6 Гц, в 5 лет — менее 7Гц, в 8 лет и старше — менее 8 Гц.
Периодическое замедление. Периодическое замедление может быть нерегулярным и ритмическим, генерализованным и региональным. Выраженное периодическое ритмическое генерализованное замедление (обычно с преобладанием в лобных отведениях) иногда наблюдается при генерализованных формах эпилепсии. Нерегулярное региональное замедление (чаще в височных отведениях) может быть косвенным ЭЭГ признаком парциальной эпилепсии или локального органического поражения головного мозга.
Продолженное замедление констатируют в случае если данный паттерн занимает около 90% записи, и нет реакции на внешние стимулы. Всегда является патологическим признаком и свидетельствует об прогрессирующем очагово-деструктивном поражении мозга. В этом случае медленно-волновая активность отражает изменение коркового электрогенеза, вызванного анатомическим дефектом неирональных сетей. Она может сочетаться с нормальным или замедленным основным ритмом; возникает по одному из отведений (например, левому височному) или по всей гемисфере. Как правило, представлено тета (реже дельта) активностью низкой амплитуды, не реагирующей на экзогенные стимулы.
4.4. Провоцирующие пробы
Провоцирующие пробы. Фоновая запись биоэлектрической активности головного мозга осуществляется в состоянии пассивного бодрствования пациента с закрытыми глазами. С целью выявления нарушений ЭЭГ применяются провоцирующие пробы, Наиболее значимые из них следующие:
- Открывание-закрывание глаз.
- Гипервентиляция.
- Ритмическая фотостимуляция.
- Фоностимуляция.
- Депривация сна.
- Стимуляция умственной активности.
- Стимуляция мануальной активности.
Подробно остановимся на первых.
Проба на открывание-закрывание глаз служит для установления контакта с пациентом. При этом медицинский работник убеждается, что пациент находится в сознании и выполняет инструкции. Данная проба позволяет выявить реактивность альфа-ритма и других видов активности на открывание глаз. В норме при открывании глаза блокируется альфа ритм, нормальная и условно нормальная медленноволновая активность. Наоборот, отсугсгвие реакции паттернов на открывание глаз — как правило, признак патологической активности. Блокирование при открывании глаз затылочной пик-волновой активности у пациентов с доброкачественной затылочной эпилепсией Гасто является важным дифференциальным признаком с симптоматической затылочной эпилепсией. Следует помнить, что при некоторых формах фотосенситивной эпилепсии, эпилепти-формная активность на ЭЭГ возникает в момент закрывания глаз. Это может быть связано с исчезновением фиксации взора при закрытых глазах. Данный феномен был описан Panayiotopoulos (1998) и назван им «fixation off» или фотосенситивностью.
Гипервентиляция реально проводима у детей после 3-х лет. Продолжительность от 3 мин у детей до 5 мин у взрослых. Гипервентиляцию нельзя проводить в самом конце записи ЭЭГ, так как патологическая активность нередко появляется спустя некоторое время после окончания пробы. Основное назначение гипервентиляции — выявление генерализованной пик-волновой активности, а иногда и визуализация самого приступа (обычно абсанса). Реже появляется региональная эпилептиформная активность. Согласно наблюдениям Благо-склоновой Н.К. и Новиковой Л. А. (1994), появление пароксизмальных вспышек медленных волн при гипервентиляции свойственно здоровым детям и подросткам и является вариантом нормы. По мнению Daly & Pediey (1997), патологическая реакция на гипервентиляцию включает только появление на ЭЭГ пик-волновой активности или выраженной асимметрии паттернов. Принципиально важно, что любая другая реакция, в том числе и появление дельта активности, — индивидуальный вариант нормы. Таким образом, согласно современным воззрениям, оценка пароксизмальной генерализованной (нередко с бифронтальным преобладанием) ритмической тета-дельта активности при гипервентиляции как гипотетической «дисфункции мезо-диэнцефальных структур» несостоятельна. Подобная оценка нормальных, по своей сути, паттернов не имеет никакого значения для клиники, приводит к терминологической путанице и напрасному беспокойству, как врачей неврологов, так и самих пациентов.
Ритмическая фотостимуляция (РФС) является важнейшей пробой для выявления патологической активности при фотосенситивных формах эпилепсии. Используется классическая методика Jeavons & Harding (1975). Лампа стробоскопа должна находиться на расстоянии 30 см от закрытых глаз пациента. Необходимо использование широкого спектра частот, начиная от 1 вспышки в сек и, заканчивая частотой 50 Гц. Наиболее эффективна в выявлении эпилептиформной активности стандартная РФС с частотой 16 Гц. Возможны следующие реакции на РФС:
- Отсутствие очевидной реакции.
- Усвоение ритма: появление колебаний на ЭЭГ синхронно со вспышками при РФС.
- Фотомиоклонический ответ: при РФС возникает «трепетание» век и подергивание псриокулярной мускулатуры (миоклонический гиперкинез) синхронно со вспышками света. Это отражается на ЭЭГ отчетливым «ритмическим миографическим артефактом» в передних отведениях.
- Фотопароксизмалъный ответ: появление при РФС эпилептиформной активности, чаще возникают короткие разряды генерализованной быстрой (4 Гц и выше) полипик-волновой активности. По классификации фотосенситивных эпилепсии (Binnie и соавторы, 1992), выделяют форму фотосенситивной эпилепсии, при которой приступы возникают исключительно в лабораторных условиях во время РФС при ЭЭГ исследовании. Наиболее типично возникновение миоклонических пароксизмов, вовлекающих мышцы лица, плечевого пояса и рук, синхронно со вспышками света. В повседневной жизни приступы отсутствуют, даже при воздействии бытовых факторов РФС (мелькание света). Как правило, данная форма эпилепсии выявляется случайно при направлении больных на ЭЭГ исследование по причинам, не имеющим отношения к эпилепсии. Большинство авторов не рекомендуют назначение АЭП при этой форме, да и само отнесение таких случаев к эпилепсии вызывает сомнение. Фотопароксизмалъный ответ с высокой достоверностью коррелирует с наличием фотосенситивной эпилепсии.
4.5. Артефакты
Артефакты представляют собой любые графоэлементы на ЭЭГ, не являющиеся отражением электрической активности головного мозга. Подразделяются на механические и биоэлектрические. Механические артефакты бывают инструментальные, электродные и от электросети. Наиболее распространен артефакт вследствие «наводки» от сети переменного тока (отсутствие заземления, использование рядом различной медицинской аппаратуры) в виде появления синусоидальных колебаний частоты 50 Гц.
Биоэлектрические артефакты подразделяются на следующие:
- Миогенные артефакты. Наиболее частый вид артефактов. Регистрируются высокочастотные колебания миограммы, обычно преобладающие в височных отведениях. Они чаще вызваны напряжением жевательной мускулатуры, мимических мышц, мышц шеи. Артефакт от фасцикуляторного тремора напоминает аркообразный мю-ритм и наблюдается максимально в лобно-височных отведениях. Глоссокинетический артефакт возникает при ритмичных движениях языка, например, во время разговора или сосания (кормление младенцев во время ЭЭГ исследования).
- Сердечные и дыхательные артефакты. Электрод, находящийся на крупном сосуде, может вызывать артефакт, напоминающий графоэлемент реоэнцефалограммы. На ЭЭГ могут быть зарегистрированы электрокардиографические потенциалы, которые необходимо отличать от доброкачественных эпилептиформных нарушений детства. Данные потенциалы преобладают на электроэнцефалограмме при электроцеребральной инактивации (гибель мозга). Также встречаются артефакты, обусловленные экскурсией грудной клетки (часто во время проведения гипервентиляции).
- Окулографичесше артефакты. Связаны с активностью m. orbicularis oculi и регистрируются обычно в лобных отведениях. Возникают при ритмическом моргании (тикоидный гиперкинез), нистагме.
- Артефакты, вызванные изменением сопротивления кожи. Изменение сопротивления кожных покровов может быть обусловлено различными биохимическими процессами в организме. Наиболее часто данный тип артефактов возникает при волнении пациентов во время ЭЭГ исследования, что сопровождается выраженной потливостью.
При этом врач осуществляющий мониторинг должен уметь дифференцировать эти артефакты. Если, например, артефакт не уходит с течением времени, необходимо проверить электрод на полноценность соединения с усилителем, с пациентом и в случае необходимости заменить его/настроить.
5. Эпилептиформная активность
Эпилептиформная активность характеризуется появлением на ЭЭГ острых волн или пиков, которые резко отличаются от основной активности фона и возникают преимущественно у лиц, страдающих эпилепсией. Классификация нарушений ЭЭГ, принятая Американской ассоциацией нейрофизиологов [Daly & Pedley, 1997], придерживается строгой терминологии в обозначении патологических феноменов. В классификации общепринят термин «эпилептиформная активность», в связи с его исключительным применением к электроэнцефалографическим феноменам.
Согласно классификации нарушений ЭЭГ различают 9 межприступных (интериктальных) и два приступных (иктальных) эпилептиформных паттерна.
Межприступные эпилептиформные изменения:
- пики (спайки);
- острые волны;
- доброкачественные эпилептиформные нарушения детства (ДЭНД, «роландические» комплексы);
- комплексы пик-медленная волна;
- комплексы пик-медленная волна 3 Гц;
- медленные комплексы пик-медленная волна;
- множественные пики (полиспайки);
- гипсаритмия;
- фотопароксизмальный ответ (фотопароксизмальная реакция).
Иктальные эпилептиформные изменения:
- ЭЭГ приступа;
- ЭЭГ статуса.
Рассмотрим все указанные варианты эпилептиформных нарушений на ЭЭГ:
1. Пики (спайки) — эпилептиформный феномен, отличный от основной активности и имеющий пикообразную форму. Период пика составляет от 40 до 80 мсек. Это специфичный эпилептиформный паттерн, который наблюдается в рамках различных форм эпилепсии (генерализованных и парциальных). Одиночные пики встречаются исключительно редко; обычно они предшествуют появлению волн. Согласно базисным принципам электрофизиологии, появление спайков на ЭЭГ отражает процессы возбуждения корковых нейронов, а медленных волн — процессы торможения.
2. Острая волна — эпилептиформный феномен, отличный от основной активности, период которого составляет 80-200 мсек. Согласно данным ряда авторов [Eed-Oloffson, 1971; Gregori 1993], этот паттерн редко наблюдается у здоровых людей, и высоко специфичен в отношении эпилепсии. Острые волны, также как и пики, могут регистрироваться в виде региональных, мультирегиональных и генерализованных феноменов. Острая волна может встречаться, как изолированно (особенно, при парциальных формах эпилепсии), так и предшествуя медленной волне. Следует помнить, что острые волны, как и пики, могут представлять нормальные физиологические феномены: доброкачественные эпилептиформные транзиты сна (BETS), Wicket — потенциалы, 14 и 6 Гц позитивные спайки и некоторые другие.
3. Доброкачественные эпилептиформные нарушения детства (ДЭНД) — эпилептиформный феномен, который представлен в виде стереотипного электрического диполя, состоящего из острой волны, с последующей медленной волной. Амплитуда негативного полюса составляет 150-300 мкВ, — часто в 2 раза больше позитивного. Общий период комплекса составляет 80-120 мсек. Этот паттерн легко узнаваем, благодаря типичной морфологии, напоминающей зубцы QRST на ЭКГ [Мухин К. Ю. и соавт., 2001]. Для комплексов ДЭНД характерна тенденция к их группированию (дуплеты, триплеты и т.д.), а также усиление их представленности и амплитуды в фазу медленного сна. Доброкачественные эпилептиформные нарушения детства возникают, преимущественно, в возрасте от 3 до 14 лет и являются характерным паттерном при идиопатических парциальных формах эпилепсии. С наступлением пубертата их выраженность уменьшается, и они в большинстве случаев постепенно исчезают после 14-15 лет. Предполагается, что данный ЭЭГ паттерн является возраст-зависимым и генетически детерминированным с аутосомно-доминантным наследованием с низкой пенетрантностью и вариабельной экспрессивностью [Stephani, 2002].
4. Комплексы пик-медленная волна — представляют паттерн, состоящий из пика и следующей за ним медленной волны. Наиболее часто комплексы пик-медленная волна регистрируются в виде генерализованных разрядов, представленность и амплитуда которых усиливается в ФМС, при ГВ и РФС. Данная ЭЭГ картина высоко специфична для идиопатических генерализованных форм эпилепсии детского и юношеского возраста. Однако по данным Doose & Baier (1987), в 10-17% случаев генерализованные комплексы пик-медленная волна могут быть обнаружены у клинически здоровых лиц, в основном, у родственников пробандов с абсансными формами эпилепсии.
В виде единичных паттернов комплексы пик-медленная (или острая-медленная) волна встречаются при криптогенных и симптоматических формах парциальной эпилепсии.
5. Комплексы пик-медленная волна с частотой 3 Гц — представляют регулярный разряд генерализованных паттернов, состоящих из единичных спайков со следующей медленной волной с частотой от 2,5 до 3,5 Гц. Согласно классификации нарушений ЭЭГ, для отнесения паттернов в данную группу, продолжительность этих комплексов должна составлять более 3 секунд. Частота комплексов во время разряда непостоянна. В начале разряда она составляет 3-4 Гц, тогда как к финалу снижается до 2,5-2,25 Гц. Характерно амплитудное преобладание паттернов в лобных отведениях. Медленный сон вызывает активацию пик-волновых комплексов. При этом продолжительность разрядов во время сна укорачивается и одновременно возможно некоторое замедление частоты комплексов. Данный ЭЭГ паттерн характерен для абсансных форм эпилепсии, особенно — детской абсанс эпилепсии. Продолжительность разряда пик-волновых комплексов более 3 сек с высокой вероятностью является иктальным феноменом типичных абсансов.
6. Медленные комплексы пик-медленная волна — представляют собой нерегулярные разряды комплексов пик (а чаще — острая волна)-медленная волна, частотой менее 2,5 Гц. Согласно классификации нарушений ЭЭГ, продолжительность этих комплексов должна составлять более 3 секунд. Комплексы состоят из би- и трифазных негативных острых волн с периодом 150-200 мсек. и следующих за ними высокоамплитудных (300-400 мкВ) негативных медленных волн. Они билатерально-синхронны, однако, в ряде случаев возможна их амплитудная асимметрия и начальная асинхрония. Характерная особенность этого паттерна — тенденция к усилению выраженности изменений во время ФМС.
7. Полипики (множественные пики) — определяются как группа генерализованных билатерально-синхронных, следующих друг за другом 3-х и более пиков частоты от 10 Гц и выше. Каждая группа полипиков может завершаться медленной волной (полипик-волновые комплексы). Генерализованные полипики являются специфичным паттерном для миоклонических форм эпилепсии, таких как юношеская миоклоническая эпилепсия, доброкачественная миоклоническая эпилепсия младенчества. Однако этот паттерн может встречаться и при парциальных формах эпилепсии, у больных синдромом Леннокса-Гасто, а также в случаях прогрессирующих эпилепсии с миоклонусом (болезни Лафора, Унферрихта-Лундборга и др.).
8. Гипсаритмия — эпилептиформный паттерн, характеризующийся нерегулярной диффузной продолженной высокоамплитудной (>300 мкВ) медленноволновой активностью (1-3 Гц), на фоне которой регистрируются мультирегиональные пики и острые волны. В отдельных случаях возможно преходящее кратковременное уплощение этой активности (вплоть до биоэлектрического молчания). Данный вариант гипсаритмии Ohtahara (1978) назвал паттерном вспышка-угнетение. В некоторых случаях (симптоматический вариант синдрома Веста) гипсаритмия существенно доминирует в одной из гемисфер, сочетаясь со стойкими региональными спайками в этой зоне. Сон существенно модифицирует гипсаритмию: во время ФМС амплитуда и представленность эпилептиформных изменений увеличивается и становится периодической, тогда как в быстром сне она уменьшается или исчезает полностью.
9. Фотопароксизмальный ответ. Характеризуется появлением эпилептиформной активности, как генерализованного характера, так и регионального (преимущественно, в затылочных отделах коры головного мозга), которая появляется при предъявлении ритмической фотостимуляции различной частоты. Максимальный ответ наблюдается при частоте РФС около 16 Гц при закрытых глазах. Лучше выявляется при референтном монтаже. Фотопароксизмальный ответ может продолжаться и после окончания световой стимуляции, что характерно для фотосенситивных форм эпилепсии: первичная фотосенситивная эпилепсия, идиопатическая фотосенситивная затылочная эпилепсия, болезнь Унферрихта-Лундборга и некоторые другие.
10. Иктальные ЭЭГ паттерны. ЭЭГ приступа — внезапное изменение биоэлектрической активности, регионального или диффузного характера, ассоциированное с эпилептическим приступом. Во многих случаях для дифференциальной диагностики иктальных и межприступных эпилептиформных нарушений на ЭЭГ единственным методом является видео-ЭЭГ-мониторинг. Однако кратковременность возникновения некоторых паттернов (например, разрядов генерализованных пик-волновых комплексов, продолжительностью 1-2 сек) не всегда позволяет точно зафиксировать наличие приступа, синхронно с ним. В этих случаях ряд авторов рекомендует употреблять термин «субклинические эпилептиформные нарушения на ЭЭГ» [Binnie, 1993]. ЭЭГ паттерн приступа может возникать как генерализованно, так и регионально. Это высокоспецифичный феномен для эпилепсии, даже если он возникает без клинических симптомов. При наличии в клинике пароксизмов неясной этиологии этот паттерн доказывает эпилептическую их природу.
11. ЭЭГ статуса определяется в случае продолженных эпилептиформных паттернов ЭЭГ приступа или часто повторяющихся паттернов ЭЭГ приступа без восстановления нормального ритма фоновой записи между ними. Следует отметить, что ЭЭГ статуса может не коррелировать с клиническими симптомами эпилептического статуса. Классический тому пример — электрический эпилептический статус медленного сна; тяжелая форма эпилепсии с выраженными когнитивными нарушениями, при которой частота и выраженность эпилептических приступов может быть минимальна или приступы отсутствуют вовсе. Таким образом, даже высоко специфичные паттерны ЭЭГ приступа и ЭЭГ статуса, следует рассматривать только в контексте с клиническими данными. Особенности иктальной ЭЭГ при различных типах эпилептических приступов в рамках отдельных форм эпилепсии будут рассмотрены в следующих главах.
6. Расшифровка и заключение ЭЭГ
Таким образом мы подошли к интерпретации ЭЭГ-нарушений
Эти рекомендации не являются строгими правилами. Они относятся в первую очередь к стандартной ЭЭГ. При описании более специализированных записей (неонатальные записи, электроцеребральное молчание) представление технических деталей должно быть более полным — в соответствии со стандартами ACNS (1 — «Minimum Technical Requirements (MTR) for Performing Clinical EEG»; 2 — «Minimal Technical Standards for Pediatric Electroencephalography»; 3 — «Minimum Technical Standards for EEG Recording in Suspected Cerebral Death»).
Отчет ВЭЭГ должен состоять из 3 основных частей:
- введение,
- описание,
- интерпретация, включая
- впечатление (мнение) касательно нормальности или степени аномальности,
- корреляцию данных ЭЭГ с клинической картиной.
1. Введение.
Введение должно начинаться с описания специальной подготовки, если таковая предпринималась перед записью.
2. Описание.
Описание ЭЭГ должно включать все характеристики записи, включая нормальные и аномальные, представленные объективным способом, максимально избегая утверждений об их значимости.
Целью является полный и объективный отчет, который позволит другим ЭЭГ-специалистам придти к выводу касательно нормальности или степени аномальности записи по описанию — без необходимости просматривать исходную ЭЭГ. Этот вывод может отличаться от исходного вывода, поскольку в определенной мере субъективен.
Описание начинается с фоновой активности, доминирующей активности, ее частоты, количества (постоянная, преходящая), локализации, амплитуды, симметрии или асимметрии, является ли она ритмической или иррегулярной. Частота должна указывать в Гц или циклах в секунду. В целях стандартизации отчета рекомендуется определять амплитуду в отведениях, включающих смежные электроды по схеме 10-20. Желательно, но не обязательно, оценивать амплитуду в микровольтах. Это позволит избежать таких терминов, как «низкий», «средний» и «высокий». Недоминирующая активность — частота, количество, амплитуда, локализация, симметрия или асимметрия, ритмичность или ее недостаточность, должна описываться с использованием таких же единиц измерения, как и для доминантной активности.
Если проводились тесты — должны быть описаны реакции на открытие и закрытие глаз, а также произвольных, целенаправленных движений. Включается описание указания на симметрию или асимметрию, полноту или неполноту, устойчивость или неустойчивость.
Аномальные записи, неонатальные записи, или записи только во время сна, могут не содержать четкого доминирующего ритма. В таких случаях, должны быть описаны другие виды активности (амплитуда, частота, и пр.) в любом порядке. Если запись демонстрирует заметную межполушарную асимметрию, характеристики по каждому полушарию должны быть представлены по отдельности (доминантная, недоминантная активность).
Вслед за фоновой активностью должно идти описание нарушений, не относящихся к фоновой активности. В описание включаются: тип нарушения (спайки, острые волны, медленные волны), распространенность (диффузные, локальные), топография или локализация, симметрия, синхронность (внутри— и межполушарная), амплитуда, временные характеристики (непрерывная, периодическая, эпизодическая, или пароксизмальная) и количество аномальных паттернов. Количество нарушений описывается субъективным способом, поскольку в клинической ЭЭГ невозможно точно измерить количество или соотношение.
Если аномалия является эпизодической, необходимо обратить внимание на отсутствие или наличие периодичности между эпизодами, ритмичность или иррегулярность паттерна внутри каждого эпизода. Необходимо представить временной диапазон продолжительности эпизодов.
В описании процедур активации необходимо включать утверждение об их качестве (например, хорошая, удовлетворительная или плохая гипервентиляция, длительность сна, стадии сна, которые были достигнуты во время исследования). Надо указать тип (глиссандо, пошаговая) фотостимуляции и диапазон частот стимуляции. Описываются эффекты гипервентиляции и фотостимуляции, включая нормальные и аномальные ответы. Если гипервентиляция или фотостимуляция не проводились, необходимо указать причину. Поскольку направляющий врач предполагает, что эти процедуры используются по умолчанию, он может ожидать описания их результатов — даже в том случае, если необходимость их проведения не была указана явно в направлении.
Нет нужды указывать на отсутствие определенных характеристик, за исключением нормальных, — таких как низкоамплитудная быстрая активность, сонные веретена, и др. Такие фразы как «отсутствие фокальной патологии» или «нет эпилептиформных нарушений» могут использоваться только в разделе интерпретации — при наличии явного или предполагаемого запроса направляющего доктора. Они не должны использоваться в описательной части.
Артефакты должны описываться только в сомнительных случаях (например, сохраняется вероятность того, что они отражают церебральную активность) или, когда они носят необычный характер, мешают интерпретации записи, а также когда они обладают определенной диагностической ценностью (например, миокимии, нистагм, и др.).
3. Интерпретация.
(I) Впечатление — это субъективное мнение специалиста о степени нормальности записи. Описание записи предназначено, в первую очередь, для электроэнцефалографиста, который использует его для последующего вывода, или другого эксперта, и должно быть детальным и объективным. Впечатление, с другой стороны, пишется в первую очередь для направляющего врача, и, следовательно, должно быть по возможности сжатым. Большинство клиницистов из предшествующего опыта предполагают, что чтение детального описания не дает им существенно новой информации, и поэтому ограничиваются интерпретаций. Если оно слишком большое и выглядит иррелевантно клинической картине, клиницист может потерять интерес, что в итоге приводит в снижению пользы от всего ЭЭГ отчета. Если запись считается аномальной, желательно указывать ее степень — с целью облегчить сравнение между повторными исследованиями. Поскольку эта часть отчета носит довольно субъективный характер, степень нарушений может варьировать от лаборатории к лаборатории. Однако в каждой лаборатории следует четко определять критерии степени нарушения и строго следовать им.
После определения степени нарушений, необходимо указать причины, на основе которых строится вывод. Если присутствуют несколько видов нарушений, желательно ограничиться списком из двух или трех главных нарушений, которые наиболее характерны для данной записи. Если перечислять все нарушения, наиболее существенные «растворяются» в тексте и теряется значимость выводов. При наличии данных предыдущих ЭЭГ записей, необходимо включать их сравнение с результатами данного исследования.
(II) Клиническая корреляция — это попытка показать насколько данные ЭЭГ укладываются (или нет) в общую клиническую картину. Оно может варьировать — в зависимости от того, кому оно адресуется. Для адресата, далекого от неврологии или ЭЭГ, оно должно быть более тщательным и выверенным.
Если ЭЭГ аномальная — это указывает на церебральную дисфункцию, поскольку ЭЭГ является отражением церебральной функции. Тем не менее, фраза «церебральная дисфункция» может звучать излишне угрожающе и должна использоваться только когда нарушение квалифицируется как «более чем легкое» и когда имеется достаточно клинической информации, чтобы считать такой вывод реалистичным в данном клиническом контексте. В остальных случаях допустимы предложения типа «Запись указывает на легкую иррегулярность церебральной функции». Определенные паттерны ЭЭГ являются подтверждающими для более или менее специфических клинических ситуаций; дельта фокус может говорить о структурном поражении в соответствующем клиническом контексте; определенные типы спайков или острых волн подтверждают потенциальный эпилептогенез. Если нарушение ЭЭГ соответствует клинической информации, которая содержит диагноз или подозрение на наличие подобного состояния, можно указать, что данные ЭЭГ согласуются или подтверждают диагноз.
Цифровые способы записи, генерации и передачи отчета позволяют, при необходимости, включать в отчет короткие отрезки реальной записи, в том числе с примерами нарушений.
7. ВЭЭГ-мониторинг в оценке эффективности противосудорожной терапии
Одним из основных критериев объективизации действия противоэпилептических препаратов является изменение биоэлектрической активности мозга, регистрируемое с помощью ЭЭГ.
Эти изменения носят различный характер и зависят от формы эпилепсии и применяемой терапии.
Помимо воздействия антиконвульсантов на эпилептическую активность, они также оказывают влияние на характер фоновой ритмической активности. Хорошо описаны изменения фоновой ритмики, появляющиеся при длительном приеме бензодиазепинов и барбитуратов.
При прогрессирующем течении заболевания отмечается нарастание индекса эпилептической активности в очаге.
Другим маркером отрицательной динамики является появление дополнительных очагов эпилептической активности. Они могут быть зависимы от первичного очага или существовать независимо.
К характеристикам проградиентного течения заболевания относится появление феномена вторичной билатеральной синхронизации (ВБС).
К ЭЭГ-критериям, отражающим положительное влияние ПЭП, относятся: снижение индекса пароксизмальности в очаге, уменьшение количества эпилептических очагов и регресс эффекта ВБС.
Динамические ВЭЭГ-исследования в период отмены терапии с высокой точностью позволяют оценить риск возобновления приступов.
8. Эффективность ЭЭГ-мониторинга
Была проанализирована достоверность направляющего диагноза «Эпилепсия» у первичных пациентов, поступающих в эпилептологический стационар (НПЦ медицинской помощи детям, ДЗ Москвы).
Исследуемая группа составила 1154 пациента в возрасте от 0 до 18 лет. Всем пациентам проводились следующие методы обследования: оценка нервно-психического статуса, видео-ЭЭГ-мониторинг продолжительностью 6 и более часов, и, в большинстве случаев, МРТ головного мозга.
Результаты: Диагноз «эпилепсия» был достоверно подтвержден у 643 пациентов (56%); у 240 (20,8%) пациентов не было получено электроэнцефалографических паттернов эпилепсии, но диагноз оставлен в прежнем виде с учетом данных анамнеза и других методов обследования; у 133 пациентов (11,5%) диагноз «эпилепсия» был снят; у 46 (4%) пациентов диагностированы парасомнии; у 39 (3,4%) — псевдоэпилептические (психогенные) приступы; у 8 (0.7%) — тики; в группу пациентов из 45 (3,9%) человек вошли дети с аффект-респираторными пароксизмами, синдромом Туретта, синкопальными состояниями, хореоатетозом/дистонией, мигренью, аутизмом, синдромом Мюнхаузена, мастурбацией.
Таким образом, у 23,2% (267) пациентов диагноз «эпилепсия» был исключен. Наиболее частыми пароксизмальными состояниями, мимикрирующими эпилепсию являлись парасомнии и психогенные приступы. Нельзя также забывать о большой группе (11,5% — 133 пациента) абсолютно здоровых детей, ошибочная постановка диагноза «эпилепсия» у которых, в большинстве случаев, была связана с неверной трактовкой поведенческих реакций, характерных для того или иного возраста. В подавляющем большинстве этих случаев причины гипердиагностики эпилепсии заключались в недостаточно полном и точном сборе анамнеза, неправильной трактовке результатов ЭЭГ, а в ряде случаев в психологическом давлении родственников пациента на врача.
9. Заключение
Успешное лечение эпилепсии напрямую зависит от своевременно и правильно установленного диагноза. Использование неинформативных методов диагностики на стартовом этапе лечения эпилепсии приводит к трудностям в подборе адекватной терапии, прогрессированию заболевания. В ЭЭГ это проявляется в виде появления множественных вторичных очагов эпилептической активности, развитию феномена вторичной билатеральной синхронизации при фокальных формах и значительному нарастанию индекса генерализованных разрядов при генерализованных формах эпилепсии.
Нередко наличие у пациента эпилептических приступов, несмотря на их очевидную курабельность, побуждает врача необоснованно вводить социальные ограничения, применять полипрагмазию в лечении.
С другой стороны, необоснованная констатация ремиссии у пациентов с эпилепсией также имеет неблагоприятные для пациента последствия, поскольку сохраняются клинически «невидимые» виды приступов или эпилептиформная активность на ЭЭГ.
Отсутствие изменений в записанном фрагменте ЭЭГ бодрствования длительностью до 30 мин (рекомендации ILAE) может создать ложное впечатление о положительной динамике на фоне лечения. Опираясь на полученные данные, врач может ошибочно констатировать клинико-энцефалографическую ремиссию. С другой стороны, выявление эпилептической активности на контрольной динамической ЭЭГ на фоне подобранной терапии может содержать фрагмент эпилептической активности, которую врач ошибочно трактует как «отрицательную динамику». В некоторых случаях на коротких фрагментах записи ЭЭГ-характеристики могут выглядеть как «нормальные» при сохраняющихся приступах. При этом объективный анализ продолженной записи свидетельствует, что характер биоэлектрической активности у пациента значимо не менялся. Ошибки при интерпретации связаны с чередованием нормальных и патологических фрагментов ЭЭГ.
Можно утверждать, что объективная трактовка изменений ЭЭГ может проводиться только при проведении ВЭЭГ-мониторинга.
Введение в алгоритм диагностики и динамического обследования ВЭЭГ-мониторинга позволяет, используя объективные клинико-нейрофизиологические критерии, своевременно диагностировать заболевание, оценивать состояние больного на разных этапах лечения, оптимизировать терапевтическую тактику и избегать диагностических ошибок у пациентов с эпилепсиями и эпилептическими синдромами.
Анализ длительного катамнеза больных эпилепсией (взрослых и детей) позволил разработать и внедрить в специализированных отделениях и кабинетах высокодостоверный комплексный клинико-нейрофизиологический подход к дифференциальной диагностике эпилепсий и судорожных синдромов, значительно повысить качество проводимой терапии в этой сложной группе пациентов.
Врач-педиатр, врач высшей категории,
невролог Тамбиев И. Е..
Ковалев И. Г.
Жу/РсНкДиЛй ДЕТСКОЙ Д 2
НЕВРОЛОГИИ ТОМ IX Tt S
Анализ основных причин ошибочной диагностики эпилептических приступов и эпилептических синдромов (клинические особенности
эпилептических приступов)
М.Б. Миронов
ООО «Институт детской неврологии и эпилепсии им. Святителя Луки», Россия, 143396, Москва, Троицк, п. Пучково, ул. Светлая, 6
Контакты: Михаил Борисович Миронов mironovmb@mail.ru
Эпилепсия — хроническое заболевание головного мозга, требующее длительной терапии и постоянного тщательного контроля над состоянием пациента. В связи с этим крайне опасны как гипердиагностика данного заболевания, так и гиподиагностика. Гипердиагностика ведет к необоснованному социальному «клейму», ограничению в правах, значительному снижению качества жизни пациента, проблемам в семье, назначению длительной антиэпилептической терапии, которая может приводить к возможным побочным эффектам. Гиподиагностика эпилепсии нередко приводит к дальнейшей резистентности приступов к лечению, их учащению, вероятности развития эпилептического статуса, жизнеугрожающих ситуаций, возможности развития когнитивных нарушений, связанных с заболеванием. Значительный прогресс в эпилептологии и медицинских технологиях (видеоэлектроэнцефалографический (ЭЭГ) мониторинг, методы нейровизуализации, генетические исследования), который был отмечен в последние десятилетия, позволил минимизировать ошибки лечащих врачей. Несмотря на это, и в настоящее время остаются сложности в диагностике эпилепсии.
По мнению автора, существует круг эпилептических приступов, визуальная оценка которых крайне затруднена и без проведения видео-ЭЭГ-мониторинга практически невозможна. К таким сложно диагностируемым приступам могут быть отнесены короткие, фантомные, атипичные абсансы, абсансы во вне, эпилептический миоклонус век с абсансами или без, миоклонические, тонические, геластические, фокальные гипермоторные приступы, эпилептические ауры, фокальные версивные приступы, эпилептические спазмы, иктальные синкопы, негативный миоклонус, фокальный эпилептический миоклонус, эпилептические приступы, возникающие при закрывании глаз, и самоиндуцированные пациентами приступы.
Автор подробно рассматривает каждый из этих видов эпилептических приступов, делая акцент на их диагностических критериях и характеристиках клинико-ЭЭГ-картины, которые наиболее важны при проведении дифференциальной диагностики. Собственный опыт автора и данные литературы показывают, что окончательную трактовку пароксизмальных состояний в целях минимизации диагностических ошибок следует проводить после проведения видео-ЭЭГ-мониторинга.
Ключевые слова: эпилепсия, эпилептические приступы, диагностика, дифференциальный диагноз, видеоэлектроэнцефалографи-ческий мониторинг, абсанс, фантомный абсанс, атипичный абсанс, абсансы во сне, эпилептический миоклонус век с абсансами или без, миоклонические приступы, эпилептическая аура, тонические приступы, геластические приступы, фокальные гипермоторные приступы, эпилептические спазмы, фокальные версивные приступы, иктальные синкопы, негативный миоклонус, фокальный эпилептический миоклонус
ANALYSIS OF MAIN REASONS FOR MISTAKES IN DIAGNOSTICS OF EPILEPTIC SEIZURES AND EPILEPTIC SYNDROMES (CLINICAL PECULIARITIES OF EPILEPTIC SEIZURES)
M.B. Mironov
Svt. Luka’s Institute of Child Neurology and Epilepsy, 6 Svetlaya St., Puchkovo Settlement, Troitsk, Moscow, 143396, Russia
CO
Epilepsy is a chronic brain disease that requires long therapy and continuous careful supervision of the status of the patient. In connection with this, both overdiagnosis and underdiagnosis of this disease is extremely dangerous. Overdiagnosis causes ungrounded social «label», limitation in rights, significant decreasing quality of life of the patient, family problems, prescription of long-term anti-epileptic therapy that may cause potential side effects. Underdiagnosis of epilepsy frequently causes further resistance of seizures to therapy, they become more frequent, there appears the possibility of development of epileptic status, life threatening situations, possibility of development of cognitive disorders associated with the disease. A significant progress in epileptology and medical technologies (video electroencephalographs (EEG) monitoring, neuroimag-ing methods, genetic studies) that has been marked in recent decades has allowed minimizing errors of physicians. Despite this, certain difficulties still remain in diagnostics of epilepsy.
In the author’s opinion, there is a range of epileptic seizures visual assessment of which is extremely difficult and is literally impossible without video EEG monitoring. Short, phantom, atypical absences, absences on the outside, epileptic myoclonus of the eyelids with or without absences, myoclonic, tonic, gelastic, focal hyperkinetic seizures, epileptic aura, reversingfocalseizures, epileptic spasms, ictalsyncopes, negative myoclonus, focal epileptic myoclonus, epileptic seizures arising when closing the eyes, and self-induced seizures can be attributed to such seizures with difficulties in diagnosis.
The author reviews each of these types epileptic seizures in details focusing the attention on their diagnostic criteria and characteristics of the clinical and the EEF features that are of utmost importance in the course of performance of differential diagnostics.
Own experience of the author and data of literature show that one should perform final interpretation of paroxysmal states only after video EEG monitoring for the purpose of minimizing diagnostic errors.
Key words: epilepsy, seizures, diagnosis, differential diagnosis, video electroencephalographs monitoring, absence, phantom absence, atypical absence, absences during sleep, epileptic myoclonus of the eyelids with or without absences, myoclonic seizures, epileptic aura, tonic seizures, gelastic seizures, focal hyperkinetic seizures, epileptic spasms, versive focal seizures, ictal syncope, negative myoclonus, focal epileptic myoclonus
4
о
ТОМ IX JL <N
Эпилепсия — хроническое заболевание головного мозга, требующее длительной терапии и постоянного тщательного контроля над состоянием пациента. В связи с этим крайне опасны как гипердиагностика данного заболевания, так и гиподиагностика. Гипердиагностика ведет к необоснованному социальному «клейму», ограничению в правах, значительному снижению качества жизни пациента, проблемам в семье, назначению длительной антиэпилептической терапии, которая может приводить к возможным побочным эффектам. Гиподиагностика эпилепсии нередко приводит к дальнейшей резистентности приступов к лечению, их учащению, вероятности развития эпилептического статуса, жизнеугрожающих ситуаций, возможности развития когнитивных нарушений, связанных с заболеванием. Значительный прогресс в эпилептологии и медицинских технологиях (видеоэлек-троэнцефалографический (ЭЭГ) мониторинг, методы нейровизуализации, генетические исследования), который был отмечен в последние десятилетия, позволил минимизировать ошибки лечащих врачей. Несмотря на это, и в настоящее время остаются сложности диагностики эпилепсии.
Наш опыт показывает, что существует круг эпилептических приступов, визуальная оценка которых крайне затруднена, а подчас без проведения видео-ЭЭГ-мониторинга практически невозможна. Сложность диагностики отдельных видов приступов неоднократно обсуждалась в научной литературе. К таким сложно диагностируемым приступам могут быть отнесены нижеперечисленные виды.
Короткие абсансы
Проблема обнаружения коротких абсансов заключается в том, что факт выключения сознания достаточно сложно определить ввиду кратковременности (продолжительность приступа не более 2—5 с), и внешне данные приступы могут практически не отличаться от повседневной двигательной активности пациента [22]. Клинически абсансы, возникающие в период коротких генерализованных билатерально-синхронных разрядов комплексов пик—волна, поли-пик—волна на ЭЭГ, могут проявляться незначительными запинками в речи, едва заметным заведением
глазных яблок вверх, подергиванием бровей, ресниц. При этом выявление изменения уровня сознания (основного критерия абсансного приступа) возможно, как правило, лишь при длительном непрерывном разговоре, чтении или счете пациента, что следует помнить при тестировании больного в ходе видео-ЭЭГ-мониторинга [2, 7, 9].
Фантомные абсансы
Термин «фантомные абсансы» предложен R. Ferner и C.P. Panayiotopoulos в 1993 г. и обозначает типичные абсансы, протекающие незаметно для пациента и/или для окружающих [33]. Наш опыт показывает, что остановка движения и изменение сознания при данном типе приступов могут выявляться лишь в первые несколько секунд после начала абсан-са. Вслед за этим пациент, как правило, выполняет простые инструкции на фоне продолжающегося разряда генерализованной пик-волновой активности на ЭЭГ, однако в этот момент больной может переживать ощущения, обычно с трудом им дифференцируемые. Клинически в период приступа пациент может приостановить начатую деятельность, возможна незначительная гипомимия лицевой мускулатуры с мио-клоническим компонентом или без него в периорби-тальной мускулатуре, в момент разговора могут отмечаться запинки, повторение отдельных слов, прекращение речи [22].
Атипичные абсансы
Атипичные абсансы проявляются, как правило, постепенным снижением уровня сознания (в отличие от типичных абсансов), приостановлением двигательной активности пациентов, общей заторможенностью [53]. Сознание пациентов в период приступа нередко флюктуирует, может появляться слюнотечение. Данный тип приступов может сопровождаться атоническим компонентом, который проявляется в виде кивков, опускания плеч, наклонов туловища, каскадных падений. Реже выявляется миоклонический компонент (подергивание конечностей и лицевой мускулатуры, кивки) и автоматизмы [7, 9, 22]. Следует учитывать сложность регистрации атипичных абсансов, так как у детей с данным типом приступов нередко сни-
Е га Е
жен интеллект [47]. При отсутствии контакта с пациентом возникает необходимость в создании ситуаций, при которых будет установлен факт снижения уровня сознания. В нашей лаборатории мы добиваемся этого путем игры пациента с родителями или медицинским персоналом. В период игры в пользу атипичного аб-санса будет свидетельствовать прекращение начатой деятельности, замирание, гипомимия, остановка взора, появившиеся на фоне диффузного пик-волнового разряда на ЭЭГ [7, 9]. В целях выявления атонического компонента в структуре приступа пациенты должны тестироваться в пробе Баре. У детей данную пробу можно провести в виде игры с передачей игрушек в руки пациента. Также важна проба с длительным ортостатическим положением пациента и сменой положения с вертикального на горизонтальное. Это позволяет выявить скрытый, не заметный в лежачем положении атонический компонент, а также дифференцировать негативный миоклонус от миоклониче-ского компонента.
Абсансы во сне
Абсансные приступы могут возникать не только в состоянии бодрствования, но и во сне [12, 44, 55]. Впервые на эту особенность обратил внимание E. Niedermeyer в 1965 г.: «Мы обследовали 91 пациента с клиническими и ЭЭГ-признаками petit mal epilepsy, у которых было проведено ЭЭГ-исследование как в бодрствовании, так и во сне. ЭЭГ характеризовалась наличием четких устойчивых билатерально-синхронных пик-волновых разрядов частотой 2,5—3,5 в секунду. Во время записи ЭЭГ у 50 больных были зарегистрированы приступы типичных абсансов» [44]. В обсуждении полученных результатов автор отмечает, что клинические признаки абсансов во сне и бодрствовании не отличались друг от друга: «Сопутствующие приступам симптомы были одинаковыми во сне и бодрствовании; это касалось и глазных признаков, главным образом подергивания век. Уровень сознания во время приступов определить было трудно».
В ходе нашего исследования, проведенного в 2008 г., у всех пациентов с абсансными формами эпилепсии во сне выявлены ЭЭГ-паттерны абсансов [12]. Генерализованные билатерально-синхронные разряды коррелировали с клиническими проявлениями в виде миоклонуса век, периназального миоклонуса, ритмичного приоткрывания глаз. Таким образом, нами зарегистрированы эпилептические приступы во сне, проявляющиеся миоклонусом век, ритмичным приоткрыванием глаз, периназальным миоклонусом и имеющие ЭЭГ-изменения, характерные для абсансов. Основной проблемой в дефинитивной трактовке описанных выше приступов является отсутствие возможности тестировать уровень сознания во сне. Мы имеем все клинико-ЭЭГ-характеристики абсансных
приступов, за исключением самой главной — констатации факта снижения уровня сознания во время приступа. Мы предложили называть данный подтип приступов абсансами во сне [12]. Во-первых, имеется клинико-ЭЭГ-коррелят сложных типичных абсансов, а во вторых, подчеркивается невозможность адекватного тестирования сознания во сне. Выделение нового подтипа приступов — абсансы во сне — важно для контроля эффективности лечения эпилепсии. Интересен тот факт, что ни в одном случае пациенты, родители и лечащие врачи не отмечали абсансы у пациентов во сне. Все ночные приступы были впервые выявлены в ходе видео-ЭЭГ-мониторинга. Нереги-стрируемые приступы, как известно, являются фактором риска рецидивов эпилепсии и приводят к ложному впечатлению о мнимом благополучии — феномену псевдоремиссии.
Эпилептический миоклонус век с абсансами или без
Эпилептический миоклонус век с абсансами или без — эпилептические приступы, проявляющиеся прикрыванием глаз и частыми (3—6 раз в секунду) ритмическими миоклониями век (трепетание век) [50]. Могут сопровождаться короткими абсансами или протекают без потери сознания. В проекте Международной классификации эпилептических приступов эпилептический миоклонус век включен в группу абсансных приступов со специальными проявлениями [26]. Проблема диагностики данных приступов возникает вследствие их кратковременности и, как правило, отсутствия признаков снижения уровня сознания [5]. Следует отметить, что родители и окружающие далеко не всегда замечают эпилептический миоклонус век, и в 64,7 % случаев этот вид приступов впервые был выявлен при проведении видео-ЭЭГ-мониторинга, вне зависимости от наличия или отсутствия других типов приступов в этот период [8]. Эпилептический миоклонус век внешне напоминает манерность или тики. Наше исследование показало, что у всех пациентов кроме приступов эпилептического миокло-нуса век выявляются также навязчивые движения глаз, которые клинически внешне идентичны приступам, что дополнительно затрудняет правильную оценку состояния пациента [8].
Миоклонические приступы
Миоклонические приступы (эпилептический миоклонус) характеризуются внезапными, короткими, как правило, билатеральными и синхронными подергиваниями мышц [28]. Миоклонические приступы могут захватывать мышцы шеи, плеч, рук или ног. В большинстве случаев в приступ вовлекаются мышцы плечевого пояса и рук. При эпилептическом миокло-нусе движение чаще идет вверх, чем вниз. Падения в момент миоклонического приступа не характерны,
ГН
о (N
но возможны, если пациент долго находился вертикально, стоя в неудобной позе. Важной характеристикой, отличающей эпилептический миоклонус от других генерализованных типов приступов, является сохранное сознание в момент приступа [22].
Кинематические проявления миоклонического приступа напоминают таковые при гиперкинезах неэпилептической природы (например, при генерализованных тиках, стартл-рефлексе, гиперэксплексии, сильном испуге, синдроме Феджермана) [13, 22]. Особую сложность представляет выявление эпилептического миоклонуса во сне. В большинстве случаев не удается на основании анамнеза и даже при визуальном контроле дифференцировать эпилептический приступ от парасомний (доброкачественный миокло-нус сна, парциальные пробуждения).
Тонические приступы
Тонические эпилептические приступы проявляются устойчивым мышечным сокращением одной или нескольких мышечных групп, результатом которого является тоническая установка конечности или всего тела; их продолжительность обычно более 3 с [42, 43].
Тонические приступы могут протекать с минимальным моторным компонентом и/или коротким замиранием. При этом моторный компонент проявляется в виде короткого замирания с кратковременным по длительности расширением зрачков, едва заметным заведением глазных яблок вверх и/или в сторону, незначительным по выраженности тоническим приподниманием плеч (возможно с минимальным приподниманием рук в локтевых суставах) и/или характерным едва заметным тоническим насильственным наклоном головы вперед и вниз с изменением мимики: приподнимание век (вид удивленного человека) с легким заведением глазных яблок вверх [21, 22]. Следует отметить, что минимальный тонический компонент (в тех или иных проявлениях) в случае малых моторных приступов отмечается в большинстве наблюдений. Еще в 70-х годах прошлого столетия великие эпилептологи H. Gastaut (1970), J. Bancaud et al. (1981) отметили, что тонические приступы могут выглядеть клинически как диа-лептические (в виде замираний) [38, 53]. В Проектах классификаций эпилептических приступов (1970, 1981) к группе атипичных абсансов были отнесены не только классические атипичные абсансы, сопровождающиеся по их описанию более или менее ритмичными разрядами комплексов острая—медленная волна, но и приступы, имеющие на ЭЭГ паттерн в виде появления низкоамплитудной быстроволновой активности (fast activity) частотой 10 Гц и более. При описании тонических приступов авторы указали тот же ЭЭГ-паттерн. То есть под термином «абсанс»
описаны приступы, имеющие клинические характеристики диалептических приступов и ЭЭГ-паттерн тонических приступов.
Клинические проявления тонических приступов могут быть похожи на другие пароксизмальные состояния неэпилептического генеза. Например, дистони-ческие атаки или аноксические приступы с тоническим компонентом.
Эпилептическая аура
Эпилептическая аура — эпилептический приступ, сопровождающийся субъективными ощущениями пациента. В настоящее время в классификации Международной антиэпилептической лиги (ILAE) предложен синоним — фокальный сенсорный приступ (ФСП) [31]. ФСП нередко предшествует началу моторного приступа.
Возникновение иктального ощущения чаще протекает на фоне сохранного сознания. Однако в период переживания сложных психических аур пациент может утрачивать связь с окружающим. Несмотря на возможное отсутствие реакции на внешние раздражители в этот период, у пациента, как правило, остается память на переживаемые ощущения. ФСП проявляются в виде появления внутренних ощущений пациента, которые не заметны окружающим, и могут расцениваться больным долгое время как обыкновенные, неэпилептические [17]. В связи с этим следует отметить, что термины «эпилептическая аура» или «фокальный сенсорный приступ» правомерны только в случае документального подтверждения: выявления эпилепти-формных изменений на ЭЭГ синхронно с внезапно возникшими ощущениями пациента или в случаях, когда аура входит в структуру диалептического или моторного приступа [42].
Геластические приступы
Геластические приступы (ГП) (от греч. gelos — смех) — фокальные эпилептические приступы, проявляющиеся внезапными эпизодами насильственного смеха [30].
В 1971 г. G.G. Gascon и C.T. Lombroso сформулировали критерии ГП [37]:
1) повторение стереотипных приступов в виде улыбки или смеха;
2) отсутствие внешних провоцирующих факторов;
3) сочетание с другими проявлениями эпилепсии;
4) наличие межприступной эпилептиформной активности на ЭЭГ;
5) отсутствие других состояний, при которых мог бы отмечаться патологический смех.
Наше исследование, завершенное в 2014 г., показало, что могут возникать значительные сложности выявления ГП [6]. Нередки случаи гиподиагностики. Эпилептические пароксизмы смеха длительное время
т а т
Е га Е
могут не обращать на себя внимания как со стороны близких, так и со стороны врачей и расцениваться как поведенческие реакции. Но также возможны случаи гипердиагностики. В связи с этим крайне важно помнить критерии ГП.
Гипермоторные приступы
Фокальные эпилептические приступы с гиперкинетическими автоматизмами (ФПГА) (фокальные приступы с гипермоторными автоматизмами, фокальные гипермоторные приступы) — приступы, исходящие обычно из лобной или височной долей, характеризующиеся чрезмерными движениями, локализованными в основном в проксимальных отделах конечностей и в области туловища (по типу боксирования, педалирования, тазовых движений и т. д.) и возникающие чаще во время сна [43]. Большинство авторов отмечают хронологическую приуроченность ФПГА ко сну. Возникновение приступов в ночное время — важный критерий ФПГА. Чаще они появляются при засыпании или перед пробуждением, но могут быть и в течение всей ночи. У некоторых пациентов пароксизмы наблюдаются в строго определенное время ночи (чаще во II стадию фазы медленного сна), что сближает их с пара-сомниями. Значительно реже приступы констатируются во время дневного сна, и лишь около 10 % больных имеют приступы в период бодрствования [57]. По результатам нашего исследования, ФПГА в 57,9 % случаях отмечались только во сне, у 42,1 % пациентов приступы возникали как во сне, так и в бодрствовании. Исключительно в состоянии бодрствования гипермоторные приступы не наблюдались ни в одном случае [15]. Гипермоторные приступы имеют кинематическое сходство с парасом-ниями и не ассоциируются, как правило, в обществе с эпилепсией.
Эпилептические спазмы
Эпилептические спазмы (ЭС) — приступы с внезапным сгибанием, разгибанием или смешанного сги-бательно-разгибательного типа, вовлекающие преимущественно проксимальную и туловищную мускулатуру, которые обычно более длительные, чем миоклонические, но более короткие, чем тонические приступы; длятся около 1 с. Могут встречаться изолированные формы: гримасы, кивки. ЭС часто возникают серийно [28].
Клинические проявления ЭС могут варьировать и зависят от преимущественного вовлечения в приступ флексорной или экстензорной мускулатуры, а также от степени вовлечения различных групп мышц [16, 25]. Вид спазмов может меняться у одного и того же пациента: от массивных сокращений, вовлекающих в приступ большие группы мышц, до едва заметных
кивков, захватывающих только мышцы шеи или брюшной мускулатуры.
Долгое время ЭС могут оставаться незамеченными или расцениваться как кишечные колики. Дифференцированный диагноз необходимо проводить с мио-клоническими приступами и рядом сходных по кинематике неэпилептических пароксизмальных состояний: пароксизмальными дискинезиями, синдромом Сандифера, пароксизмальной кривошеей, пароксизмальным хореоатетозом, медикаментозной интоксикацией, неонатальным феноменом jitteriness, spasmus nutans, эссенциальным тремором, доброкачественным неонатальным миоклонусом сна, гиперэкс-плексией, синдромом Феджермана, тоническими поз-ными феноменами в рамках стартл-рефлекса [13].
Следует отметить, что на фоне положительного эффекта антиэпилептической терапии клинические проявления эпилептических спазмов могут становиться минимальными и нередко наблюдается их трансформация в фокальные версивные приступы [10].
Фокальные версивные приступы
Версивные приступы характеризуются девиацией глаз латерально. В большинстве случаев наблюдается версия головы и часто также туловища в момент, когда глаза достигли крайнего бокового положения. По выражению Ханса Отто Людерса: «как будто глаза «тянут» голову» [43]. Начальное латеральное отведение глаз может быть тоническим или с клоническим компонентом [42, 52]. Не все движения головой в сторону и не каждое отведение взгляда в сторону могут быть отнесены к версивным приступам. Только длительные, чрезмерные и неестественные отведения головы лате-рально (обычно движение головой совершается не только в сторону, но также и вверх) могут быть классифицированы как версивные приступы [42]. Версивные приступы возникают при раздражении лобной или затылочной коры и при этом сходны по клиническим проявлениям. Из дополнительных симптомов, которые могут помочь дифференцировать долевую принадлежность версивных приступов, можно выделить следующие: более быстрое возможное вовлечение в приступ мускулатуры конечностей и лица при раздражении лобной доли (за счет близости представительства моторной коры) и нередкое начало приступа с визуальной ауры при затылочной локализации эпилептогенного очага [10].
В большинстве случаев версивные приступы долгое время не замечаются близкими пациента и могут быть неправильно расценены как нистагм, дистонические феномены глазодвигательной мускулатуры и т. д. [1].
Иктальные синкопы
Клиническая картина данного вида эпилептических приступов напоминает клиническую картину
ГН
о сч
синкопальных состояний. Различают иктальные (ау-тономные) синкопы (ИС), исходящие из височной и затылочной областей. При височных синкопах в ряде случаев приступы могут начинаться с ауры (головокружение, тревога); иногда пациенты успевают принять сидячее положение и приготовиться. Обычно ИС предшествуют аутомоторные приступы; редко они могут возникать изолированно. Характерно относительно медленное выключение сознания с последующим «обмяканием» и падением (нерезкое падение). Возможно легкое тоническое напряжение мышц конечностей, лицевой мускулатуры; появление ороали-ментарных или жестовых автоматизмов [24, 32, 41].
На основании результатов нашего исследования мы предложили критерии фокальных аутомоторных приступов с атоническим компонентом, исходящих из височной доли [18]:
1) приступы состоят из нескольких фаз: начальная диалептическая, атоническая, фаза автоматизмов, тоническая; при этом атония никогда не является инициирующей фазой приступа;
2) приступы не сопровождаются резким падением, отмечается медленное «обмякание», не приводящее к травматизации пациентов;
3) приступы сопровождаются снижением уровня сознания или его полным выключением; в большинстве случаев сознание флюктуирует;
4) ЭЭГ-паттерн фокальных аутомоторных приступов с атоническим компонентом представлен ритмической региональной медленноволновой или пик-волновой активностью в височной области с дальнейшим диффузным распространением разрядов, но с сохранением амплитудного преобладания в височной области.
ИС, исходящие из затылочной коры, впервые описаны С.Р. Рапаую1орои1о$ (1989) при идиопатической затылочной эпилепсии [48, 49]. Автор указал на возможность возникновения приступов «обмякания» у 20 % больных с ранней формой идиопатической затылочной эпилепсии, что позже было подтверждено в других исследованиях [34, 35, 46]. Клиническая характеристика иктальных проявлений свидетельствует о том, что синкопы при синдроме Панайотопулоса, так же как и височные синкопы, сопровождаются атонией мышц, которую сам автор называл феноменом «тряпичной куклы» [46, 48]. Синкопы при синдроме Панайотопулоса представляют собой внезапную или постепенную потерю сознания, «обмякание» и падение [36]. Степень нарушения сознания может варьировать от частичной утраты до полного отсутствия [51]. Перед началом приступа дети могут жаловаться на тошноту, головокружение, испытывать беспокойство, страх, однако приступ может начаться внезапно без какой-либо ауры и предвестников. Иктальные проявления затылочных синкопов могут быть как изо-
лированными, так и сочетаться с другими симптомами: адверсия глаз и головы, различные вегетативные нарушения (тошнота, рвота, головная боль), судороги, в том числе и гемиконвульсивные [45, 48].
По нашему опыту, долгое время указанный тип приступов расценивается в рамках неэпилептических обмороков (синкопов).
Негативный миоклонус
Эпилептический негативный миоклонус (ЭНМ) — один из редких типов эпилептических приступов у детей. Определяется как внезапное резкое прерывание тонической мышечной активности, совпадающее по времени с эпилептиформными разрядами на ЭЭГ без предшествующего миоклонического компонента [39, 40, 56].
Основной клинической особенностью ЭНМ является внезапная мышечная атония по градиенту силы тяжести. ЭНМ может проявляться в виде выпадения предметов из рук, подергивания конечностей, что приводит к затруднениям письма или ходьбы; пассивных кивков; ритмичных ступенчатых приседаний; приступов внезапных падений [23, 29]. Клинические проявления могут быть как унилатеральными, так и билатеральными [56].
Клинические проявления ЭНМ могут значительно варьировать даже у одного пациента: кивки головой, легкие наклоны головы к плечу, короткие пассивные пропульсивные движения верхней части корпуса (поклоны) или падения вперед, ретропульсивные отклонения корпуса или падение назад из положения сидя, внезапное падение ребенка из положения стоя. Помимо типичных клинических проявлений ЭНМ могут наблюдаться весьма необычные симптомы. Нередка ситуация, когда ЭНМ захватывает только периорби-тальную мускулатуру, что клинически проявляется в виде эпизодов полуптоза [11, 20].
Фокальный эпилептический миоклонус
Фокальный эпилептический миоклонус (ФЭМ) — спонтанные регулярные или нерегулярные мышечные подергивания, затрагивающие ограниченную часть тела, иногда усугубляющиеся движением или сенсорными стимулами, возникающие в течение минимум 1 ч и периодически с интервалом не более 10 с [27]. ФЭМ, как правило, ограничен одной частью тела, подергивания повторяются регулярно или нерегулярно без утраты сознания. ФЭМ сохраняется в течение нескольких дней или недель непрерывно или с перерывами, локализуется в одной группе мышц, но может распространяться на соседние мышечные группы с развитием статуса вторично-генерализованных судорожных приступов. В связи с продолженным характером течения данного типа приступов многие авторы считают, что ФЭМ
т а т
является редким вариантом фокального эпилептического статуса [27, 39, 40, 54]. ФЭМ отмечается при резистентных (нередко прогрессирующих) формах эпилепсии [3].
В большинстве случаев и родители, и неврологи, как правило, не обращают внимания на данный тип приступов, расценивая данные пароксизмы как неэпилептические (тики) [4, 14, 19].
Эпилептические приступы, возникающие при закрывании глаз
Принципиально важно отметить, что имеются в виду не моргательные движения век, а прикрывание глаз на более длительное время. В англоязычной литературе данный феномен известен как еуе closure related spike and wave discharges и описан в основном при идиопатической генерализованной эпилепсии [47]. В нашем исследовании среди приступов этого типа встречались типичные абсансы, миоклониче-ские приступы в виде миоклонуса верхних конечностей и эпилептического миоклонуса век [8]. Эти приступы часто остаются нераспознанными, так как в обычной жизни длительное закрывание глаз чаще всего происходит в состоянии расслабленного бодрствования, дремы или ночью перед засыпанием. В связи с этим контроль сознания в момент парок-
iНе можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
сизма со стороны окружающих затруднен, а двигательные проявления приступа отсутствуют или минимальны, например, в виде едва заметных миоклонических подергиваний век.
Группа приступов, самоиндуцируемых пациентом путем выполнения различных манипуляций
Пациенты при этом могут получать необъяснимое удовольствие. Описываются различные способы ауто-индукции: путем прикрывания глаз и заведением глазных яблок вверх с ритмичными подергиваниями век, различные манипуляции, вызывающие ритмический свет, рассматривание определенных цветовых паттернов и др. Проблема диагностики данных изменений заключается в том, что в этой группе пациентов желание получить удовольствие часто перерастает в навязчивость. При этом даже в случае медикаментозного купирования приступов у пациентов, как правило, сохраняются привычные попытки безуспешной самоиндукции, что затрудняет визуальный контроль приступов.
Наш опыт и данные других авторов показывают, что окончательную трактовку пароксизмальных состояний в целях минимизации диагностических ошибок следует проводить после проведения видео-ЭЭГ-мо-ниторинга.
ЛИТЕРАТУРА
т а т
1. Бобылова М.Ю., Миронов М.Б., Мухин К.Ю., Петрухин А.С. Глазодвигательные нарушения у детей. Журнал неврологии и психиатрии им. С.С. Корсакова 2014;1:81— 92. [Bobylova M.Yu., Mironov M.B., Mukhin K.Yu., Petrukhin A.S. Oculomotor disorders of children. S.S. Korsakov Journal of Neurology and Psychiatrics 2014;1:81-92. (In Russ.)].
2. Карлов В.А., Гнездицкий В.В. Абсансная эпилепсия у детей и взрослых. М.: Прес-сервис, 2005. 63 с. [Karlov V.A., Gnezditskiy V.V. Absence epilepsy of children and adults. Moscow: Presservice, 2005. 63 p. (In Russ.)].
3. Кваскова Н.Е., Мухин К.Ю., Миронов М.Б. Фокальный эпилептический миоклонус: дифференциальный диагноз и прогноз. Русский журнал детской неврологии 2014;9(3):6-12. [Kvaskova N.E., Mukhin K.Yu., Mironov M.B. Focal epileptic myoclonus: differential diagnosis and forecast. Russian Journal of Child Neurology 2014;9(3):6-12. (In Russ.)].
4. Котов А.С., Рудакова И.Г., Мухин К.Ю. и др. Энцефалит Расмуссена. Описание двух клинических случаев. Русский журнал детской неврологии 2009;4(2):42-50.
[Kotov A.S., Rudakova I.G., Mukhin K.Yu. et al. Rasmussen’s encephalitis. Two clinical case reports. Russian Journal of Child Neurology 2009;4(2):42-50. (In Russ.)].
5. Миронов М.Б. Эпилептический миоклонус век (лекция). Русский журнал детской неврологии 2010;5(4):29-38. [Mironov M.B. Epileptic myoclonus of the eyelids (lecture). Russian Journal of Child Neurology 2010;5(4):29-38. (In Russ.)].
6. Миронов М.Б., Иванова И.В., Мухин К.Ю. Геластические приступы. Эпилепсия 2014;6(3):20-9. [Mironov M.B., Ivanova I.V., Mukhin K.Yu. Gelastic seizures. Epilepsy 2014;6(3):20-9. (In Russ.)].
7. Миронов М.Б., Мухин К.Ю. Атипичные абсансы — распространенность, электроклинические и нейровизуализационные характеристики. Журнал неврологии и психиатрии им. С.С. Корсакова 2012;112(6):18-26. [Mironov M.B., Mukhin K.Yu. Atypical asences: prevalence, electroclinical and neuroimaging characteristics. S.S. Korsakov Journal
of Neurology and Psychiatrics 2012;112(6): 18-26. (In Russ.)].
8. Миронов М.Б., Мухин К.Ю. Клинические, электроэнцефалографические и ней-
ровизуализационные характеристики пациентов с эпилептическим миоклонусом век. Русский журнал детской неврологии 2014; 9(2):15-23. [Mironov M.B., Mukhin K.Yu. Clinical, electroencephalographic and neuroimaging characteristics of patients with epileptic myoclonus of the eyelids. Russian Journal of Child Neurology 2014;9(2):15-23. (In Russ.)].
9. Миронов М.Б., Мухин К.Ю. Эффективность антиэпилептической терапии в лечении эпилептических синдромов, ассоциированных с атипичными абсансами. Фарматека. Психиатрия и неврология 2012;s3-12:55-60. [Mironov M.B., Mukhin K.Yu. Efficacy of antiepileptic therapy for treatment of epileptic syndromes associated with atypical absences. Pharmateka. Psychiatry and Neurology 2012;s3-12:55-60. (In Russ.)].
10. Миронов М.Б., Мухин К.Ю.,
Гоева И.А. и др. Окципитальные окулото-нические приступы при симптоматическом варианте синдрома Веста (клиническое наблюдение). Русский журнал детской неврологии 2009;4(3):34-40. [Mironov M.B., Mukhin K.Yu., Goyeva I.A. et al. Occipital oculotonic seizures with syptomatic variant of the west syndrome (clinical observation).
ГН
о (N
Russian Journal of Child Neurology 2009;4(3):34-40. (In Russ.)].
11. Миронов М.Б., Мухин К.Ю., Кременчугская М.Р., Петрухин А.С. Видео-ЭЭГ-мониторинг в диагностике эпилептического негативного миоклонуса. Клинический случай. Русский журнал детской неврологии 2009;4(2):51—9. [Mironov M.B., Mukhin K.Yu., Kremenchugskaya M.R., Petrukhin A.S. Video EEG monitoring
in diagnostics of epileptic negative mioclonus. Clinical case report. Russian Journal of Child Neurology 2009;4(2):51-9. (In Russ.)].
12. Миронов М.Б., Мухин К.Ю., Теплышева А.М. и др. Эпилептические приступы во сне, имеющие клинико-элек-троэнцефалографические характеристики абсансов. Абсансы во сне: конфликт дефиниций. Русский журнал детской неврологии 2008;2(3):24-9. [Mironov M.B., Mukhin K.Yu., Teplysheva A.M. et al. Epileptic seizures during sleep that have clinical and electroencephalographic characteristics of absences. Absances during sleep: conflict of definitions. Russian Journal of Child Neurology 2008;2(3):24-9.
(In Russ.)].
13. Миронов М.Б., Ноговицын В.Ю., Абрамов М.О. и др. Синдром Феджермана (доброкачественный неэпилептический миоклонус младенчества). Клинические случаи. Эпилепсия 2013;2:42-6. [Mironov M.B., Nogovitsyn V.Yu., Abramov M.O. et al. Fejerman syndrome (benign non-epileptic mioclonus of early infancy). Clinical case reports. Epilepsy 2013;2:42-6. (In Russ.)].
14. Мухин К.Ю., Кваскова Н.Е., Миронов М.Б. и др. Кожевниковская эпилепсия при клещевом русском весенне-летнем энцефалите. Детская больница 2011;2:30-4. [Mukhin K.Yu., Kvaskova N.E., Mironov M.B. et al. Kozhevnikov epilepsy with russian tick-borne spring and summer encephalitis. Detskaya Bolnitsa 2011;2: 30-4. (In Russ.)].
15. Мухин К.Ю., Миронов М.Б. Фокальные приступы с гиперкинетическими (гипермоторными) автоматизмами
в педиатрической практике. Эпилепсия 2014;6(2):19-28. [Mukhin K.Yu., Mironov M.B. Focal seizures with hyperkinetic automatisms in pediatric practice. Epilepsy 2014;6(2):19-28. (In Russ.)].
16. Мухин К.Ю., Миронов М.Б. Эпилептические спазмы: нозологическая характеристика и подходы к терапии. Неврология, нейропсихиатрия, психосоматика. Эпилепсия 2012;спецвыпуск 1:4-9. [Mukhin K.Yu., Mironov M.B. Epileptic spasms: nosological characteristics and approaches to therapy. Neurology, meuropsychiatry, psychosomatics. Epilepsy 2012;Special Issue 1:4-9. (In Russ.)].
17. Мухин К.Ю., Миронов М.Б., Барлетова Е.И. Эпилептические ауры: клинические характеристики и топическое
значение. Русский журнал детской неврологии 2011;6(1):19—30. [Mukhin K.Yu., Mironov M.B., Barletova E.I. Epileptic auras: clinical characteristics and topical importance. Russian Journal of Child Neurology 2011;6(1):19-30. (In Russ.)].
18. Мухин К.Ю., Миронов М.Б., Какаулина В.С. и др. Фокальные аутомо-торные приступы с атоническим компонентом, исходящие из височной коры. Русский журнал детской неврологии 2010;5(4):3-16. [Mukhin K.Yu.,
Mironov M.B., Kakaulina V.S. et al. Focal automotoric seizures with atonic component originating from the temporal cortex. Russian Journal of Child Neurology 2010;5(4): 3-16. (In Russ.)].
19. Мухин К.Ю., Миронов М.Б., Кваскова Н.Е. и др. Эпилепсия Кожевникова у детей. Русский журнал детской неврологии 2006;1(2):19-29. [Mukhin K.Yu., Mironov M.B., Kvaskova N.E. et al. Kozhevnikov epilepsy of children. Russian Journal of Child Neurology 2006;1(2): 19-29. (In Russ.)].
20. Мухин К.Ю., Миронов М.Б., Кваскова Н.Е. и др. Эпилептический негативный миоклонус. Эпилепсия 2011;2: 15-21. [Mukhin K.Yu., Mironov M.B., Kvaskova N.E. et al. Epileptic negative mioclonus. Epilepsy 2011;2:15-21. (In Russ.)].
21. Мухин К.Ю., Миронов М.Б. Клинико-электроэнцефалографические характеристики и лечение эпилептических синдромов, ассоциированных с тоническими приступами. Русский журнал детской неврологии 2014;9(3):13-22. [Mukhin K.Yu., Mironov M.B. Clinical and electroencephalographic characteristics and treatment of epileptic syndromes associated with tonic seizures. Russian Journal of Child Neurology 2014;9(3):13-22. (In Russ.)].
22. Мухин К.Ю., Миронов М.Б., Петрухин А.С. Эпилептические синдромы. Диагностика и терапия. Руководство для врачей. М.: Системные решения, 2014. 376 с. [Mukhin K.Yu., Mironov M.B., Petrukhin A.S. Epileptic syndromes. Diagnostics and therapy. Manual for physicians. Moscow: Systemnye Resheniya, 2014. 376 p. (In Russ.)].
23. Мухин К.Ю., Петрухин А.С. Идиопати-ческие формы эпилепсии: систематика, диагностика, терапия. М., 2000. 319 с. [Mukhin K.Yu., Petrukhin A.S. Idiopathic forms of epilepsy: systematics, diagnostics, therapy. Мoscow, 2000. 319 p. (In Russ.)].
24. Петрухин А.С., Мухин К.Ю., Благосклонова Н.К. Эпилептология детского возраста. М.: Медицина, 2000. [Petrukhin A.S., Mukhin K.Yu., Blagosklonova N.K. Epileptology of childhood. Moscow: Medicine, 2000. (In Russ.)].
25. Холин А.А., Мухин К.Ю. Синдром Веста. Этиология, электроклинические характеристики и дифференциальный диагноз.
В кн.: Мухин К.Ю., Петрухин А.С., Холин А.А. Эпилептические энцефалопатии и схожие синдромы у детей. М.: Арт-Сервис Лтд., 2011. С. 95-133. [Kholin A.A., Mukhin K.Yu. West syndrome. Etiology, electroclinical characteristics, and differential diagnosis. In: Mukhin K.Yu., Petrukhin A.S., Kholin A.A. Epileptic encephalopathies and similar syndromes of children. Moscow: ArtService Ltd. 2011. Pp. 95-133. (In Russ.)].
26. Berg A.T., Berkovic S.F., Brodie M.J. et al. Revised terminology and concepts
for organization of the epilepsies: report of the ILAE Commission on Classification and Terminology, 2005-2009. Epilepsia 2010;51(4):676-85.
27. Bien C.G., Elger C.E. Epilepsia partialis continua: semiology and differential diagnoses. Epileptic Disord 2008;10(1):3-7.
28. Blume W.T., Luders H.O., Mizrahi E. et al. Glossary of descriptive terminology for ictal semiology: report of the ILAE task force
on classification and terminology. Epilepsia 2001;42(9):1212-8.
29. Dalla Bernardina B., Fontana E., Michelizza B. еt al. Partial epilepsies of childhood, bilateral synchronization, continuous spike-wave during slow sleep.
In: Advances in epileptology. XVIIth Epilepsy International Symposium. J. Manelis, E. Bental, J.N. Loeber, F.E. Dreifuss (eds.). N. Y.: Raven Press, 1989. Рр. 295-302.
30. Daly D.D., Mulder D.W. Gelastic epilepsy. Neurology 1957;7(3):189-92.
31. Engel J.Jr.; International League Against Epilepsy (ILAE). A proposed diagnostic scheme for people with epileptic seizures and with epilepsy: Report of the ILAE Task Force on Classification and Terminology. Epilepsia 2001;42(6):796-803.
32. Escueta A.V., Bacsal F.E., Treiman D.M. Complex partial seizures on closed-circuit television and EEG: a study of 691 attacks
in 79 patients. Ann Neurol 1982;11(3):292-300.
33. Ferner R., Panayiotopoulos C.P. Phantom typical absences, absence status, and experiential phenomena. Seizure 1993;2(3):253-6.
34. Ferrie C., Caraballo R., Covanis A. et al. Panayiotopoulos syndrome: a consensus view. Dev Med Child Neurol 2006;48(3):236-40.
35. Ferrie C.D., Caraballo R., Covanis A. et al. Autonomic status epilepticus in Panayiotopoulos syndrome and other childhood and adult epilepsies: a consensus view. Epilepsia 2007;48(6):1165-72.
36. Ferrie C.D., Koutroumanidis M., Rowlinson S. et al. Atypical evolution
of Panayiotopoulos syndrome: a case report. Epileptic Disord 2002;4(1):35-42.
37. Gascon G.G., Lombroso C.T. Epileptic (gelastic) laughter. Epilepsia 1971;12(1):63-76.
38. Gastaut H. Clinical and electroencephalographical classification of epileptic seizures. Epilepsia 1970;11(1): 102-13.
E
W
E
TOM IX
4
39. Guerrini R., Dravet C., Genton P. et al. Epileptic negative myoclonus. Neurology 1993;43(6):1078—83.
40. Guerrini R., Takahashi T. Myoclonus and epilepsy. Handb Clin Neurol 2013;111:667-79.
41. Holmes G.L. Partial complex seizures in children: an analysis of 69 seizures in 24 patients using EEG FM radiotelemetry and videotape recording. Electroencephalogr Clin Neurophysiol 1984;57(1):13-20.
42. Luders H.O., Noachtar S. Atlas of epileptic seizures and syndromes. Philadelphia:
W.B. Saunders Company, 2001. Pp. 26-7.
43. Luders H.O., Noachtar S. Epileptic seizures. Pathophysiology and clinical semiology. N. Y., 2000. 796 p.
44. Niedermeyer E. Sleep electroencephalograms in petit mal. Arch Neurol 1965;12:625-30.
45. Oguni H., Hayashi K., Imai K. et al. Study on the early-onset variant of benign childhood epilepsy with occipital paroxysms otherwise described as early-onset benign occipital seizure susceptibility syndrome. Epilepsia 1999;40(7):1020-30.
46. Panayiotopoulos C.P. A Clinical Guide to Epileptic Syndromes and their Treatment. UK: Blandon Medical Publishing, 2002.
96 p.
47. Panayiotopoulos C.P. A Clinical Guide to Epileptic Syndromes and their Treatment. 2nd edition. Springer, 2010. 620 p.
48. Panayiotopoulos C.P. Autonomic seizures and autonomic status epilepticus peculiar
to childhood: diagnosis and management. Epilepsy Behav 2004;5(3):286-95.
49. Panayiotopoulos C.P. Benign nocturnal childhood occipital epilepsy: a new syndrome with nocturnal seizures, tonic deviation of the eyes, and vomiting. J Child Neurol 1989;4(1):43-9.
50. Panayiotopoulos C.P., Agathonikou A., Koutroumanidis M. et al. Eyelid myoclonia with absences: the symptoms. In: Eyelid myoclonia with absences. J.S. Duncan, C.P. Panayiotopoulos (eds.). London: John Libbey and Company Ltd, 1996. Pp. 17-26.
51. Parisi P., Ferri R., Pagani J. et al. Ictal video-polysomnography and EEG spectral analysis in a child with severe Panayiotopoulos syndrome. Epileptic Disord 2005;7(4):333-9.
52. Penfield W., Jasper K. Epilepsy and the functional anatomy of the human brain. Boston: Little, Brown, 1954.
53. Proposal for revised clinical and electroencephalographs classification
of epileptic seizures. From the Commission on Classification and Terminology of the International League Against Epilepsy. Epilepsia 1981;22(4):489- 501.
54. Riqueta A., Auvina S., Cuisseta J.M. et al. Epilepsia partialis continua and defects in the mitochondrial respiratory chain. Epilepsy Res 2008;78(1):1-6.
55. Tassinari C.A., Bureau M., Thomas P. Epilepsy with myoclonic absences. In: Epileptic syndromes in infancy, childhood and adolescence. J. Roger, M. Bureau, C. Dravet, F.E. Dreifuss, A. Perret, P. Wolf (eds.). London: John Libbey, 1992. Pp. 151-60.
56. Tassinari C.A., Rubboli G., Parmeggiani L. et al. Epileptic negative myoclonus. Adv Neurol 1995;67:181-97.
57. Tinuper P., Lugaresi E., Vigevano F. et al. Nocturnal frontal lobe epilepsy. In: Epilepsy and movement disorders. R. Guerrini et al. (eds.). Cambridge, 2001. Pp. 97-109.
E ra E
