ИССЛЕДОВАНИЯ.
ПОТЕНЦИАЛЬНЫЕ ОШИБКИ
ЭПИДЕМИОЛОГИЧЕСКИХ
ИССЛЕДОВАНИЙ
Цель
аналитического
этапа исследования — оценка гипотез о
причинах (факторах
риска) возникновения заболеваний (других
исходов). К
аналитическим
приемам исследований относятся:
-
Приемы формальной
логики. -
Приемы
статистики (оценка коэффициента
корреляции, коэффициента
регрессии,
относительного риска, отношения
преобладаний и др.). -
Когортные
исследования. -
Исследования
«случай-контроль».
Формулировка
гипотез начинается на описательном
этапе. На аналитическом этапе
продолжается использование приемов
формальной логики для формулировки
новых гипотез. Провести четкую границу
между описательным и аналитическим
этапом в плане формулировки гипотез
практически невозможно.
Для
обоснования причинно-следственных
связей используют приемы различия,
сходства, сопутствующих изменений,
аналогии, остатков. Для количественной
оценки связи между двумя анализируемыми
показателями проводят корреляционный
анализ. С помощью регрессионного анализа
устанавливают форму
корреляционной связи.
Воздействие
факторов риска всегда предшествует
развитию заболевания. Воздействие
может быть однократным, например,
облучение населения при аварии
на атомной станции. Чаще контакт с
факторами риска, вызывающими
хронические
заболевания, происходит в течение
некоторого периода времени (курение,
артериальная гипертензия, беспорядочные
половые связи, инсоляция).
Лучшим
способом выяснить, действительно ли
воздействие потенциального фактора
риска увеличивает вероятность заболевания,
был бы эксперимент. К
сожалению, воздействие большинства
факторов риска на человека нельзя
изучать
с помощью экспериментальных исследований,
когда исследователь определяет, кого
подвергать воздействию. Клинические
исследования, в которых исследователь
собирает данные путем простого наблюдения
событий в их естественном течении,
не вмешиваясь в них активно, называются
обсервационными
исследованиями (observational
studies).
Таково большинство исследований риска;
сюда относятся когортные
‘исследования (cohort
studies)
и исследования
«случай—контроль»
(case
control
studies),
Когортные
исследования — это продольные
исследования. Продольные
аналитические
эпидемиологические исследования
(longitudinal
studies)
процессов
заболеваемости или смертности направлены
на изучение частоты, с которой лица
в сравниваемых популяциях переходят
из состояния «здоровый» («живой»)
в состояние «больной» («умерший»).
Когортные
аналитические эпидемиологические
исследования предполагают
изучение процесса заболеваемости в
когортах лиц, подверженных и не
подвержных
изучаемому воздействию. При когортных
исследованиях идут от фактора
к патологии.
Когорта
— это группа людей, которая изначально
объединена каким- либо общим признаком
и наблюдаемых в течение определенного
времени, чтобы проследить,
что с ними произойдет в дальнейшем.
Например: прослеживают людей, подвергающихся
воздействию свинца, затем смотрят, чем
они болеют и от
чего умирают. Существует два способа
проведения когортных исследований:
проспективное
когортное исследование и ретроспективное
когортное исследование.
Когорта
может быть сформирована в настоящее
время и прослежена в будущем (проспективное
когортное исследование, concurrent
cohort
study),
т.е. когорта
формируется на день исследования и
изучается на протяжении последующего
времени (например формируется в 2007 г.,
а наблюдаются до 2017 г.), при
этом основным способом оценки является
регистрация новых случаев заболевания
в течение определенного срока. При
проспективном исследовании предполагается,
что начало заболевания совпадает с
началом исследований.
При
ретроспективном исследовании
(ретроспективное
когортное исследование,
historical
cohort
study)
оценку изучаемого фактора риска проводят
на исторической
когорте, когда группа наблюдения
сформирована на основе ретроспективы.
При ретроспективном способе формирования
когорты начало исследования
не совпадает с началом периода наблюдения.
Сбор информации о характере
и уровнях экспозиции и заболеваниях,
развивавшихся у членов когорты,
осуществляется на основе архивных
данных и регистрационных записей,
относящихся
к
периоду, предшествовавшему времени
проведения исследований. И так когорта
прослеживается вплоть до настоящего
времени.
Достоинства и
недостатки когортных исследований
Некоторые
достоинства и недостатки когортных
исследований по изучению
факторов риска обобщены. Когортные
исследования риска — наилучшая замена
истинного эксперимента в ситуации,
когда эксперимент невозможен. Они
основаны на той же логике, что и клинические
испытания, и позволяют выявить
воздействие возможного фактора риска,
избегая систематических ошибок,
которые непременно возникают, если
оценка воздействия производится уже
после того, как стал известен исход.
Достоинства:
-
Единственный
способ непосредственной оценки
заболеваемости. -
Отвечают
на клинический вопрос, заболеют ли
люди, если они подверглись воздействию
фактора риска.
3. При
оценке эффекта воздействия позволяют
избежать систематической ошибки,
которая обычно возникает, если исход
известен заранее.
4. Позволяют
оценить связь между воздействием фактора
риска и несколькими заболеваниями.
Недостатки:
1.
Число включенных лиц должно быть
значительно больше, чем число пациентов
с изучаемым заболеванием, поэтому метод
непригоден для редких заболеваний.
-
Лица,
включенные в группу, обычно живут
свободно, а не под контролем исследователей.
Для поддержания контакта с ними требуются
значительные усилия
и средства. Поэтому когортные исследования
стоят дорого, иногда миллионы
рублей. -
Результаты долгое
время остаются неизвестными. -
Позволяют
оценить связь между заболеванием и
воздействием относительно небольшого
числа факторов (тех, что были определены
в начале исследований).
Поскольку
затраты времени и денег ограничивают
использование когортных
исследований, они применяются для
получения ответов только на самые важные
вопросы.
В научном аспекте
основной недостаток обсервационных
исследований, включая когортные, состоит
в том, что они в большей степени, чем
экспериментальные, подвержены
систематическим ошибкам.
Таким
образом, классическая схема когортного
исследования характеризуется тем,
что из популяции отбирают 2 группы лиц,
отличающиеся наличием экспозиции
исследуемому фактору. Обе группы состоят
из лиц, не болеющих изучаемым заболеванием
в начальный период времени. Лица,
включенные в когорту,
классифицируются по характеристикам
(потенциальным факторам риска),
которые могут влиять на исход.
Эту
когорту наблюдают в течение определенного
периода, чтобы установить, у кого из
ее участников возникнет изучаемый
исход. По истечении периода наблюдения
каждую из групп подразделяют на 2
составляющие: заболевшие и
не заболевшие.
экспонируемые:
-
заболевшие (а)
-
не
заболевшие (b)
не экспонируемые:
-
заболевшие (с)
-
не
заболевшие (d).
Аналитические
возможности этого метода позволяют
одновременно изучать влияние
нескольких факторов риска на возникновение
одной заранее выбранной нозологической
формы или одного класса болезней. При
этом появляется возможность
анализировать совместное влияние тех’
или иных сочетаний факторов и оценивать
результаты их взаимодействия.
Теория
исследований «случай — контроль» вытекает
из теории когортных
исследований. Ее можно было бы описать
как попытку реконструировать когортное
исследование после того, как события
(заболевания) уже произошли. При
исследовании «случай — контроль» группу
заболевших (опытная) сравнивают
с контрольной (референтная), в которой
заболевших не было. При данном
эпидемиологическом
наблюдении идут от патологии к изучению
факторов.
Главным
типом исследований этиологии болезней
человека являются исследования
типа «случай — контроль» (ИСК,
case-control
studies,
CCS,
англ.). В основе
ИСК лежит сопоставление экспозиций,
которым подвергались больные, с
прошлыми экспозициями здоровых людей.
Из-за
этого ИСК иногда называют ретроспективными
исследованиями, что неверно, поскольку
в ИСК реконструируется нормальное
(проспективное)
течение
событий во времени на основе доступной
информации. В условиях, когда
экспериментальное или проспективное
исследования невозможны, ИСК являются
способом реконструкции развития
заболеваний по данным однократного
исследования. ИСК являются наиболее
оперативными исследованиями, экономны
в реализации и при корректном проведении
способны дать правильную оценку гипотезы.
Исследование
«случай — контроль» стало распространенным
методом изучения
этиологии и клинического течения
заболеваний. Его преимущества заключаются,
прежде всего, в том, что исследователи
могут выявлять случаи и делать сравнения,
независимо от распространенности
заболевания. Важнейшее достоинство
этой схемы состоит в значительной
экономии времени и снижении трудоемкости
исследования за счет уменьшения
численности групп.
Схема
«случай—контроль» особенно эффективна
при изучении редких заболеваний
или болезней с длительным латентным
периодом. Реальное преимущество
исследований «случай—контроль» при
установлении роли причинных
или прогностических факторов состоит
в отсутствии необходимости ожидать
ответа длительное время. Многие
заболевания имеют продолжительный
латентный период — промежуток времени
от воздействия фактора риска до проявления
патологического эффекта. Так,
канцерогенность некоторых химических
веществ проявляется только через 10-20
лет после воздействия этих факторов.
От исследователей и медиков потребовалось
бы слишком много терпения,
чтобы выяснить, подтвердится ли
подозреваемый риск.
Вместе
с тем эта схема имеет ряд недостатков,
и главный из них — меньшая
достоверность получаемых результатов
по сравнению с данными когортных
исследований. Это обусловлено, прежде
всего, сравнительно невысокой
точностью оценки воздействия факторов
риска в прошлом, чаще основывающейся
на субъективных данных. Значительные
трудности в проведении таких
исследований появляются в случае
изучения редких воздействий.
Основные
характеристики исследования «случай
— контроль»:
-
популяция,
подвергающаяся воздействию фактора
риска, не обязательно
определена; -
случаи
отбираются исследователем из имеющейся
совокупности больных; -
контрольная
группа отбирается исследователем таким
образом, чтобы
она
была сходной с экспериментальной
группой; -
факт
воздействия оценивается и
восстанавливается
по памяти после развития заболевания; -
риск
или заболеваемость нельзя измерить
непосредственно, относительный
риск воздействия можно оценить по
отношению шансов.
Особенность
проведения эпидемиологических
исследований «случай -контроль»
состоит в том, что наличие связи между
воздействием и заболеванием
оценивают путем сравнения распространенности
изучаемого воздействия в группах лиц,
имеющих и не имеющих данную форму
патологии.
Оценка
связи между воздействием фактора риска
и развитием болезни
в аналитических исследованиях
|
Результат |
Наличие болезни |
Всего |
|
|
Аналитические |
присутствует | |
||
|
Экспонированная |
а с |
b d |
a+b c+d |
|
Всего |
а+с |
b+d |
a+b+c+d |
Для
количественной оценки связи между
воздействием фактора риска и развитием
болезни вычисляют следующие показатели:
a.
отношение
шансов (ad/bc);
b.
относительный
риск (a(c+d)/c(a+b);
c.
атрибутивный
риск (a/(a+b)-c/(c+d);
d.
популяционный
риск (произведение атрибутивного риска
на распространенность фактора риска
среди населения) и
некоторые другие.
Потенциальные
ошибки различных эпидемиологических
исследований
Систематическая
ошибка, или
смещение — это систематическое
(неслучайное,
однонаправленное) отклонение результатов
от истинных значений.
Наблюдение
за больными (при лечении или в исследовании)
особенно подвержено систематическим
ошибкам вследствие простой небрежности.
Участвуя в исследовании, больные
часто продолжают вести себя так, как им
хочется, что подчас не отвечает
условиям получения строгих научных
результатов. Когда
с ними пытаются провести эксперимент
наподобие лабораторного, из этого
часто ничего не получается. Некоторые
больные отказываются участвовать,
другие выбывают в процессе исследования
или предпочитают сменить метод
лечения. Более того, некоторые самые
важные с человеческой точки зрения
характеристики — эмоции, ощущение
комфорта, поведение — измерить гораздо
труднее, чем физические параметры, такие
как артериальное давление или содержание
натрия в сыворотке. К тому же клиницисты
сами склонны верить в успех применяемого
ими лечения (большинство больных и не
захотели бы лечиться у врача, который
думает иначе). Из-за этой установки,
которая так важна в
медицинской
практике, клинические наблюдения
особенно подвержены систематическим
ошибкам. Хотя существуют десятки
разновидностей систематических
ошибок, большинство из них может быть
отнесено к одной из трех основных
категорий:
-
Систематическая
ошибка, обусловленная отбором, возникает
когда
сравниваемые группы пациентов различаются
не только по изучаемому
признаку,
но и по другим факторам, влияющим на
исход. -
Систематическая
ошибка, обусловленная измерением,
возникает,
когда
в сравниваемых группах больных
используются разные методы измерения.
3.
Систематическая ошибка, обусловленная
вмешивающимися факторами,
возникает,
когда один фактор связан с другим, и
эффект одного искажает
эффект другого.
Систематическая
ошибка, обусловленная
отбором
(selection
bias),
возникает,
когда сравниваемые группы пациентов
различаются не только по главным
изучаемым признакам, но и по другим
факторам, влияющим на результат
исследования. Группы пациентов часто
различаются по многим параметрам —
возрасту, полу, степени тяжести
заболевания, сопутствующим заболеваниям,
методам вмешательства. Если мы сравним
данные по двум группам, которые
различаются
не только по специфическим интересующим
нас факторам (например,
метод лечения или предполагаемая причина
заболевания), но и по другим признакам,
от которых тоже зависит исход, то
результат сравнения получится смещенным
и не позволит сделать выводы о степени
влияния интересующего нас
фактора.
Систематическая
ошибка, обусловленная измерением
(measurement
bias),
возникает,
когда в сравниваемых группах пациентов
применяются неодинаковые
методы оценки.
Систематическая
ошибка, обусловленная вмешивающимися
факторами (confounding
bias),
возникает, когда два фактора взаимосвязаны
(«ходят парой»), причем
один из них искажает эффект другого.
Это может произойти из-за систематической
ошибки при отборе, под действием
случайности или вследствие реально
существующей взаимосвязи между факторами.
Систематические
ошибки, возникающие при отборе и при
воздействии вмешивающихся факторов,
не исключают друг друга. Однако они
рассматриваются
по отдельности, поскольку относятся к
разным этапам клинического наблюдения
или исследования.
Систематическая
ошибка при отборе возникает при
формировании групп пациентов
для наблюдения, следовательно, об этой
опасности следует помнить во
время планирования исследования. Ошибка
из-за вмешивающихся факторов должна
учитываться в процессе анализа данных
после окончания исследования.
Часто в одном и
том же исследовании обнаруживается
несколько видов систематических ошибок.
Случайная ошибка
Заболевания
обычно изучаются на выборках пациентов,
а не на общей популяции
(генеральной совокупности) всех лиц с
рассматриваемым состоянием.
Результаты наблюдений в выборке, даже
если эта выборка несмещенная, могут
не отражать положения в популяции в
целом из-за случайной ошибки. Однако
если повторять наблюдения во многих
выборках таких больных, то получаемые
результаты будут колебаться около
истинной величины. Отклонение результата
(отдельного) наблюдения в выборке от
истинного значения в популяции,
обусловленное исключительно случайностью,
называется случайной
вариацией. Случайная
ошибка может вмещаться на любом этапе
клинического наблюдения.
В
отличие от систематической ошибки,
которая вызывает отклонение оценки
от истины либо в одну, либо в другую
сторону, случайная вариация с
одинаковой
вероятностью приводит к завышенной и
к заниженной оценке. В итоге, среднее
значение результатов множества
несмещенных наблюдений в выборках
стремится к истинному значению в
популяции, даже если результаты,
полученные
в отдельных небольших выборках, далеки
от этого.
При
анализе клинических данных вероятность
случайных вариаций определяется
статистическими методами. Применение
статистики также помогает минимизировать
случайную ошибку путем выбора оптимальных
методов исследования
и анализа данных. Однако случайную
вариацию никогда нельзя исключить
полностью и следует обязательно учитывать
при оценке результатов клинических
наблюдений.
Два
источника ошибок — смещение и случайность
— не исключают друг друга. Как правило,
они присутствуют одновременно. Их
необходимо различать,
поскольку бороться с тем и другим
приходится по-разному. Теоретически
систематическую ошибку можно предотвратить
путем правильного проведения клинических
наблюдений или коррекцией при последующем
анализе данных.
Понятие «риск»
в эпидемиологии
Под
риском обычно понимают вероятность
какого-то неблагоприятного события.
Эпидемиологический
риск можно
определить как возможность осложнения
эпидемиологической ситуации, такое
осложнение может иметь место в
определенное время («время риска»), на
определенной территории («территория
риска»), в определенной группе населения
(«группа риска»).
Таким
образом, эпидемиологический риск — это
потенциальная возможность осложнения
эпидемиологической ситуации, ожидаемая
или возникшая в связи
с неблагоприятным воздействием на нее
определенных факторов риска. В тех
случаях, когда дается количественная
характеристика риска, его определяют
не как возможность, а как вероятность
осложнения эпидемиологической ситуации.
Практически
каждого человека волнует, насколько
велик риск возникновения
у него того или иного заболевания. Эта
озабоченность обусловливает появление
множества популярных книг и газетных
статей о риске развития рака молочной
железы при воздействии токсичных
химических веществ, риске заражения
СПИДом при переливании крови или риске
развития рака предстательной
железы после операции вазэктомии, а
также о путях снижения риска этих
и других заболеваний.
Факторами
риска (risk
factors)
называются особенности организма или
внешние
воздействия, приводящие к увеличению
риска возникновения заболевания.
Работа по программе «Геном человека»
позволила идентифицировать ряд
заболеваний со специфическими генами
в качестве факторов риска: в частности,
рак толстой кишки, остеопороз, боковой
амиотрофический склероз. Другие
факторы риска, такие как возбудители
инфекций, фармакологические препараты
и токсины, находятся в окружающей среде.
Некоторые факторы являются частью
социального окружения. Показано,
например, что эмоциональная нагрузка
в связи с потерей супруга, изменениями
повседневной жизни или скученностью
проживания повышают частоту заболеваний,
причем не только психических,
но и соматических. Некоторые из наиболее
значимых факторов риска относятся к
сфере поведения человека: курение,
избыточное потребление алкоголя,
пренебрежение ремнями безопасности
при езде на автомобиле, беспорядочная
половая жизнь.
Воздействие
факторов риска всегда предшествует
развитию заболевания. Воздействие
может быть однократным, например
облучение населения при аварии
на атомной станции. Чаще контакт с
факторами риска, вызывающими хронические
заболевания, происходит в течение
некоторого периода времени (курение,
артериальная гипертензия, беспорядочные
половые связи, инсоляция).
Существует несколько способов описания
воздействия факторов риска: наличие
факта воздействия, действующая доза,
максимальная доза, общая накопленная
доза, продолжительность воздействия в
годах, время, прошедшее после
первого контакта с фактором риска и
т.д. Несмотря на то, что многие из этих
количественных показателей могут быть
вычислены один из другого, некоторые
из них демонстрируют связь между дозой
и эффектом, в то время как для
других эта связь отсутствует.
Так,
общая накопленная доза солнечной
радиации является фактором риска
развития немеланомного рака кожи, а
сильные солнечные ожоги больше
предрасполагают
к развитию меланомы.
Если
некоторое воздействие быстро и с высокой
вероятностью приводит К
развитию определенного заболевания,
то нетрудно догадаться, что это
воздействие является фактором риска
для данного заболевания. В частности,
оценка причин таких состояний, как
ветряная оспа, солнечный ожог или
передозировка
аспирина не составляет труда, поскольку
соответствующие заболевания следуют
относительно быстро за воздействием
очевидных факторов риска. Однако
заболеваемость и смертность в большей
степени обусловлены хроническими
болезнями, для которых связь между
воздействием фактора риска и развитием
заболевания носит не столь явный
характер. Поэтому врач, каким бы
проницательным он ни был, не может
оценить риск на основании своей личной
практики.
Многие
факторы риска, такие как курение или
потребление пищи с высоким
содержанием холестерина и насыщенных
жиров, настолько распространены в
нашем обществе, что в течение многих
лет не казались опасными. Только при
сравнении заболеваемости людей с этими
факторами риска и без них или путем
исследования особых подгрупп, например
мормонов (которые не курят) или
вегетарианцев (которые употребляют
пищу с низким содержанием холестерина),
удалось понять значимость этих факторов
риска.
Применение
показателей риска:
-
Прогнозирование.
Знание
факторов риска используется, прежде
всего,
для
прогнозирования заболевания. Наиболее
полную информацию для прогнозирования
болезни у индивидуума можно получить,
обобщив фактический материал,
полученный при изучении большого числа
людей со сходным фактором
риска. -
Причина.
Хотя
предсказать заболевание по наличию
тех или иных факторов
риска можно, они не всегда служат его
причиной. Фактор риска может
оказаться
косвенным маркером исхода благодаря
связи с одним или несколькими
причинными факторами, т.е. он может лишь
находиться под влиянием причинного
фактора. Фактор риска, не являющийся
причиной заболевания, называется
маркером, поскольку он служит «меткой»
(marker)
повышенной вероятности развития
заболевания.
3.
Профилактика.
Если
фактор риска является к тому же причиной
болезни, то его устранение можно
использовать в качестве профилактической
меры,
независимо от того, известен или нет
патогенез заболевания. Иллюстрацией
служат
некоторые классические примеры из
истории эпидемиологии. Так, еще до того
как был идентифицирован возбудитель,
Сноу заметил, что холерой чаще
заболевают люди, употребляющие воду из
определенных источников, и предотвратил
эпидемию, перекрыв эти источники.
Популяционный
риск. Мы
можем посмотреть на риск и с другой
стороны, задав
вопрос: каков вклад фактора риска в
общую заболеваемость группы людей,
а не отдельных индивидуумов? Такого
рода информация позволяет определить,
какие факторы риска действительно
важны, а какие не имеют особого значения
для здоровья общества. Это помогает
административным органам системы
здравоохранения определять приоритеты
при распределении ресурсов. Относительно
слабый фактор риска (с низким относительным
риском), но с высокой
распространенностью в данной популяции
может создать более значительную
заболеваемость, чем сильный, но редкий
фактор риска.
Для
того чтобы оценить риск в популяции,
необходимо знать, с какой частотой
члены рассматриваемой популяции
подвергаются воздействию фактора
риска. Популяционный
добавочный (атрибутивный)
риск
(population
attributable
risk)
рассчитывается как произведение
добавочного риска на распространенность
фактора риска в
популяции.
Этот показатель отражает дополнительную
заболеваемость в популяции, связанную
с фактором риска. Кроме
того, можно определить долю заболеваемости
в популяции, связанную с данным
фактором риска, т.е. добавочную долю
популяционного риска. Она рассчитывается
путем деления добавочного популяционного
риска на общую заболеваемость
в популяции.
Доказательная
медицина
В
последнее
десятилетие существенно возросла роль
такого направления в
здравоохранении как доказательная
медицина. В
основе доказательной медицины лежит
клиническая
эпидемиология, ее
главнейший постулат — любое решение в
медицинской практике должно опираться
на строго доказанные научные
факты.
Доказательная
медицина
—
это раздел медицины, использующий
эпидемиологический
метод для получения медицинской
информации, основанной
только на строго доказанных научных
фактах, исключающих влияние
систематических и случайных ошибок.
Часто
складывается такая ситуация, когда
результаты отдельных исследований
бывают неопределенными, в частности,
из-за малого числа популяции пациентов
или редко развивающихся исходов. Выходом
из таких ситуаций является
объединение данных нескольких
разрозненных, но сходных клинических
исследований, посвященных одному и тому
же вопросу, и формирование как бы одного
большого исследования. Такой подход
обеспечивает большую статистическую
мощность за счёт увеличения размера
выборки — мета-анализ.
Мета-анализ
(анализ анализов, синтез информации)
предназначен для повышения
достоверности оценок. Увеличение
количества данных снижает вероятность
систематических и случайных ошибок, в
результате чего возрастает достоверность
данных и обеспечивается большая
надежность принятия решений.
Контрольные
вопросы по теме
1. В
официальной статистике РФ для отражения
состояния здоровья на
селения
используют:
а) кумулятивный
показатель заболеваемости
б) данные
ВОЗ
в) результаты
скрининговых исследований
г) результаты
анкетирования
2.
Показатель
превалентности (распространенности):
а) показатель
заболеваемости, характеризующий риск
заболевания у лиц,
контактировавших
с инфекционным больным
б) показатель
заболеваемости, используемый для оценки
риска заболеть
хроническими инфекциями
(например, туберкулезом)
в) показатель
заболеваемости, учитывающий все случаи
какого-либо заболевания
независимо от времени его возникновения
г) отражает
риск лиц, относящихся к одной
профессиональной группе,
заболеть
определенной болезнью
3. Основные
этапы эпидемиологического исследования:
а) подготовительный,
сбор данных, описательный, аналитический
б) организация
исследования и анализ
в) сбор
информации и ее первичная обработка
г) анализ
статистических данных и формулирование
выводов
4. Синонимы
термина «эпидемиологическое исследование»:
а) эпидемиологическая
диагностика
б) расследование
вспышек болезней
в) эпидемиологический
анализ
г) обследование
эпидемических очагов
5. Наблюдательные
эпидемиологические исследования
отличаются от
экспериментальных тем,
что:
а) исследуемая
и контрольная группы могут быть разной
численности
б) наблюдательные
исследования бывают только когортными
в) наблюдательные
исследования бывают только проспективными
г) наблюдательные
исследования не предусматривают
вмешательства в
естественное
течение событий
6. Аналитическое
эпидемиологическое исследование может
быть:
а) ретроспективным
б) наблюдательным
в) выборочным
г) полевым
7. В
городе Н. в январе 1996 г. специалисты
кардиоцентра для оценки
распространённости
ревмокардита среди подростков обследовали
25% школьников
старших классов. Проведенная ими работа:
а) не
является эпидемиологическим исследованием,
так как изучалась
лишь
частота возникновения ревмокардита, а
не его факторы риска
б) не
является эпидемиологическим исследованием,
так как ревмокардит
нельзя считать
типичным инфекционным заболеванием
в) является
одномоментным эпидемиологическим
исследованием
г) является
наблюдательным эпидемиологическим
исследованием
8. Эпидемиологическим
исследованием является:
а) расследование
вспышки инфекционных заболеваний
б) исследование
типа «случай — контроль», проводимое в
клинике
в) полевое
исследование типа «случай — контроль»
г) расследование
вспышки болезни неизвестной этиологии
9. Целью
отдельных эпидемиологических исследований
могут быть:
а) описание
заболеваемости какой-либо болезнью
б) оценка
потенциальной эффективности
профилактических и лечебных
средств
в) выявление
факторов риска распространения болезни
г) планирование
противоэпидемических мероприятий
10. Можно
ли называть эпидемиологическим
исследованием расследование
вспышки дизентерии в детском дошкольном
учреждении:
а) нет,
так как это не эпидемиологическое
исследование, а обследование
эпидемического
очага с множественными случаями
б) да,
это вариант эпидемиологического
исследования типа «случай — контроль»
в) нет,
так как это обычная рутинная работа
эпидемиолога
г) да,
это вариант аналитического
эпидемиологического исследования
Ситуационные
задачи
Задача №1
С
целью оздоровления условий труда
монтажниц микросхем, соприкасающихся
с парами и аэрозолями редкоземельных
элементов, изучена за 3-х летний период
частота временной нетрудоспособности
(заболеваемость) 150
работниц
крупного радиозавода в возрасте 30-49 лет
(основная группа). Установлено, что
среди
данной группы заболевших было 98 чел.,
здоровых — 52 чел. В качестве контрольной
группы выбраны 150 работниц заводоуправления
аналогичного
возраста, не контактирующие с парами и
аэрозолями редкоземельных
элементов. При анализе заболеваемости
среди них установлено, что заболевших
в этой группе 41. чел., здоровых — 109 чел.
Задание:
1) составить четырехпольную таблицу; 2)
рассчитать абсолютный риск,
относительный риск, атрибутивный риск;
относительную разность рисков,
шансы на развитие заболевания при
наличии фактора риска и при отсутствии
фактора риска; 3) оценить достоверность
различий состояния здоровья
работниц основной и контрольной групп.
Задача №2
С
целью изучения причин развития ишемической
болезни сердца (ИБС) были
проведены исследования «случай —
контроль». Был поставлен вопрос,
увеличивает
ли риск развития ИБС ежедневное
употребление кофе. В контрольную
группу были включены 108 больных с ИБС
терапевтического отделения
городской больницы, в опытную — 108 больных
ЛОР-отделения, не имеющие
ИБС. При опросе больных было установлено,
что в опытной группе ежедневно употребляли
кофе 79 чел., употребляли его редко 29
чел.; в контрольной группе ежедневно
употребляли кофе 36 чел., употребляли
редко — 72 чел.
Задание:
1) составить четырехпольную таблицу; 2)
рассчитать шансы и отношение
шансов; 3)провести оценку отношения
шансов.
Слайд 1
Менеджмент научных исследований
Кошмаганбетова Г.К.
отдел непрерывного профессионального развития

Методология научных исследований
Слайд 2
Клиническая эпидемиология и ее практическое воплощение – доказательная

медицина (evidence based medicine) являются основой методологии научных исследований
Слайд 3
Клиническая эпидемиология (Clinical epidemiology) – это наука, позволяющая осуществлять

прогнозирование для каждого конкретного пациента на основании изучения клинического
течения болезни в аналогичных случаях с использованием строгих научных методов
изучения групп больных для обеспечения точности прогнозов.
Слайд 4
Цель клинической эпидемиологии
– разработка и применение таких

методов клинического наблюдения, которые дают возможность делать справедливые заключения,
избегая влияния систематических и случайных ошибок.
В этом заключается важнейший подход
к получению информации, необходимой врачам для принятия правильных решений.
Слайд 5
Основные положения клинической эпидемиологии
• в большинстве случаев диагноз,

прогноз и результаты лечения для конкретного больного однозначно не
определены и потому должны быть выражены через вероятности;
• эти вероятности
для конкретного больного лучше всего оцениваются на основе предыдущего опыта, накопленного в отношении групп аналогичных больных;
Слайд 6
• поскольку клинические наблюдения проводятся на свободных в

своем поведении больных, и делают эти наблюдения врачи с
разной квалификацией и собственным мнением, результаты могут быть подвержены систематическим
ошибкам, ведущим к неверным заключениям;
• любые наблюдения, и клинические в том числе, подвержены влиянию случайности;
• чтобы избежать неверных выводов, врачи должны полагаться на исследования, основанные на строгих научных принципах, с использованием методов минимизации систематических ошибок и учета случайных ошибок.
Слайд 7
Основные принципы КЭ
внедрять методы клинического наблюдения и анализа

данных, обеспечивающие принятие верных решений
Слайд 8
Доказательная медицина – это использование результатов лучших клинических

исследований для выбора лечения конкретного пациента, это интеграция лучших
научных доказательств с клиническим опытом и ожиданиями пациентов.
Слайд 9
5 ШАГОВ В ПРОЦЕССЕ ДМ
Сформулировать вопрос на

который можно ответить(спроси)
Найти наилучшие доказательства(приобрети)
Критически оценить доказательства (оцени)
Интегрировать
с клиническими знаниями и ценностями пациента(примени)
Мониторинг вашей эффективности(измерь)
Слайд 11
Клинические явления, представляющие интерес для клинической эпидемиологии –
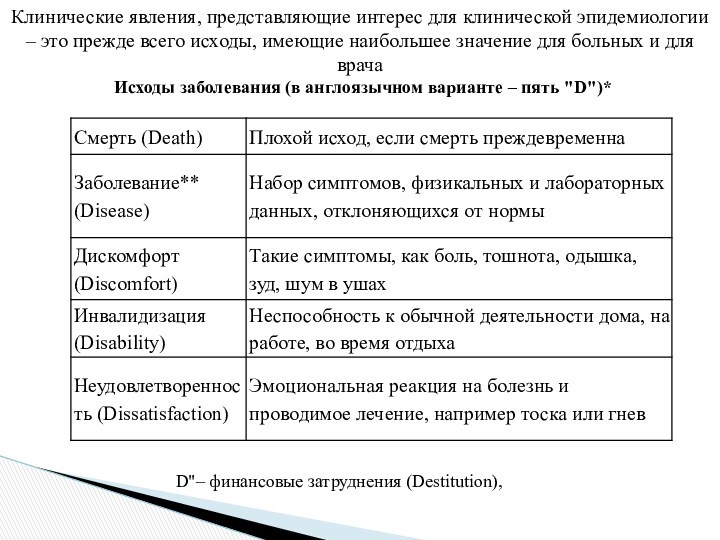
это прежде всего исходы, имеющие наибольшее значение для больных
и для врача
Исходы заболевания (в англоязычном варианте –
пять «D»)*
D»– финансовые затруднения (Destitution),
Слайд 13
Систематические ошибки в клиническом наблюдении
• Систематическая ошибка, обусловленная отбором(selection

bias), возникает, когда сравниваемые группы пациентов различаются не только
по изучаемому признаку, но и по другим факторам, влияющим на
исход.
• Систематическая ошибка, обусловленная измерением(measurement bias), возникает, когда в сравниваемых группах больных используются разные методы измерения.
• Систематическая ошибка, обусловленная вмешивающимися факторами(confounding bias), возникает, когда один фактор связан с другим, и эффект одного искажает эффект другого.
это «систематическое (неслучайное, однонаправленное) отклонение результатов от истинных значений»
Слайд 14
Отклонение результата (отдельного) наблюдения в выборке от истинного

значения в популяции, обусловленное исключительно случайностью, называется случайной вариацией.
Слайд 15
справедливы ли полученные выводы для всех элементов выборки?

Достоверность (internal validity)
исследования определяется тем, в какой мере полученные
результаты справедливы в отношении данной выборки. Это внутренняя характеристика, она
касается именно данной группы больных и не обязательно распространяется на другие группы. Достоверность клинического исследования определяется тем, насколько хорошо разработан план, правильно проведены сбор и анализ данных; степень достоверности определяется наличием и выраженностью систематических и случайных ошибок.
Слайд 16
Обобщаемость (external validity, or generalizability) –
внешняя характеристика, она

определяется тем, в какой мере результаты данного исследования применимы
к другим группам больных. Для врача это соответствует ответу на
вопрос: «Если результаты данного исследования верны, то применимы ли они к моему пациенту?»
Слайд 17
Постановка проблемы с помощью вопросов PICO — Т
метод

формулировки проблемы, который ставит вопросы относительно к конкретной клинической
практике.
P-patient or population – пациент или популяция,
I-intervention –
вмешательство,
C-comparison – сравнение,
О-outcomes – исходы
Т-time-время
Перед началом поиска следует выбрать ответы на указанные вопросы PICO, которые станут ключевыми терминами при онлайновом поиске
Слайд 19
Вопрос должен быть составлен таким образом, чтобы учитывать

следующее:
1.Группу больных (Р);
2.Воздейсвие интересующего Вас лекарства (I);
3.Имеющееся на данный
момент сравнительное лечение (C);
4.РезультатИсход, который хотят получить врачи и пациенты
(О).
Слайд 20
пример:
Способствует ли использование метформина (I) снижению риска

возникновения инсульта (О) у пациента с сахарным диабетом старше
60 лет (Р) по сравнению с глибенкламидом (C)?
P- – пациенты
с сахарным диабетом старше 60 лет
I- использование метформина
C- по сравнению с глибенкламидом
О- снижение риска возникновения инсульта
Слайд 21
Алгоритм информационного поиска
Слайд 22
Что искать?
Источники медицинской информации подразделяются на три

категории: первичные, вторичные и третичные
Первичная литература — включает в
себя статьи из журналов и неопубликованные результаты исследований, которые можно
получить в редакциях журналов и в службах, публикующих полные статьи.
Преимущества: позволяет получить наиболее полную информацию по вопросу, так как все данные, представленные в статье, доступны для читателя.
Недостатки первичной литературы заключаются в том, что читатель должен обладать соответствующими навыками оценки статей, а также иметь достаточно времени для внимательного прочтения и анализа.
Слайд 23
Что искать?
Перечень основных первичных информационных ресурсов:
Британский Медицинский

Журнал (British Medical Journal) http://www.bmj.com;
Ланцет (Lancet) http://www.thelancet.com/ ;
Журнал по Медицине Новой
Англии (New England Journal of Medicine) http://www.nejm.org ;
Журнал Американской Медицинской Ассоциации (Journal
of the American Medical Association) http://jama.ama-assn.org/ ;
Анналы Медицины Внутренних Болезней (Annals of Internal Medicine) http://www.annals.org/ .
Слайд 24
Что искать?
Вторичная литература — включает в себя реферативные

издания, в которых представлены ссылки и краткие обзоры статей.
Обычно это публикуется в бюллетенях, в электронных базах данных и
в Интернете.
Преимущества: легко доступная и простая для прочтения информация.
Недостатки: длительный период времени между исходной публикацией и переизданием в бюллетене или службой публикации рефератов.
Слайд 25
Что искать?
Перечень основных вторичных информационных ресурсов:
Медицинский Бюллетень

(Medical Letter) http://www.medicalletter.org/ ;
Австралийский Врач (Australian Prescriber) www.australianprescriber.com;
Журнальный Обзор (Journal Watch) Journal
Watch http://www.jwatch.org/ ;
Краткие обзоры статей в MEDLINE www.nlm.nih.gov и EMBASE http://www.embase.com/;
Краткие обзоры статей и оценки
Библиотеки Кохрейн (Cochrane Library) http://www3.interscience.wiley.com/cgi-bin/mrwhome/106568753/HOME;
Центр обзоров и распространения Centre for Review and Dissemination, включающий в себя материалы из баз данных DARE, HTA, NHS EEDhttp://www.crd.york.ac.uk ;
Национальные Институты Здоровья (NIH)— http://www.nih.gov/;
Краткие обзоры международных статей по ЛС (International Pharmaceutical Abstracts);
Всемирная организация здравоохранения (ВОЗ)— http://www.who.int/ ;
Администрация по контролю пищевых продуктов и лекарственных препаратов (FDA)— http://www.fda.gov/ ;
Агентство Исследований и Обеспечения Качества в Здравоохранении (AHRQ)— http://www.ahrq.gov/ ;
Центры по контролю и профилактике заболеваемости (CDC)— http://www.cdc.gov/ ;
Доказательства Национальной системы здравоохранения Великобритании NHS Evidence http://www.evidence.nhs.uk;
Национальная электронная библиотека по лекарственным средствам — сервис UK Medicines Information по лекарственным средствамhttp://www.nelm.nhs.uk/en/
Слайд 26
Что искать?
Третичные информационные источники — включают в себя

опубликованные учебники, которые могут быть прекрасным источником информации, если
при их написании использованы признанные и современные источники.
Преимущества: легко доступная информация,
не требуется много времени для прочтения и усвоения информации.
Недостатки: невозможность доступа к исходным источникам информации; субъективность, привносимая автором текста; устаревание информации вследствие значительного времени, которое требуется для публикации текста.
Слайд 27
Что искать?
Перечень основных третичных информационных ресурсов:
Мартиндейл: Экстра

Фармакопея (Martindale: The Extra Pharmacopoeia) платный ресурс – доступен
через сервисhttps://www.medicinescomplete.com;
Американская Служба Больничных Формуляров (American Hospital Formulary Service —
AHFS) — платный ресурс – доступен через сервисhttp://www.medicinescomplete.com;
База данных взаимодействия лекарственных средств Стоклис Stockley’s Drug Interaction — платный ресурс – доступен через сервисhttp://www.medicinescomplete.com;
Британский Национальный Формуляр (British National Formulary) http://www.bnf.org;
BNFC (British National Formulary for Children) http://www.bnfc.org;
Информация о ЛС для профессионалов: Фармакопея Соединенных Штатов (United States Pharmacopeia Dispensing Information (USP DI) Drug Information for the Health Care Professional);
Факты и Сравнения (Facts and Comparison) http://www.factsandcomparisons.com/
Слайд 28
имеется несколько баз данных, содержащих клинические руководства по лечению заболеваний:
Сайт

межрегиональной общественной организации «Общество фармакоэкономических исследований» http://www.rspor.ru/ ;
База данных Национальной службы
здравоохранения Великобритании (NHS) и Национального института качества здравоохранения и клинической
практики (NICE – National Institute for Health and Clinical Excellence): http://www.library.nhs.uk/guidelinesfinder/;
Вэб-сайт Американского Агентства исследований и качества системы здравоохранения (Agency for Healthcare Research and Quality (AHRQ), Департамента здравоохранения и социальной службы США (U.S. Department of Health and Human Services) — http://www.guideline.gov/;
Клинические руководства организации NICE (National Institute for Health and Clinical Excellence, Великобритания) — http://www.nice.org.uk/;
New Zealand Guidelines Group (Группа разработки руководств Новой Зеландии) — Guidelines Library — http://www.nzgg.org.nz/ ;
Australian National Health and Medical Research Council (Австралийский Национальный совет по медицинским исследованиям и здравоохранению): Clinical Practice Guidelines – http://www.nhmrc.gov.au;
Canadian Medical Association (Канадская медицинская ассоциация) — Infobase : Clinical Practice Guidelines – http://www.cma.ca;
Government of Victoria, Australia, Department of Human Services/Public Health Division : The Blue Book — Guidelines for the control of infectious diseases (Голубая книга – Руководства по контролю инфекционных заболеваний Подразделение общественного здравоохранения/ Департамент социальной службы Правительства Виктории, Австралия — http://www.health.vic.gov.au;
Health Canada (Здравоохранение Канады): Guidelines — http://www.hcsc.gc.ca/ahc-asc/legislation/guide-ld/index-eng.php;
Public Health Agency of Canada (Агентство общественного здравоохранения Канады: Guidelines – http://www.phac-aspc.gc.ca;
US Agency for Healthcare Research and Quality (Агентство Исследований и качества здравоохранения США: Clinical Practice Guidelines Online -http://www.ahrq.gov (архив);
Guidelines International Network (G-I-N) (Международная сеть клинических руководств) — http://www.g-i-n.net/ (требуется приобретение членства)
Слайд 30
Где искать?
Cochrane database of systematic reviews (Cochrane DSR)
Медицинские
базы данных
Слайд 31
Где искать?
Специализированные медицинские базы данных:
ACP Journal Club
Database of

abstracts of reviews of effects (DARE)
Слайд 32
Как искать?
При инициализации поиска с обзора третичных источников

полезным может оказаться сервис google scholar (scholar.google.com), позволяющий просматривать
онлайн большое количество справочников и учебников, в т.ч. их полнотекстовые
варианты.
На втором этапе информационного поиска, при определении систематических обзоров и оригинальных исследований, следует обратиться к специализированным базам данных.
Слайд 33
Информационный поиск может проводиться: для конкретной публикации –

достаточно ввести в запрос инициалы авторов и название работы;
с целью поиска могут быть использованы любые публикации, удовлетворяющие содержанию
запроса (скрининг информации) – требуется корректно составить информационный запрос. Скрининг информации может быть начат с набора в поисковой системе сочетания ключевых слов, которые отвечают тематике требуемых данных
Как искать?
Слайд 34
Критерии эффективности
Для оценки эффективности медицинского вмешательства используются специальные критерии, называемые точками клинической

эффективности. Различают конечные и суррогатные точки.
Слайд 37
Клиническая ситуация
Девочка 5 лет с острым

средним отитом.
Мать говорит, что уши у ребенка болели и
раньше, но иногда болезнь проходила сама собой , а иногда
врачи назначали антибиотики
Сформулируйте вопрос
Основные принципы доказательной медицины
Основные принципы доказательной медицины в онкологии
Доказательная медицина (ДМ) — фундаментальная медицинская наука, основным направлением которой является прогнозирование для конкретного пациента течения его болезни и последствий проводимого (планируемого) лечения на основании изучения клинических данных аналогичных больных с использованием строгих научных методов, обеспечивающих точность прогноза. В России эту науку называют чаще всего именно “доказательной медициной”, в то время как в англоязычных странах более распространено другое название — “клиническая эпидемиология”. Цель ДМ — разработка и применение таких методов клинического наблюдения, которые дают возможность избежать влияния систематических и случайных ошибок и получить максимально достоверный прогноз.
Количественный метод оценки лечения был предложен менее 200 лет назад, когда французский врач Пьер Луи подсчитал число случаев смерти и выздоровления при лихорадке в зависимости от применения кровопускания. Его осуждали за то, что он позволил себе на основе безжизненных цифр сеять сомнения в целительной силе пиявок, но в итоге его данные послужили причиной для пересмотра существовавших тогда методов лечения.
Среди отечественных основоположников ДМ необходимо отметить академика Н.Н. Блохина (1912—1993), уделявшего огромное внимание доказательности всех клинических результатов и выступавшего
^ С.Б. Петерсон*, А.И. Беневский*, В.Н. Чехонадский**
* Кафедра онкологии РГМУ ** ГУ Российский онкологический научный центр им. Н.Н. Блохина РАМН, Москва
непримиримым противником любых ненаучных методов врачевания, а также профессора И.И. Шатрова (1902—1977), который в своих работах излагает основные принципы ДМ и определяет рациональные основы сотрудничества врачей с математиками.
Традиционное клиническое мышление заключается в том, что если мы знаем механизм заболевания, то можем предсказать течение болезни и выбрать правильное лечение (на основе данных биохимии, анатомии, физиологии и других фундаментальных наук). Но механизмы развития заболеваний известны нам лишь отчасти, а на исход болезни влияют и многие другие факторы (генетические, физические, психологические, социальные и т.п.), поэтому такие прогнозы следует рассматривать только как клинические гипотезы, которые должны выдержать проверку в клинических испытаниях. Личный опыт врача тоже важен для принятия клинических решений. Однако ни один врач не обладает достаточным практическим опытом, чтобы распознать все трудноуловимые, длительно протекающие, взаимодействующие процессы, которые имеют место при большинстве хронических заболеваний.
Хотя личный опыт врача и знание механизмов развития заболевания, безусловно, важны, необходимо принимать во внимание следующие основные положения ДМ:
1) в большинстве случаев диагноз, прогноз и результаты лечения для конкретного больного однозначно не определены и по-
Доказательная медицина
тому должны быть выражены через вероятности;
2) эти вероятности для конкретного больного лучше всего оцениваются на основе предыдущего опыта, накопленного в отношении групп аналогичных больных;
3) поскольку клинические наблюдения проводятся на свободных в своем поведении больных, и делают эти наблюдения врачи с разной квалификацией и собственным мнением, результаты могут быть подвержены систематическим ошибкам, ведущим к неверным заключениям;
4) любые наблюдения, и клинические в том числе, подвержены влиянию случайности;
5) чтобы избежать неверных выводов, врачи должны полагаться на результаты исследований, основанных на строгих научных принципах и выполненных с использованием способов минимизации систематических и случайных ошибок;
6) сведение к минимуму систематических ошибок достигается правильной структурой (организацией) исследования, адекватной его задачам;
7) сведение к минимуму случайных ошибок достигается корректным статистическим анализом данных.
Взаимоотношения врача и пациента в рамках клинических исследований (КИ) регламентирует Хельсинкская декларация, принятая 18-й ассамблеей Всемирной медицинской ассоциации в 1964 г. и затем неоднократно пересмотренная (последняя редакция принята на 52-й ассамблее в Эдинбурге в 2000 г.).
В настоящее время считается общепризнанным, что неправильно проведенное (как при планировании, так и при анализе данных) КИ является неэтичным, поскольку пациенты при этом подвергаются неоправданному риску, неэффективно используются финансовые ресурсы и время исследователей, после публикации неверных результатов дальнейшие исследования направляются в неправильное русло, а их
применение в медицинской практике может нанести вред больным. Поэтому КИ нельзя проводить без участия специалиста по прикладной медицинской статистике уже на этапе планирования.
При планировании КИ необходимо заранее четко установить, прогноз какого исхода лечения мы будем стараться определить. Наиболее значимые клинические исходы:
• смерть;
• заболевание — набор симптомов, физи-кальных и лабораторных данных, отклоняющихся от нормы;
• дискомфорт — субъективно тягостные симптомы (боль, тошнота, одышка, зуд, шум в ушах и т.п.);
• инвалидизация — неспособность к обычной деятельности на работе или дома;
• неудовлетворенность — эмоциональная реакция на болезнь и проводимое лечение (тоска, гнев и др.).
Основные понятия ДМ
Популяции и выборки Популяция — большая группа людей, проживающих в определенном географическом регионе или обладающих некоторым признаком (например, старше 65 лет). Она может состоять из пациентов, госпитализированных в определенную клинику, или пациентов с определенным заболеванием (что чаще имеет место в КИ). Таким образом, можно говорить об общей популяции, госпитальной популяции или популяции пациентов с конкретным заболеванием.
Выборка — это часть популяции, полученная путем отбора. КИ обычно выполняются на выборках, и оценивать характеристики популяции приходится путем оценки этих характеристик в выборке.
Виды ошибок
Систематическая ошибка — это систематическое (неслучайное, однонаправленное) отклонение результатов от истинных значений. Наблюдение за больными (при
Основные принципы доказательной медицины
лечении и в процессе КИ) особенно подвержено систематическим ошибкам. Больные ведут произвольно: отказываются участвовать в исследовании; выбывают из исследования; меняют метод лечения и т.п. К тому же сам исследователь склонен верить в успех нового метода.
Основные категории систематических ошибок в КИ:
• ошибка, обусловленная отбором, возникает, когда сравниваемые группы пациентов различаются не только по изучаемому признаку, но и по другим факторам, влияющим на исход;
• ошибка, обусловленная измерением, возникает, когда в сравниваемых группах больных используются разные методы измерения;
• ошибка, обусловленная вмешивающимися факторами, возникает, когда один фактор связан с другим, и эффект одного искажает эффект другого.
В одном КИ могут присутствовать систематические ошибки всех трех категорий.
Случайная ошибка — отклонение результата отдельного наблюдения в выборке от истинного значения в популяции, обусловленное исключительно случайностью.
Систематическая ошибка вызывает отклонение оценки от истины либо в одну, либо в другую сторону. Случайная ошибка вызывает отклонение оценки от истины с равной вероятностью и в одну, и в другую сторону. Систематическую ошибку можно предотвратить, а случайную ошибку предотвратить нельзя.
Достоверность и обобщаемость
Достоверность определяется тем, в какой мере полученные результаты справедливы в отношении данной выборки. Это внутренняя характеристика выборки.
Обобщаемость — внешняя характеристика выборки, определяется тем, в какой мере результаты данного КИ применимы к другим группам больных.
Типы данных, норма и отклонение
Данные, полученные в результате клинических наблюдений, бывают трех типов: качественные, порядковые и количественные.
Качественные данные — это величины, которые нельзя расположить в естествен -ном порядке (например, пол, врожденные нарушения метаболизма и др.). Они могут описывать важные дискретные события: смерть, хирургическое вмешательство и т.п. Качественные данные, которые могут быть отнесены только к двум категориям, называются дихотомическими (или бинарными).
Порядковые данные — величины, которые могут быть расположены в естественном порядке или ранжированы (от малого до большого, от хорошего до плохого), но размер интервала между такими категориями не может быть выражен количественно. Примером служит стадия онкологического заболевания, степень сердечной недостаточности и т.п.
Количественные данные — это такие величины, которым присущ естественный порядок расположения с равными интервалами между последовательными значениями, независимо от их места на шкале. Количественные данные могут быть непрерывными и дискретными. Непрерывные могут принимать любое значение на непрерывной шкале, например большинство биохимических показателей крови, масса тела, артериальное давление и т.п. Дискретные данные всегда выражаются целыми числами, например число беременностей, рождений, абортов и т.п.
Данные всех этих типов могут быть охарактеризованы достоверностью, воспроизводимостью и вариациями измерений.
Достоверность измерений (точность оценки) показывает, в какой степени полученные данные соответствуют истинным значениям, т.е. действительно отражают оцениваемое явление.
Доказательная медицина
Таблица 1. Способы представления центральной тенденции и дисперсии
Способ Определение Преимущества Недостатки
представления
Центральная тенденция
Среднее
Медиана
Мода
Диапазон
значений
Стандартное
отклонение
Процентили,
децили,
квартили
Сумма полученных значений, деленная на число наблюдений
Точка, по обе стороны которой находится равное число наблюдений
Удобна для математической обработки
Не подвержена влиянию крайних значений
Наиболее часто встречающееся Проста для понимания значение
Характеристики рассеяния
Рассеяние от минимального Охватывает все значения до максимального значений в распределении
Абсолютная величина среднего арифметического отклонения индивидуальных значений от среднего значения
Доля наблюдений, находящихся в определенной части распределения
Удобно для математической обработки
Характеризуют “необычность” значения независимо от типа распределения
Подвержена влиянию крайних значений
Не слишком удобна для математической обработки
Иногда мода отсутствует, а иногда их бывает несколько
Сильно подвержен влиянию крайних значений
Не всегда пригодно
для описания негауссовых
распределений
Неудобны
для статистических расчетов
Воспроизводимость — вероятность того, что при повторных измерениях некоего устойчивого явления, сделанных разными людьми, на разных приборах, в разное время и в разных местах, будет получен один и тот же результат.
Вариации — это разница в результатах измерений, связанная с процессом измерений, биологическими изменениями, происходящими в организме в течение времени, и биологическими различиями между разными индивидуумами.
Частотные распределения для клинических показателей имеют разную форму и характеризуются центральной тенденцией и рассеянием (дисперсией), которые могут быть представлены различными способами (табл. 1).
Значения лабораторных показателей для здоровых и больных часто перекрываются. Вследствие этого, а также из-за относительно низкой распространенности пато-
логии в общей популяции часто бывает невозможно четко разграничить две группы пациентов по результатам однократного тестирования. Точка разделения, на которой заканчивается норма и начинается патология, выбирается произвольно и обычно связана с одним из трех критериев патологии — это состояние:
1) необычное с точки зрения статистики;
2) проявляется в виде болезни;
3) поддается лечению.
Диагноз
Для оценки эффективности диагностического теста строят так называемую четырехпольную таблицу и сравнивают результаты теста при наличии и отсутствии заболевания. Для простоты изложения мы заполним такую таблицу гипотетическими цифрами (табл. 2). Предположим, что были обследованы 149 пациентов; каждому из них тест проводился однократно. Всего
Основные принципы доказательной медицины
тест был положительным в 62 случаях, а отрицательным — в 87. Затем была проведена верификация диагноза с помощью некого “золотого стандарта”, позволяющего с абсолютной точностью определить наличие или отсутствие болезни, при этом болезнь выявлена у 37 человек, отсутствовала у 112. Полученные результаты были занесены в четырехпольную таблицу.
Если у пациента болезнь присутствует, и результат теста на наличие болезни положительный, то такие результаты называют истинноположительными (в числовом примере в табл. 2 таких результатов 27).
Если у пациента болезнь отсутствует, и результат теста на наличие болезни отрицательный, то такие результаты называют истинноотрицательными (в примере таких результатов 77).
iНе можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
Если у пациента болезнь присутствует, а результат теста отрицателен, то такие результаты называют ложноотрицательными (в примере таких результатов 10).
Если у пациента болезнь отсутствует, а результат теста положительный, то такие результаты называют ложноположительными (в примере таких результатов 35).
В современной научной литературе приняты 7 основных характеристик диагностического теста.
1. Чувствительность — показывает, в каком проценте случаев распознается болезнь. В рассматриваемом числовом примере
Бе = 27 : 37 = 73%.
2. Специфичность характеризует точность отрицательного результата, т.е. насколько отрицательный результат специфичен для отсутствия заболевания. В нашем примере:
Бр = 77 : 112 = 69%.
3. Распространенность заболевания:
Р = 37 : 149 = 25%.
4. Прогностическая ценность отрицательного результата теста:
-РУ = 77 : (10 + 77) = 88%.
5. Прогностическая ценность положительного результата теста:
+РУ = 27 : (27 + 35) = 44%.
6. Ложноотрицательные ошибки (ошибки первого рода, а-ошибки) — какой процент отрицательных результатов оказывается ложным:
а = 10 : (10 + 77) = 12%.
7. Ложноположительные ошибки (ошибки второго рода, Р-ошибки) — какой процент положительных результатов оказывается ложным:
Р = 35 : (27 + 35) = 56%.
Нетрудно заметить, что:
—РУ + а = 100%;
+РУ + р = 100%.
Частота и вероятность событий
В ходе КИ можно определить только частоту некоторых событий или эффектов, а для построения прогноза необходимо иметь не частоту, а вероятность. Для демонстрации различия между этими понятиями приведем пример из радиационной онкологии.
Появление лучевого повреждения нормальных тканей зависит от большого количества различных, до конца еще не изученных факторов. Поэтому в первом приближении можно считать, что оно носит случайный характер. Если вероятность появления изучаемого эффекта при облучении конкретного больного дозой Б составляет некоторую величину п, то по причинам чисто случайным в группе из N больных, облученных этой дозой, не будет диагностировано ни одного лучевого по-
Таблица 2. Четырехпольная таблица для оценки эффективности диагностического теста
Тест Болезнь
присутствует отсутствует
Положительный 27 35
Отрицательный 10 77
Доказательная медицина
Таблица 3. Количество больных в исследуемой группе без лучевых повреждений, необходимое для клинического обоснования низких вероятностей лучевых повреждений
Доверительная
Количество больных при заданной вероятности
5% 10% 15%
0,7 23 11 7
0,9 45 21 14
0,95 58 28 18
вреждения нормальных тканей с вероятностью:
Рс = (1 — п)»
Поэтому отсутствие лучевых повреждений в группе из N больных, облученных дозой Б, правильно может быть истолковано следующим образом: с доверительной вероятностью Р = 1 — РБ вероятность эффекта при данном воздействии составляет п < 1 — Р^ = 1 — (1 — Р)1^.
Отсюда следует, что отсутствие лучевых повреждений в группе из 100 больных означает лишь, что с доверительной вероятностью Р, равной 0,8; 0,9 или 0,95, вероятность такого эффекта составляет не более чем 1,6; 2,3 и 3% соответственно.
Это же выражение позволяет количественно оценить надежность клинического определения вероятности изучаемых отрицательных эффектов. Для расчета минимального количества больных в группе (^, необходимого, чтобы сказать, что отсутствие в этой группе лучевых повреждений свидетельствует о том, что вероятность эффекта при облучении дозой Б не превышает п с доверительной вероятностью Р, используется формула
1пРБ 1п(1 — Р)
N >——— = —————
^ 1п(1 — п) 1п(1 — п).
Результаты оценок, полученных с использованием этого выражения, представлены в табл. 3. Если новому методу облучения были подвергнуты 58 больных, и ни у
одного из них не было лучевых повреждений, то частота лучевых повреждений в исследуемой группе составляет 0%, а в отношении вероятности лучевых повреждений при таком методе облучения мы можем сказать только, что она не превосходит 5% с доверительной вероятностью 0,95.
Эффект локального излечения опухоли также зависит от большого количества различных причин, и поэтому в первом приближении можно считать, что и он носит случайный характер. Поэтому если вероятность локального излечения у больного в результате облучения дозой Б составляет некоторую величину V, то по причинам чисто случайным в группе из N больных, облученной этой дозой, будет определено N локальных излечений (100% частота локальных излечений) с вероятностью
РБ = VN.
Поэтому 100% частота локальных излечений в группе из N больных, облученных дозой Б, правильно может быть истолкована следующим образом: с доверительной вероятностью Р = 1 — РБ вероятность локального излечения при облучении дозой Б составляет
V> Р^ = (1 — Р)1^.
Таким образом, 100% частота локальных излечений в группе из 100 больных означает лишь то, что с доверительной вероятностью 0,90 или 0,95 вероятность локальных излечений V составляет не менее чем 97,7 или 95% соответственно.
Аналогично приведенному выше примеру с лучевыми повреждениями, можно оценить минимально необходимое количество больных в группе:
1пРБ 1п(1 — Р)
N >—-Б = ————
^ 1nv 1nv .
Если новому методу облучения были подвергнуты 58 больных, и у всех был достигнут полный эффект, то частота локальных излечений в исследуемой группе со-
Основные принципы доказательной медицины
ставляет 100%, а в отношении вероятности локальных излечений при использовании такого метода мы можем сказать только, что она составляет не менее 95% с доверительной вероятностью 0,95 (табл. 4).
Риск
Факторы риска связаны с повышением вероятности развития заболевания. Независимо от того, является ли некий фактор риска причиной заболевания, его присутствие позволяет прогнозировать вероятность возникновения болезни.
Воздействие большинства предполагаемых факторов риска нельзя изучать в эксперименте, поэтому обычно приходится проводить наблюдения, отслеживая воздействие факторов и оценивая частоту заболевания. Один из методов такого наблюдения состоит в отборе когорты, некоторые представители которой подвергаются воздействию фактора риска. Когорта — группа лиц, изначально объединенных каким-либо общим признаком (например, здоровые лица или больные с определенной стадией заболевания) и наблюдаемых в течение определенного периода времени, чтобы проследить, что с ними произойдет в дальнейшем. После периода наблюдения сопоставляют частоту развития заболевания у лиц, подвергавшихся и не подвергавшихся воздействию этого фактора. Хотя когортные исследования риска предпочтительны с научной точки зрения, этот подход не всегда можно применить на практике, поскольку он требует значительных затрат времени, сил и средств.
Прогноз
Прогноз — это описание течения заболевания с момента его начала. По сравнению с факторами риска прогностические факторы имеют относительно высокую распространенность и могут оцениваться даже на основании индивидуального клинического опыта.
Прогноз лучше всего описывается вероятностью возникновения исхода в любой момент развития заболевания. В принципе, это может быть сделано при наблюдении когорты больных до тех пор, пока изучаемый исход не наступит у всех, у кого он может произойти. Однако поскольку такой подход неэффективен, используется другой метод, называемый анализом дожития (анализом времени наступления события). При обработке этих данных следует использовать специальные методы, уменьшающие влияние систематических ошибок.
Все основные исходы лечения, анализируемые в клинической онкологии, подпадают под определение “данные типа времени жизни” (survival data). В статистическом смысле это понятие описывает пребывание объектов в интересующем исследователя состоянии в определенный момент времени. При анализе таких данных особый интерес представляет группа объектов (пациентов), для каждого из которых определено точное событие, часто называемое “отказом”. “Отказ” происходит после некоторого интервала времени для каждого объекта только один раз.
Данные о времени жизни n объектов обычно представлены набором соответствующих интервалов времени, рассматриваемых как случайные величины. Для описания распределения таких данных используют различные статистические функции.
Функция распределения (функция надежности) случайной величины, называе-
Таблица 4. Количество больных в исследуемой группе с полным эффектом, необходимое для клинического обоснования высоких вероятностей локальных излечений
Доверительная вероятность Р Количество больных при заданной вероятности 80% 90% 95%
0,8 7 15 31
0,9 10 22 45
0,95 13 28 58
Доказательная медицина
мая также кумулятивной функцией риска отказа, отражает вероятность того, что отказ произойдет через время, меньшее, чем 1:
Б(1) = Р(Т < 1).
Вероятность противоположного события, т.е. того, что отказ не произойдет за время, меньшее, чем 1, называется функцией дожития:
Б(1) = 1 — Б(1) = Р(Т > 1).
Функция плотности вероятности описывает кривую распределения по срокам жизни:
^1) = ёР(1)/Л.
Интенсивность смерти (функция риска) характеризует риск отказа в момент 1:
М1) = «1)/Б(1).
Для выявления факторов, влияющих на вероятность того или иного исхода лечения, строится регрессионная модель, основанная на типе распределения данных времени жизни. Если основная задача исследования состоит в изучении качественного влияния воздействующих факторов на время наступления исхода, то выбор модели не имеет решающего значения. В случаях, когда задача связана с относительно “тонкими” вопросами зависимости времени жизни от воздействующих факторов, требуется выбор адекватной модели.
Окончание статьи читайте в следующем номере журнала
АТМОСФЕРА
Т ■ гггі ■ Ли . « р ■ —
НЕНИНШ БСМЕЗНН ‘1
Начинается подписка на 2005 год на научно-практический журнал “Атмосфера. Нервные болезни”
Подписку можно оформить в любом отделении связи России и СНГ Журнал выходит 4 раза в год. Стоимость подписки на полгода по каталогу агентства “Роспечать” — 44 руб., на один номер — 22 руб.
Подписной индекс 81610.
Научно-популярный журнал “Нервы” —
это журнал для тех, кто болеет, и не только.
Основной задачей издания является информирование пациентов и среднего медицинского персонала о современных подходах к профилактике, диагностике и лечению заболеваний нервной системы. Читательская аудитория журнала “Нервы” — это в первую очередь пациенты, те люди, у кого имеются проблемы со здоровьем, в частности со стороны нервной системы, а также их родственники, которым необходима качественная информация для принятия решений по оказанию помощи своим близким. Журнал также будет интересен здоровым людям, заботящимся о своем здоровье и интересующимся достижениями современной медицины.
Слайд 1МЕНЕДЖМЕНТ ИССЛЕДОВАНИЙ
Дизайны исследований
Жамалиева Л.М.
Отдел непрерывного профессионального развития
и доказательной медицины

Слайд 2 Дизайн или структура исследования – общая схема
проведения исследования
ОСНОВНЫЕ ВОПРОСЫ, ОПРЕДЕЛЯЮЩИЕ ДИЗАЙН ИССЛЕДОВАНИЯ
С
какой целью проводится исследование?
Имеет ли проблема научное или клиническое значение?
Каков наиболее походящий план исследования для достижения поставленной цели?

Слайд 3ОСНОВНОЙ ВОПРОС ИССЛЕДОВАНИЯ
Связано ли состояние с экспозицией?
Э Б
экспозиция
любой исход
Слайд 4ДВЕ КАТЕГОРИИ ИЗУЧАЕМЫХ ИСХОДОВ (OUTCOME)
Клинически значимые состояния
или события
выздоровление, качество жизни, инвалидизация, смерть
Косвенные
критерии оценки исхода
лабораторные показатели, данные инструментальных исследований
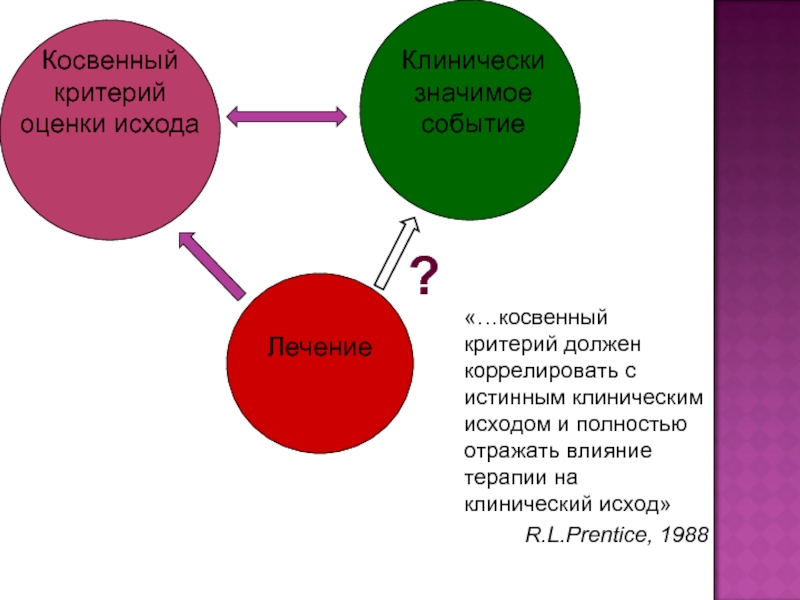
Слайд 5«…косвенный критерий должен коррелировать с истинным клиническим
исходом и полностью отражать влияние терапии на
клинический исход»
R.L.Prentice, 1988
Слайд 7ДВА КЛАССА
Методы исследований делят на две
большие группы:
Качественные
Количественные

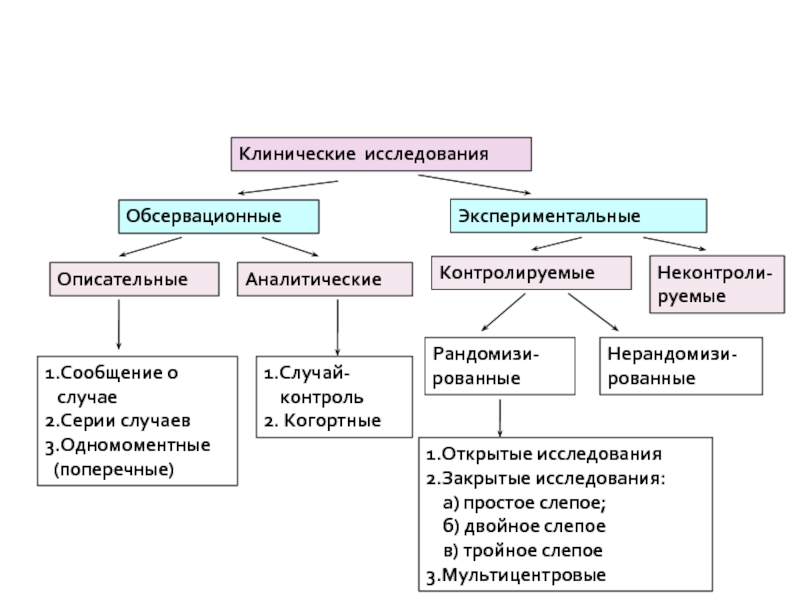
Слайд 8КЛАССИФИКАЦИЯ КЛИНИЧЕСКИХ ИССЛЕДОВАНИЙ
Клинические исследования
Обсервационные
Экспериментальные
Описательные
Аналитические
1.Сообщение
о
случае
2.Серии случаев
3.Одномоментные
(поперечные)
1.Случай-
контроль
2. Когортные
Контролируемые
Неконтроли-руемые
Рандомизи-рованные
Нерандомизи-рованные
1.Открытые исследования
2.Закрытые исследования:
а) простое слепое;
б) двойное слепое
в) тройное слепое
3.Мультицентровые
Слайд 9ТИПЫ ИССЛЕДОВАНИЙ
Первичные:
Описательные
Проявления и исходы
Аналитические
Связь экспозиции и
исхода
Проспективные и ретроспективные (сбор данных)
Обсервационные и экспериментальные
Наличие или отсутствие болезни к началу исследования
С группой сравнения или без нее
Вторичные:
Систематические обзоры
Мета-анализы

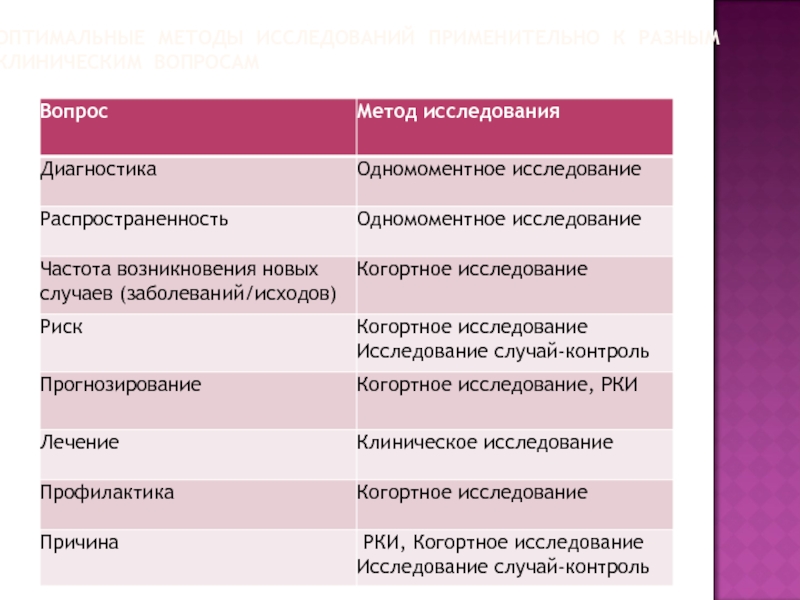
Слайд 10ОПТИМАЛЬНЫЕ МЕТОДЫ ИССЛЕДОВАНИЙ ПРИМЕНИТЕЛЬНО К РАЗНЫМ КЛИНИЧЕСКИМ
ВОПРОСАМ
Слайд 11ИССЛЕДОВАНИЕ СЕРИЙ СЛУЧАЕВ
(CASE SERIES)
Описание серии случаев
– исследование одного и того же вмешательства
у отдельных последовательно включенных больных без группы контроля. Например, сосудистый хирург может описать результаты реваскуляризации сонных артерий у 100 больных с ишемией головного мозга. Позволяет изучить закономерности в течении заболевания
Главный недостаток – отсутствие группы сравнения

Слайд 12НЕДОСТАТКИ ИССЛЕДОВАНИЯ «СЛУЧАЙ-КОНТРОЛЬ»
Ретроспективный характер не позволяет достоверно
регистрировать временные соотношения между явлениями
Возможны погрешности в
оценке достоверности воздействия
«Искусственный» подбор групп сравнения

Слайд 13ИССЛЕДОВАНИЯ «СЛУЧАЙ-КОНТРОЛЬ»
(CASE-CONTROL STUDY)
Исследование, структура которого предусматривает
сравнение двух групп участников с развившимся и
не развившимся клиническим исходом (обычно неблагоприятным) с целью выявления различий во влиянии определенных факторов риска на развитие этого клинического исхода. Такая структура исследования наиболее пригодна при попытках определить причину возникновения редко встречающихся заболеваний, например, развитие нарушений со стороны ЦНС у детей после применения коклюшной вакцины.

Слайд 14ИССЛЕДОВАНИЕ «СЛУЧАЙ-КОНТРОЛЬ»
популяция
«Контроль» — заболевание отсутствует
«Случай» —
заболевание есть
Фактор риска или воздействие
Есть
Нет
Есть
Нет
А н а м н е з
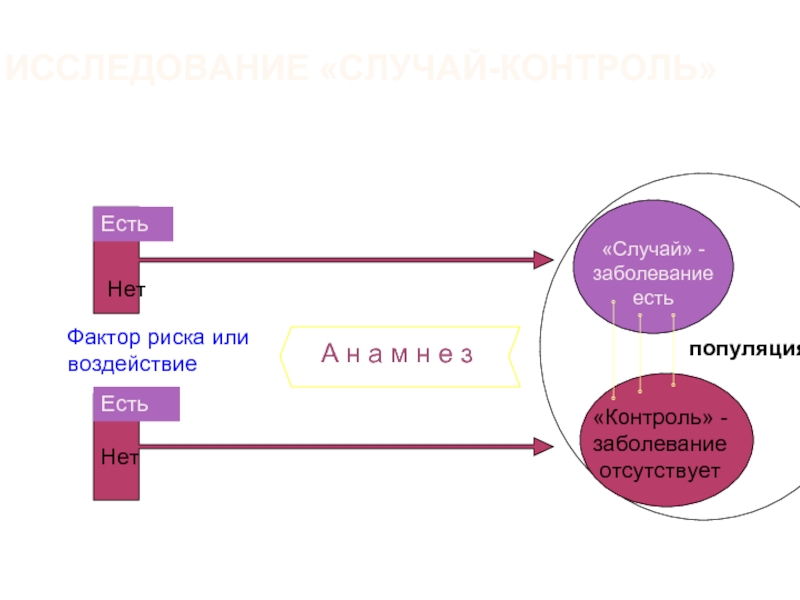
Слайд 15ПОПЕРЕЧНОЕ ИССЛЕДОВАНИЕ (CROSS-SECTIONAL STUDY)
Поперечное исследование (распространенность).
Данные
собираются в определенный момент времени
Типы: Распространенности
заболевания или исхода
Изучение течения заболевания, стадийности
Отвечают на вопрос «Сколько?»

Слайд 16ПРОСПЕКТИВНЫЕ КОГОРТНЫЕ ИССЛЕДОВАНИЯ (COHORT STUDIES)
Подбирается группа пациентов
на предмет сходного признака, которая будет прослежена
в будущем.
Начинается с предположения фактора риска или исхода. Подвергшиеся воздействию ФР и Не подвергшиеся воздействию.
Проспективное во времени, определение искомых факторов в экспонированной группе.
Отвечает на вопрос «Заболеют ли люди, если они подверглись воздействию фактора риска?» В основном – проспективные, но встречаются и исторические когортные ретроспективные).

Слайд 17Проспективные когортные исследования (cohort studies)
Лучший вид
клинических исследований для тех случаев, когда эксперимент
невозможен (исследование факторов риска, прогноза заболевания)
Главный недостаток когортных исследований – для изучения редких исходов требуется наблюдение больших групп в течение длительного времени
Фремингемское исследование (США): для установления связи факторов риска (повышенное АД, гиперхолестеринемия, сахарный диабет, курение, гипертрофия левого желудочка) и риска развития ИБС когорта из 5209 человек наблюдалась в течение 30 лет

Слайд 18РАНДОМИЗИРОВАННОЕ КОНТРОЛИРУЕМОЕ ИСПЫТАНИЕ
«золотой стандарт» любого
метода диагностики и лечения
обычно это исследование, в
котором участников в случайном порядке (рандомизированно) распределяют в две группы — основную (где применяется изучаемое вмешательство) и контрольную (где применяется плацебо или другое вмешательство.
такая структура исследования позволяет сравнить эффективность вмешательств.
При правильной организации позволяет свести к минимуму систематические ошибки

Слайд 19
РАНДОМИЗИРОВАННОЕ КЛИНИЧЕСКОЕ ИСПЫТАНИЕ
Популяция
Выборка
Вмешательство
Отсутствие вмешательства
Улучшение есть
Улучшения нет
Улучшение есть
Улучшения
нет
Основная группа
Контрольная группа
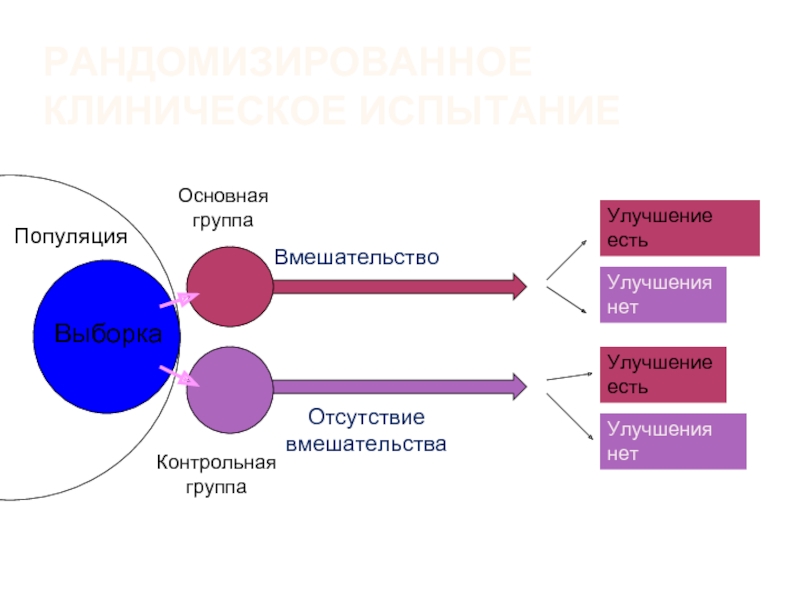
Слайд 20СТРУКТУРА ИССЛЕДОВАНИЯ
Наличие контрольной группы
Ясные критерии включения и
исключения больных, однородность групп
Размер выборки
Рандомизация
«Слепое» лечение,
«слепая» оценка результатов
«Жесткие» критерии эффективности

Слайд 21КОМПОНЕНТЫ ЛЕЧЕБНОГО ЭФФЕКТА, НАБЛЮДАЕМОГО ВРАЧОМ
Естественная редукция симптомов
Желание
пациента «помочь» врачу (эффект Готорна)
Плацебо-эффект
Специфическое лечебное действие

Слайд 22
Цель РКИ – оценить специфический («биологический») лечебный
эффект

Слайд 23СИСТЕМАТИЧЕСКИЕ ОБЗОРЫ
(SYSTEMATIC REVIEWS)
научные исследования, в которых синтезируются
результаты оригинальных клинических исследований

Слайд 24СИСТЕМАТИЧЕСКИЕ ОБЗОРЫ
Повышают достоверность научных фактов путем увеличения
статистической мощности объединенных исследований
Дают обобщенную оценку исследований
однотипных вмешательств с различающимися результатами
Позволяют уменьшить объем информации, предназначенной для конечного пользователя – врача

Слайд 26ЭТАПЫ СОСТАВЛЕНИЯ СИСТЕМАТИЧЕСКОГО ОБЗОРА
Поиск всех публикаций по
теме обзора
Выявление из всех имеющихся публикаций наиболее
надежных в плане строгости методики
Оценка соответствия статьи заранее установленным критериям качества
Объединение результатов исследований:
— качественное
— количественное — мета-анализ
Оценка результатов

Слайд 27МЕТА-АНАЛИЗ
Может быть частью систематического обзора или
это
дополнительные исследования
Систематический обзор
Мета-анализ
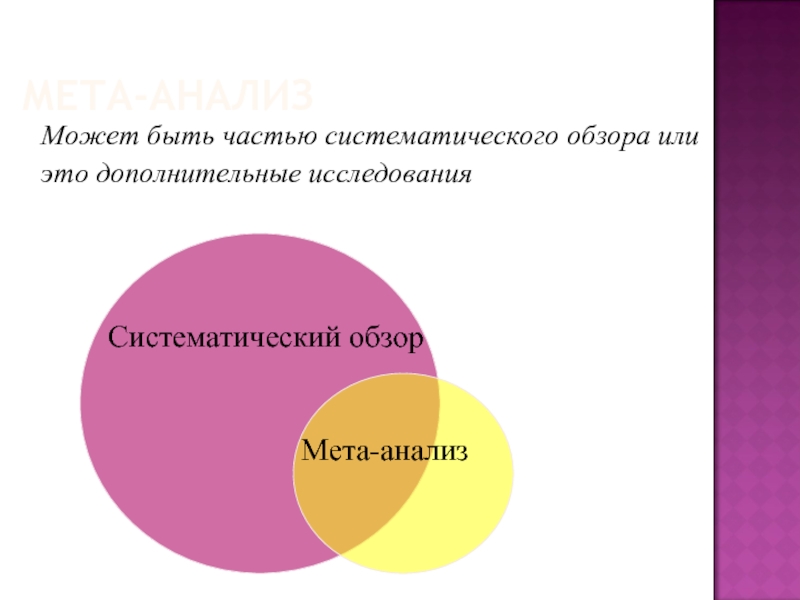
Слайд 28ГРАФИЧЕСКОЕ ПРЕДСТАВЛЕНИЕ РЕЗУЛЬТАТОВ МЕТА-АНАЛИЗА

Слайд 30
Название обзора, с чем
сравнение, что
принимается
за исход
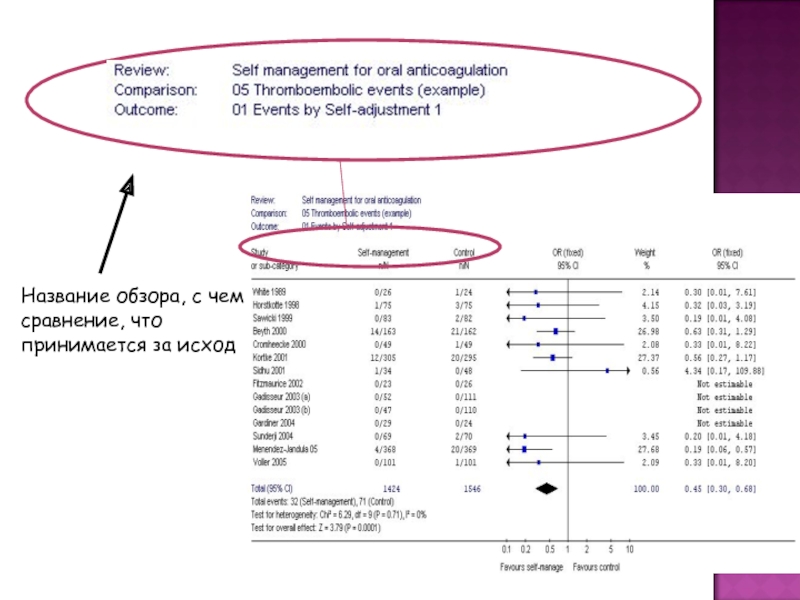
Слайд 31
На горизонтальной линии
шкала эффекта лечения
(польза в
основной группе
и в группе контроля)

Слайд 32
Вертикальная линия в центре
там, где лечение и
контроль
имеют одинаковую эффективность,
нет различий между ними
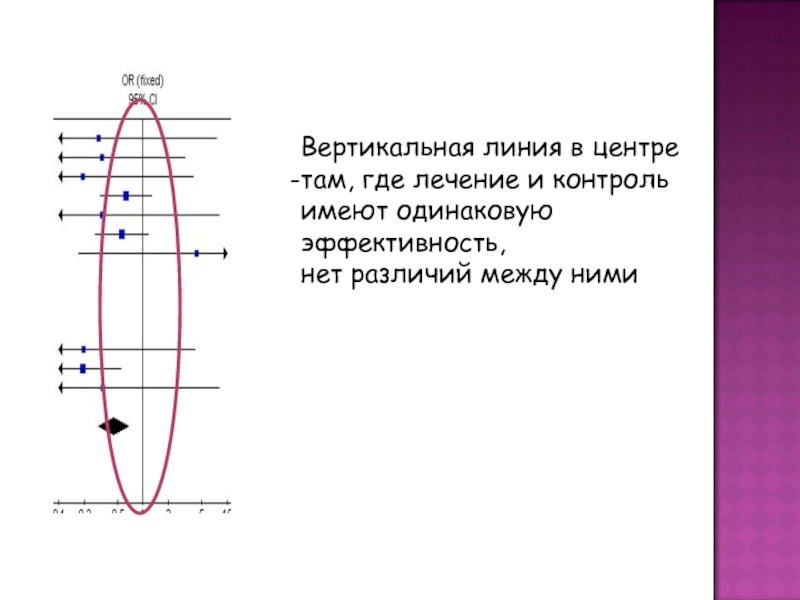
Слайд 33исследования
Численность в группах
Лечения и контроля
Это — вес
%, данный этому
исследованию в объединенном
анализе
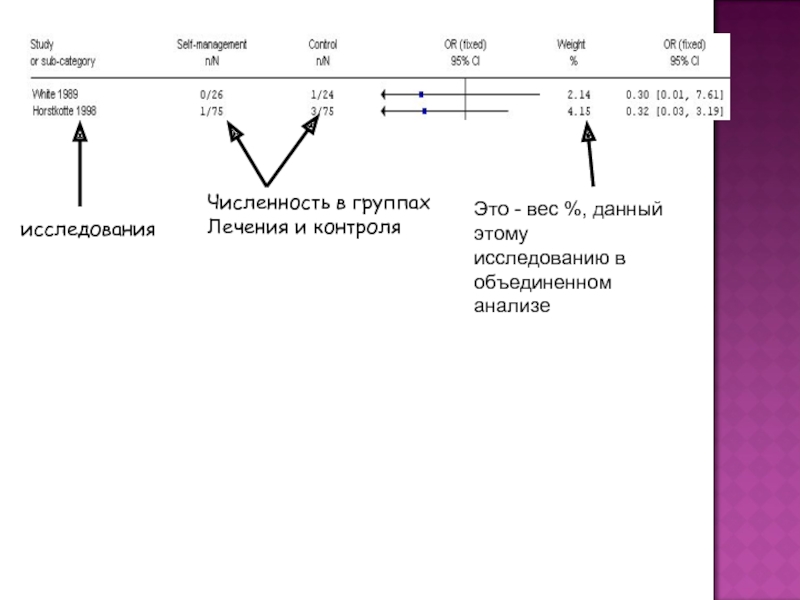
Слайд 34
какая статистическая величина
использовалась (здесь:ОШ)
Данные, показанные в
графе,
также даны в цифровой форме
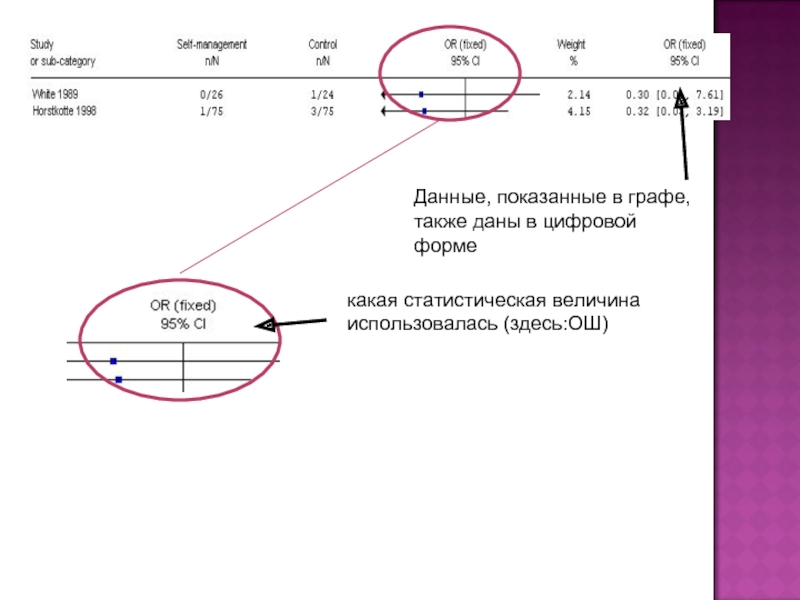
Слайд 35Объединенному анализу дают алмазную форму,
где самый
широкий бит в середине расположен
в расчетном
лучшем предположении, и горизонтальная ширина- доверительный интервал
Интерпретация:
Если доверительный интервал пересекает вертикальную линию
(отсутствие эффекта), это эквивалентно высказыванию, что мы не нашли статистически существенного различия в эффектах этих двух
вмешательств

Слайд 36ИССЛЕДОВАНИЯ МЕТОДОВ ДИАГНОСТИКИ

Слайд 37ХАРАКТЕРИСТИКИ ДИАГНОСТИЧЕСКОГО МЕТОДА (1)
Чувствительность теста – доля
лиц с положительным результатом теста в популяции
с изучаемым заболеванием
Специфичность теста – доля лиц с отрицательным результатом теста в популяции без данного заболевания

Слайд 38ИССЛЕДОВАНИЕ ХАРАКТЕРИСТИК ДИАГНОСТИЧЕСКОГО МЕТОДА
a b
c d
Чувствительность =
a / (a+b)
Специфичность = d / (c+d)
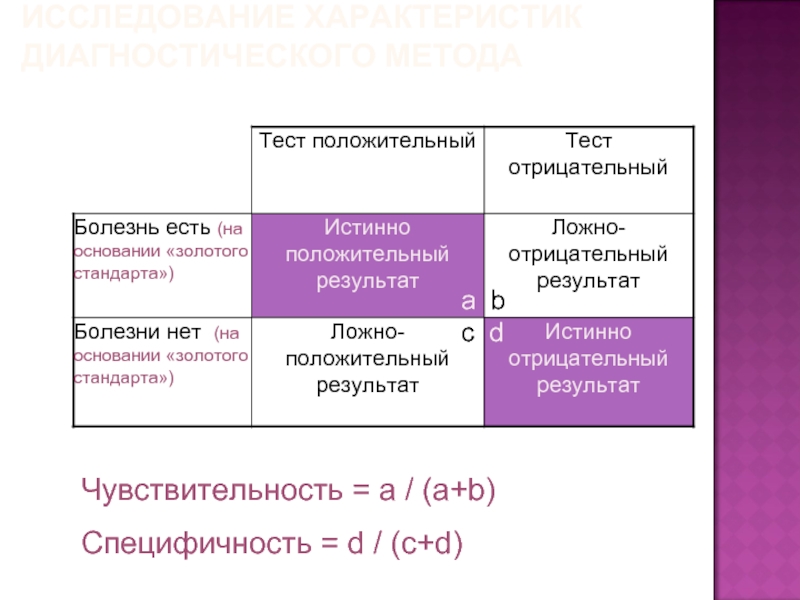
Слайд 39ХАРАКТЕРИСТИКИ ДИАГНОСТИЧЕСКОГО МЕТОДА
Прогностическая ценность положительного результата теста
– вероятность заболевания при положительном результате теста
Прогностическая
ценность отрицательного результата – вероятность отсутствия заболевания при отрицательном результате теста

Слайд 40
Нарастание знаний
о болезни и
экспозиции
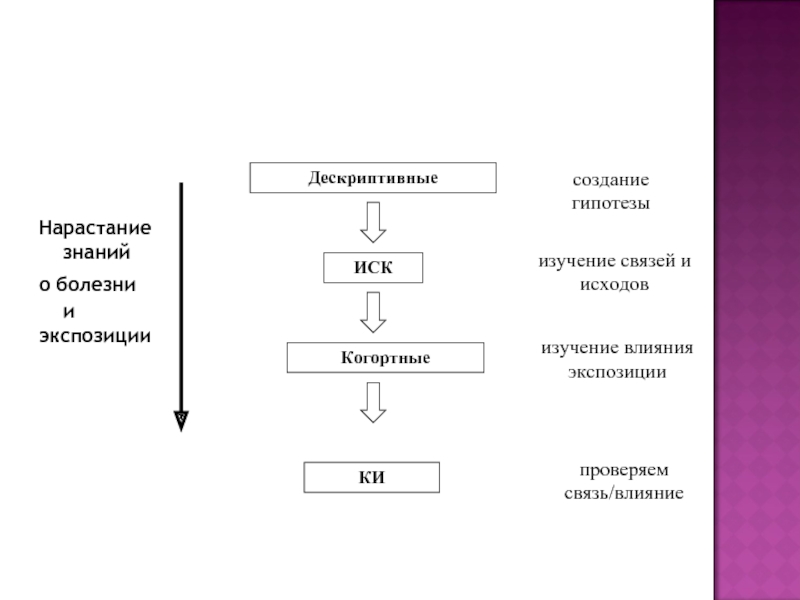
Слайд 41ЗАДАЧИ В ЭКСПЕРИМЕНТАЛЬНЫХ ИССЛЕДОВАНИЯХ
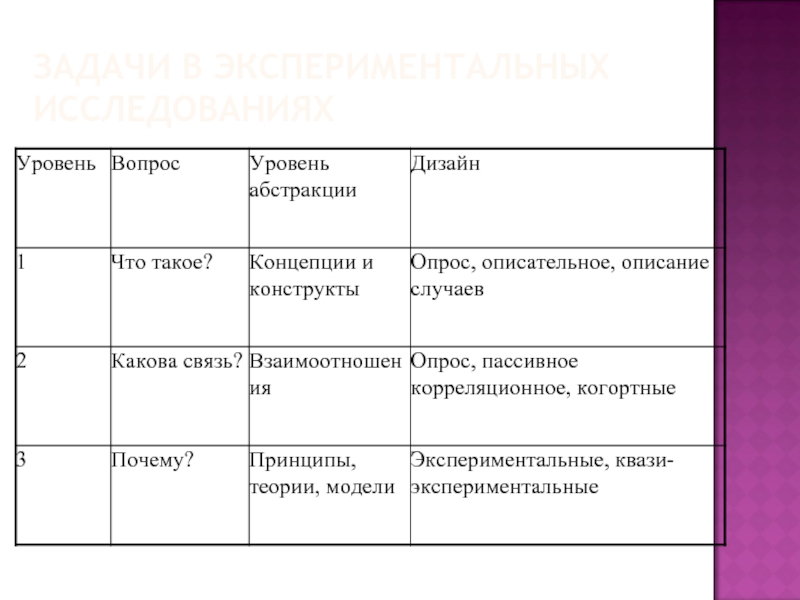
Слайд 42ЦЕЛЬ ИССЛЕДОВАНИЯ ДОЛЖНА ОПРЕДЕЛЯТЬ ВЫБОР ПЛАНА ИССЛЕДОВАНИЯ

Слайд 43ИЗМЕРЕНИЕ
Измерение явлений изучаемого мира – сложная
задача
Измерения должны быть валидными, т.е измерять то,
для чего они предназначены, и надежными (воспроизводимыми)
Мы ожидаем от средств измерения:
Сходимости (repeatability) – малые расхождения в оценках, даваемых людьми – согласие;
Правильности – тест может давать неточные результаты, но в среднем соответствующие истине;
Точности – каждый результат его применения близок к истине. У такого теста малы систематические и случайные ошибки, т.е высоки сходимость и правильность

Слайд 44ПРАВИЛЬНОСТЬ И ТОЧНОСТЬ ИЗМЕРЕНИЙ
Чем кучнее, тем выше
точность
(но не правильность)
Чем ближе к центру,
тем
выше правильность
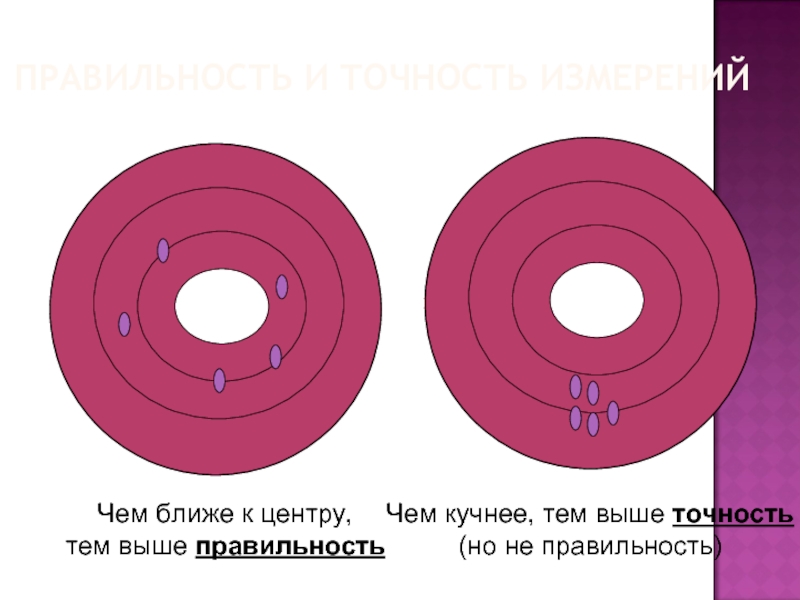
Слайд 45ВАЛИДНОСТЬ (ДОСТОВЕРНОСТЬ)
Валидность – степень, в которой измеряемое
нами соответствует тому, что мы хотим измерить
Внутренняя
валидность – степень, в которой результат исследования в выборке соответствует популяции

Слайд 46НАДЁЖНОСТЬ
— один из критериев качества теста, его
устойчивость по отношению к погрешностям измерения.
Два вида надёжности:
Устойчивость результатов теста или ретестовая надежность – возможность получения одинаковых результатов у испытуемых в различных случаях, определяется с помощью повторного тестирования (ретеста)
Внутренняя согласованность определяется связью каждого конкретного элемента теста с общим результатом, тем, насколько каждый элемент входит в противоречие с остальными, насколько каждый отдельный вопрос измеряет признак, на который направлен весь тест.

Слайд 47НАДЕЖНОСТЬ И ВАЛИДНОСТЬ
Высокие Н и В
Низкая Н
хорошая
В
Высокая Н
низкая В
Низкие Н и В
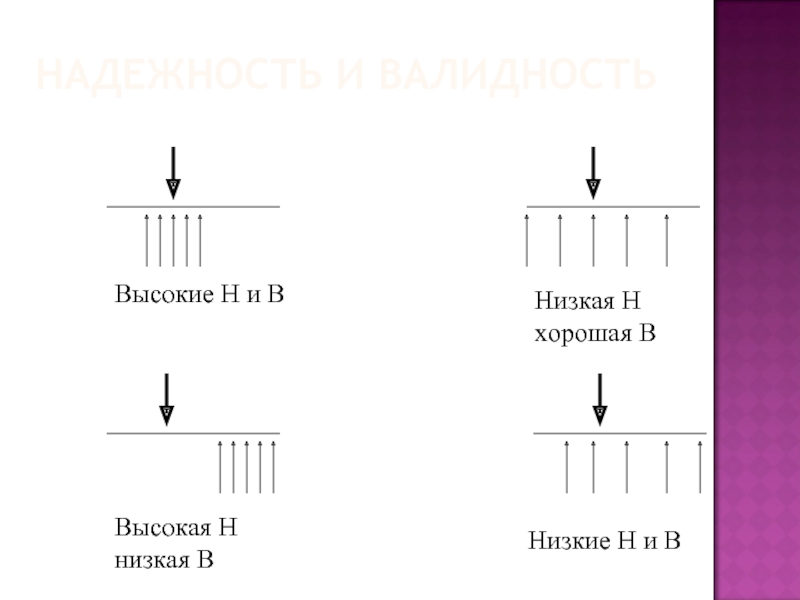
Слайд 48CИСТЕМАТИЧЕСКИЕ И СЛУЧАЙНЫЕ ОШИБКИ
Систематические ошибки обусловливаются причинами,
действующими вполне определённым образом, например, смещение стрелки
ненагруженных весов относительно нулевой отметки на некоторую постоянную величину Δm. Они могут быть устранены или достаточно точно учтены.
Случайные ошибки вызываются большим числом отдельных причин, действующих в каждом отдельном измерении различными способами, например, незаметные глазу колебания чаши весов, потоки воздуха, толчки фундамента здания, в котором стоят весы. Эти ошибки полностью исключить невозможно.
Δ = Δсл + Δсист

Слайд 49СИСТЕМАТИЧЕСКИЕ ОШИБКИ
Ошибка выборки
Отбора
Наблюдения
Памяти
Измерения
Отклика
Распределения
Интервьюера
…

Слайд 50• Систематическая ошибка, обусловленная отбором(selection bias), возникает, когда
сравниваемые группы пациентов различаются не только по
изучаемому признаку, но и по другим факторам, влияющим на исход.
• Систематическая ошибка, обусловленная измерением(measurement bias), возникает, когда в сравниваемых группах больных используются разные методы измерения.
• Систематическая ошибка, обусловленная вмешивающимися факторами(confounding bias), возникает, когда один фактор связан с другим, и эффект одного искажает эффект другого.

Слайд 51Отклонение результата (отдельного) наблюдения в выборке от
истинного значения в популяции, обусловленное исключительно случайностью,
называется случайной вариацией.

